- Thermal Properties of Lyocell Fibers by Activation Energy and Pretreatment During Oxidation
Department of Environmental Engineering, Anyang University, Anyang 14028, Korea
*Department of Chemical Engineering, Hanyang University, Seoul 04763, Korea
- 라이오셀 섬유의 활성화 에너지 및 안정화 시 전처리 조건에 따른 열적 특성 분석
안양대학교 환경공학과, *한양대학교 화학공학과
Oxidation process is
considered to be an essential process for a successive carbonization of fibers.
Herein, adequate pretreatment is necessary for cellulose fibers with their
known characteristics to have weight loss and thermal shrink after oxidation
process. In this study, we first pre-treated lyocell based precursor with H3PO4,
NaCl and KMnO4 with a variation of time. Thereafter, we finally
developed the sample form as activated carbon fibers. With thus-produced samples,
we observed surface chemical properties, thermal stability, and thermal
pyrolysis. Further, more appropriate method between Friedman and Kissinger was
also evaluated by using activation energy as a main constant. With promising
results, thermal properties and the value of Tpeak have
increased as pretreatment time of lyocell fibers increases. Lastly, Friedman
analysis was found to be more preferable than Kissinger analysis with its high
regression coefficients.
안정화 공정은 섬유의 물리화학적 구조변화를 야기하여 안정성
부여 및 후속공정에서 성공적인 섬유의 탄소화를 위한 전 단계로서 필수적인 공정 중 하나이다. 여기에서, 셀룰로오스계 섬유는 필연적인 중량 감소 및 열수축이 동반되기 때문에 안정화 시 적절한 전처리 조건이 선행되어야
우수한 열적 특성을 기대할 수 있다. 본 연구에서는 셀룰로오스계 중 라이오셀 전구체를 H3PO4, NaCI 및 KMnO4를
각기 다른 시간 동안 함침한 뒤, 활성탄소섬유 형태로 제조하였다. 제조된
샘플들을 바탕으로 표면구조, 열안정성 및 열분해 거동 등의 열적 특성을 분석하였다. 또한 도출된 활성화 에너지를 주요 상수로 라이오셀 섬유에 적합한 분석방법 또한 비교 제시하였다. 실험결과, 라이오셀 섬유는 함침시간이 길어질수록 섬유의 내열성이
향상되었으며 승온속도가 증가함에 따라 Tpeak 값 또한 증가하였다. 분석 방법의 경우, Friedman 분석방법이 Kissinger 분석방법 대비 높은
신뢰도를 보여주었다.
Oxidation process is considered to be an essential process
for a successive carbonization of fibers. Herein, we first pre-treated lyocell
based precursor with H3PO4, NaCl and KMnO4
with a variation of time. Thereafter, we finally developed the sample form as
activated carbon fibers. With thus-produced samples, we observed surface
chemical properties, thermal stability, and thermal pyrolysis.
Keywords: lyocell fiber, oxidation, pretreatment, thermal properties, activation energy
안정화 공정은 섬유제조
공정에 있어 필수적인 공정 중 하나이며, 전구체 섬유의 불융화를 통한 구성분자의 열분해를 감소시킴으로써 최종 생산품의 수율을 높이는 역할을 한다.1
안정화 공정은 산소확산이 반응을 유도하는 데 있어 전제조건이 되는 공정조건에 따른 지속시간이 대체적으로 긴 편이다. 따라서 전구체 섬유의 안정화
공정 동안 발생되는 물리화학적 변화에 따른 정량화에 대한 연구가 광범위하게 이루어지고 있다.2 섬유의 다양한 전구체 중 라이오셀은
셀룰로오스계라는 이점으로 인해 기존의 PAN(polyacrylonitrile) 또는 pitch대비 저렴한 가격으로 탄소섬유 등에의 적용이 활발히
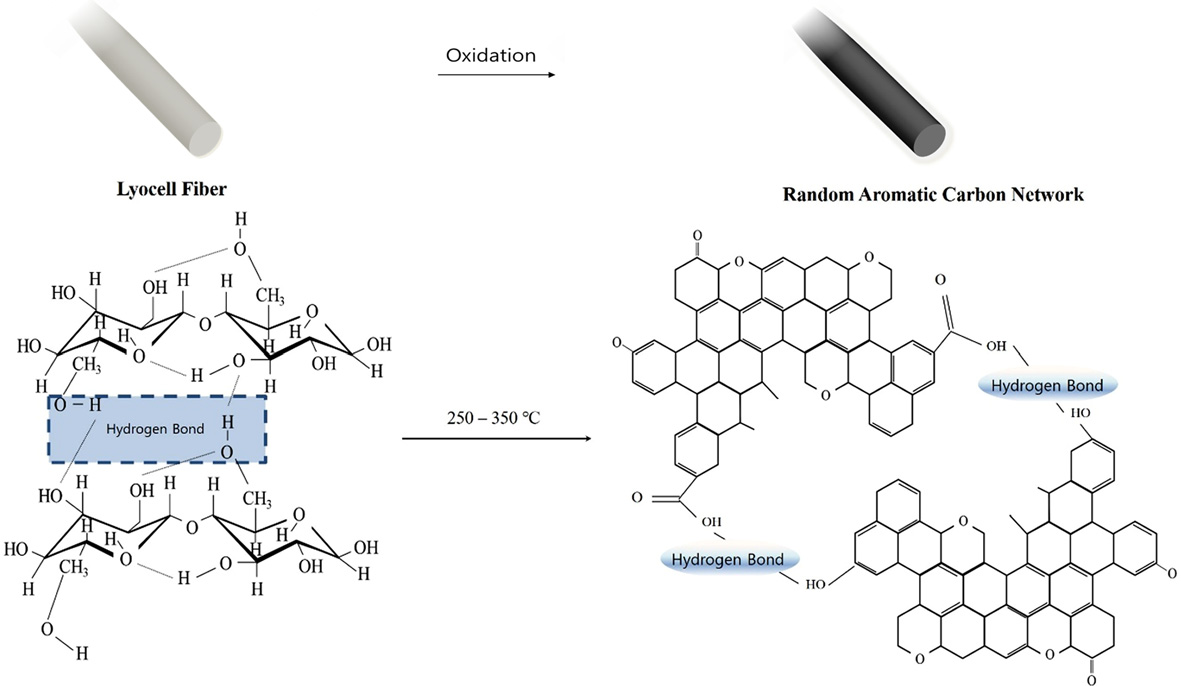
검토되고 있다.3 셀룰로오스계 섬유의 열분해는 주로 250~350 ℃ 사이에서 발생한다.4 셀룰로오스계 섬유의 열분해는 휘발성 가스, 타르 및 잔여 코크스의
형성을 초래하고, 동시다발적으로 발생하는 여러 형태의 화학반응 및 고분자 구조의 파괴가 두드러지게 나타난다.5 라이오셀 전구체
역시 대부분의 화학반응이 상기 온도조건 하에서 진행되고, 이때의 화학반응은 섬유의 질량감소, 화학구조 변화 등의 물리화학적 특성을 동반한다.6
Tang과 Bacon은 선행논문에서 셀룰로오스계 섬유는 온도변화에 대한 중량감소 경향을 다음과 같이 세 영역으로 세분하였다.7
첫째, 250 ℃ 이하의 영역에서는
구조 상에 존재하는 수소와 하이드록시기로부터 H2O 분자가 화학적으로 이탈하는 분자 내 탈수화 반응이 일어나며, 여기에서
C=O와 C=C 결합이 해리된다. 둘째, 250~350 ℃ 영역에서는 본격적인
열분해가 시작되는 단계로, 이 때 열분해는 C-O와 C-C 결합의 분해로부터 초래된다. 이 과정에서 비교적 많은 타르가 형성되고 H2O,
CO 및 CO2가 발생한다. 마지막으로 350 ℃ 이후의 영역에서는 수소제거와 함께 축합반응이 일어나며, 대상 전구체는 방향족 구조가 증가한 흑연과 같은 구조로
서서히 변환된다. 여기에서, 대상 전구체는 초기 중량 대비 약 90% 이상이 손실된다. 요약하면, 라이오셀 전구체의 대부분의 물리화학적 반응은
350 ℃ 이하의 낮은 온도영역에서 일어나기 때문에 상기 영역에서의 열처리 공정 최적화에 의한 물리화학적 제어가 내열화
공정의 핵심이라고 할 수 있다(Figure 1).
라이오셀 전구체는
온도뿐만 아니라, 노출시간에도 영향을 받는다. 350 ℃ 이상에서는 탄소의
방향족화 및 흑연구조의 형성이 서서히 진행되며, 이는 열처리 시간이 길어질수록 추가적 질량감소 및 탄소함량비의 증가를 가져온다. 본 연구에서는
라이오셀 전구체에 근거한 활성탄소섬유(ACF, activated carbon fiber)를 H3PO4,
NaCI 및 KMnO4를 각기 다른 시간 동안 함침하여 제조하였다. H3PO4는 섬유의
난연성에 기여하며, 이외에도 기공 형성제로서 작용한다. NaCl 및 KMnO4는 탄소내부 기공생성 및 수율상승에 기여한다고
보고된 바 있다. 본 연구에서 각기 다른 함침시간을 통해 제조된 라이오셀 섬유의 안정화 여부는 표면구조, 열안정성 및 열분해 거동분석을 통해 고찰하였다.
이외에도 활성화 에너지를 주요상수로 활용한 분석 결과를 통해, 라이오셀 섬유의 물리화학적 특성을 개선할 수 있는 최적조건 및 보다 높은 신뢰도의
분석방법 또한 비교 제시하였다.
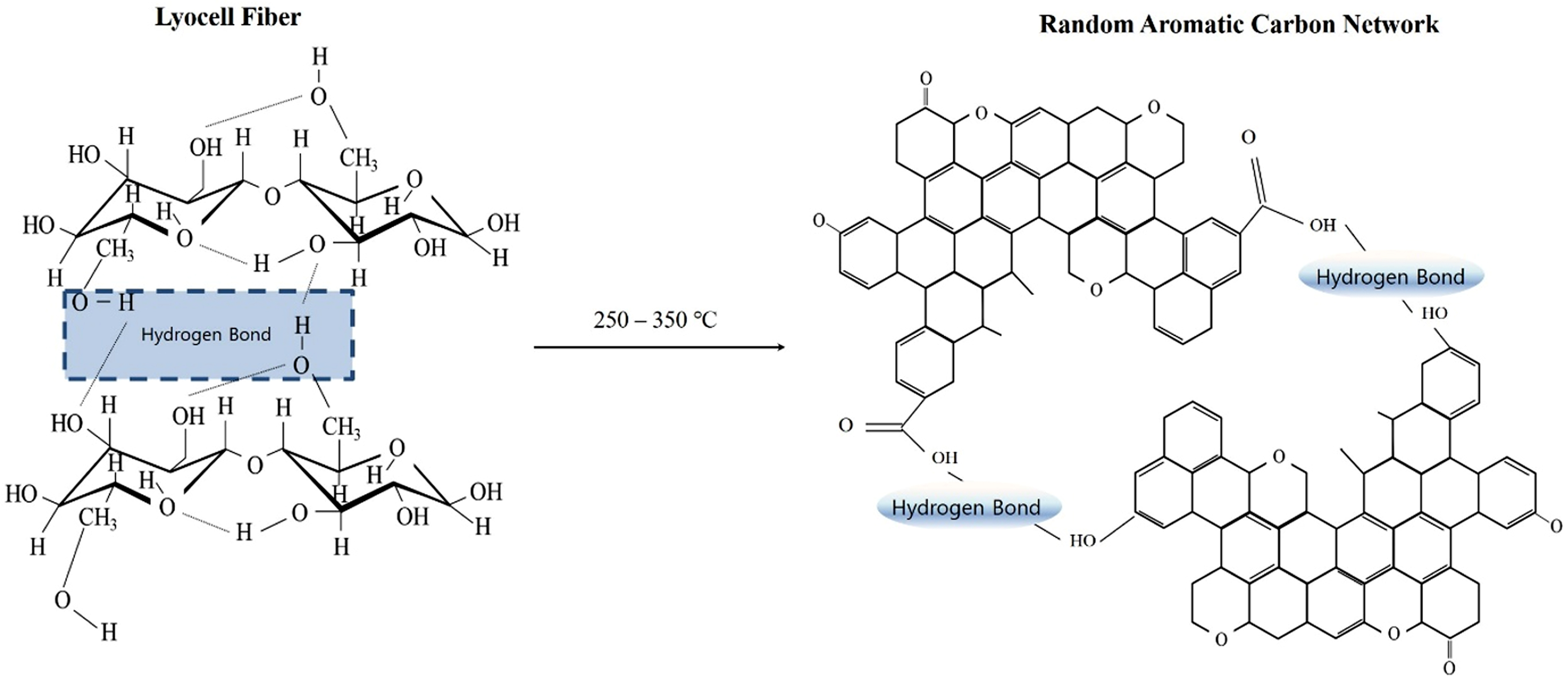
|
Figure 1 Possible physiochemical shift of lyocell precursors after the oxidation. |
라이오셀 전구체 기반 활성탄소섬유 제조. 안정화 공정은 전처리 공정의 후속으로 전처리 조건에 따라
최적 공정의 확립이 요구된다. 본 연구에서는 공기 분위기에서 승온속도 10 ℃/min으로 260 ℃까지 승온 후
1시간 동안 진행하였다(Figure 2). 전처리 용액의 경우, 선행 논문에서 기수행된 최적의 조건을 근거로 Sigma Aldrich에서 구입한
H3PO4, NaCI 및 KMnO4를 1 : 0.5 : 0.5의 비율로 제조하였다.8
여기에서 각각의 첨가량은 H3PO4 0.3 mol(100 mL), NaCl 0.125 mol (50 mL) 및 KMnO4 0.1 mol(50 mL)이다. 라이오셀 전구체를 전처리, 안정화 및 후속공정을
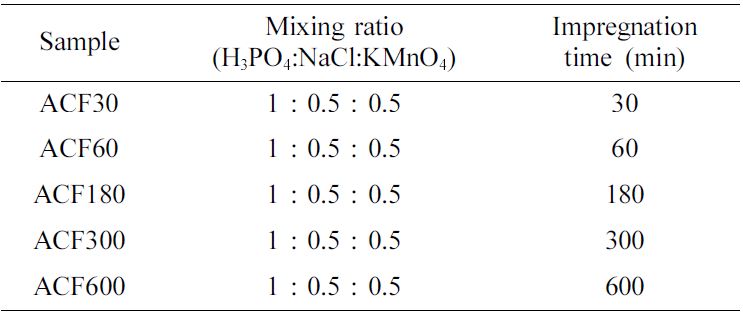
거쳐 제조된 ACF 샘플들은 Table 1과 같다. 탄화 및 활성화는 질소 분위기 하에서 H2O를 사용하여 10 ℃/min의 속도로 800 ℃ 활성화시킨 후, 최종화된
ACF 샘플을 함침시간에 따라 ACF30, ACF60, ACF180, ACF300 및 ACF600으로 명명하였다.
분석방법. 안정화 후 라이오셀 섬유의 표면구조 분석을 통해 방향족
변화여부를 판단하기 위해 FTIR(Diglab, FTS-300)을 도입하였다. 여기에서, 시험조건은 4000~500 cm-1 파장 범위에서 40회 스캔하여 이에 따른 평균값을 분석하였다.
대상샘플은 ACF180을 사용하였으며, 이때 안정화 온도 조건을 250, 260 및 270 ℃로 구분하였다. 대조군의 경우, 미안정화된 라이오셀 섬유를 선정하였다. 안정화 전∙후 라이오셀 섬유의 열안정성에 있어 승온속도가 열안정성에 미치는 영향을 알아보기 위해 열중량분석(TGA,
thermogravimetric analyzer, T-1000, Sinco 사)을 50 cc/min의 건조 질소가스가 유입되는 불활성 분위기
조건 하에서 수행하였다. 승온속도는 최대 450 ℃까지 5, 20
및 100 ℃/min의 변화를 주어 수행하였다. 활성화 에너지에 의한 열분해 거동변화 분석법은 후술하였다.
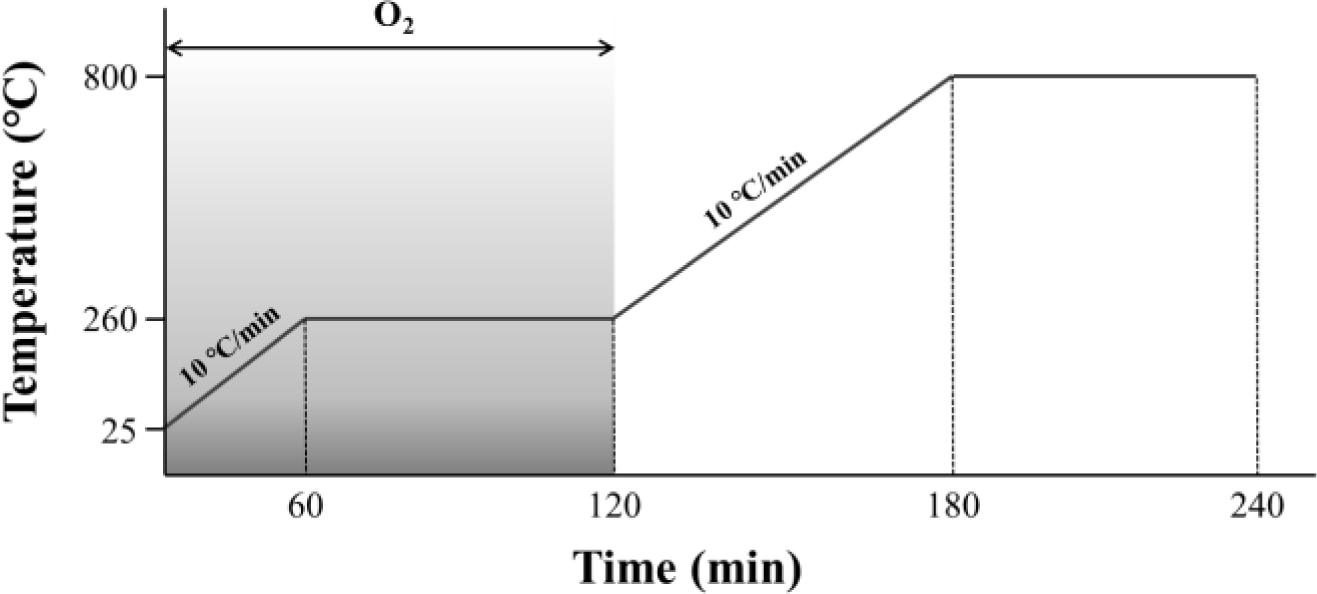
|
Figure 2 Schematic diagram of oxidation process. |
|
Table 1 Pre-treatment with Various Impregnation Time for the Synthesis of Activated Carbon Fibers |
적외선 분광분석을 통한 라이오셀 섬유의 표면구조 분석. F. Carrillo 등은9
1430~1111 cm-1 부분의 피크로서
Cellolose II와 비결정 영역을 확인할 수 있으며, 여기에서 Cellulose I은 라이오셀 섬유에 큰 부분을 차지하지 않는다고 보고하였다.
이는 Cellulose II의 경우 재생 셀룰로오스로 Cellolose I이 Cellulose II로의 전환은 비가역적이며, Cellolose
I 대비 Cellolose II가 안정하기 때문이다.10 Haibo 등11 역시 셀룰로오스의
피크가 NMMO(N-methylmorpholine N-oxide)와 결합하여 유의한
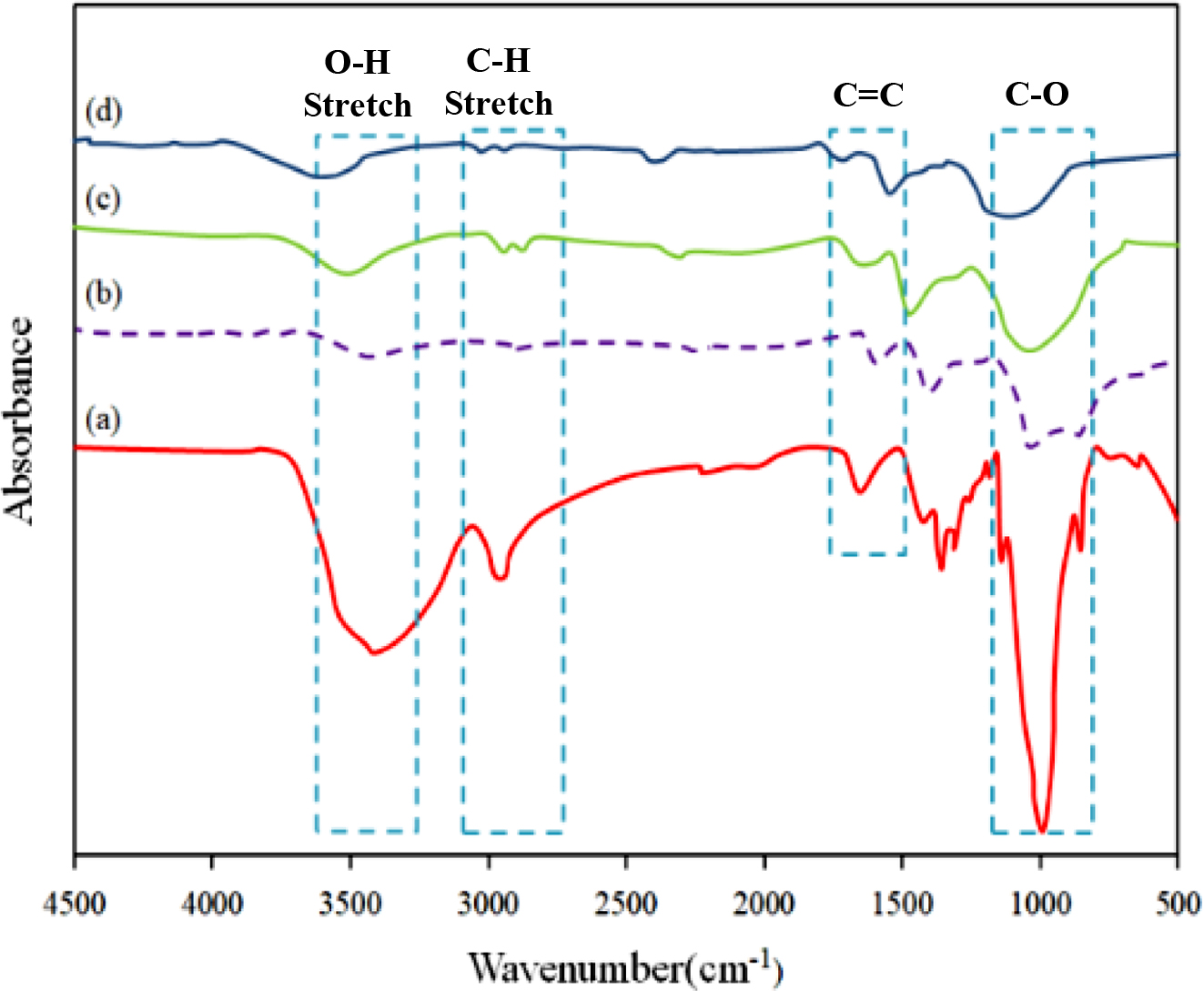
피크의 이동이 발생하였다고 보고한 바 있다. Figure 3에 안정화 전∙후 라이오셀 섬유의 적외선 분광분석 결과를 도시하였고,
3(a)는 안전화 전 라이오셀 섬유, 안정화 온도를 달리하여 3(b)는 250 ℃, 3(c)는 260 ℃ 그리고 3(d)는 270 ℃에서 진행하였다.
Figure
3(a)에서 알 수 있듯이, 안정화하지 않은 라이오셀 섬유는 4000에서 2000 cm-1까지 Cellulose I의
통상적인 피크인 OH stretching vibration과 CH stretching vibration을 보여주었다. 또한 1430 cm-1 부근에서 CH2
bending vibration과 1111 cm-1 부근에서 CO stretching vibration이 나타났다.
Figures 3(b), (c), (d)에서는 1600~1000 cm-1 에서의 피크강도가 Figure 3(a) 대비 낮아진 경향을 보였고 피크의 이동
또한 확인되었다. 이는 안정화 공정에서 250 ℃ 이하 영역에서 라이오셀
섬유가 수소와 히드록시기로부터 H2O 분자가 떨어져 나가는 분자 내 탈수화 반응이 이루어졌으며, 이 때 C=O와 C=C결합이
해리되었기 때문이다.12 안정화가 시작되는 260 ℃에서는 본격적으로
열분해가 시작되어 C-O와 C-C 결합의 분해로부터 섬유의 방향족화가 진행되는 것으로 보인다. 270 ℃에서는 붕괴된 섬유가 선형 구조(aliphatic)에서 완전한 방향족화가 진행되었으며, 섬유의 탄성저하를
가져와 부서지기 쉬운 방향족 구조를 띤다.
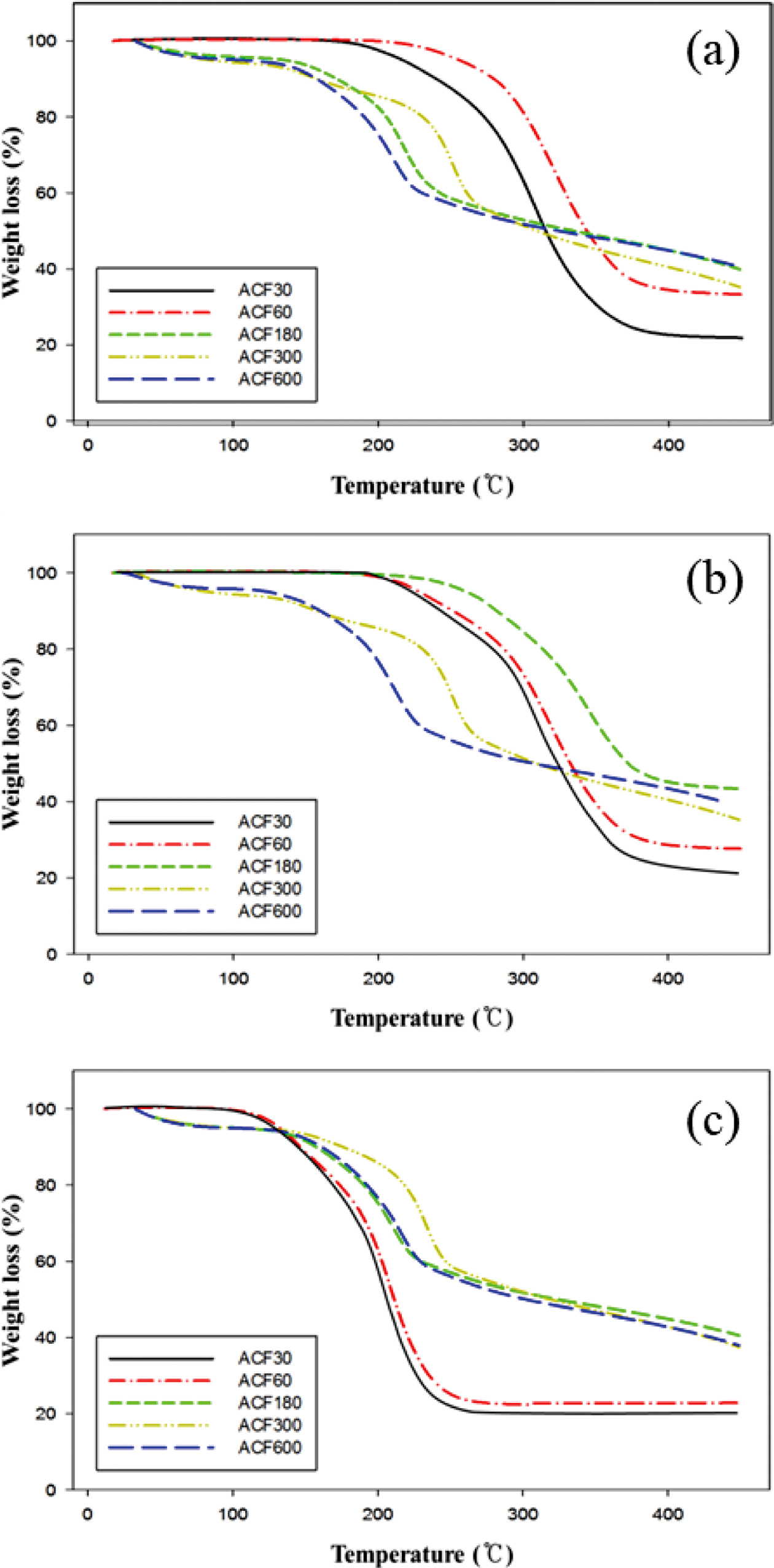
전처리 시간에 따른 열안정성 분석. Figure 4는 25~450 ℃ 사이의 온도범위에서 승온속도를 5, 10 및 20 ℃/min 로 달리하여 측정한 열중량 곡선그래프를 나타낸다. 라이오셀 섬유는 주로 용매인 NMMO가 셀룰로오스의
수소결합 네트워크를 무너뜨리고 고분자와 용매 사이에 새로운 수소결합을 생성함으로써 용매착체를 형성하는 것으로 알려져 있다.13
또한 매우 좁은 온도 범위에서 분해가 매우 두드러지게 일어나는 특징이 있기 때문에 산화공정 시 과산화에 따른 특성 변화가 심해지고, 수율이 낮아질
수 있다.14-16 승온속도를 달리하여 측정한 결과, 200 ℃ 이하에서 전체 질량의 4% 정도가 초기 분해되며, 이후 220~310 ℃ 온도 범위에서 급격한 질량 감소가 나타났다.17 최종적으로는 초기량 대비 2~5% 정도의 잔류
물질만이 존재했다. 이러한 질량 변화 양상은 셀룰로오스계인 라이오셀의 구조적 특징에 기인한다.18 셀룰로오스의 단일 분자는
보통 약 100000여 개의 D-glucopyranose 단량체들 사이의 β-1,4 결합으로 이루어진 선상 구조의 다량체이다. 이
단일 분자들이 모여 수소결합을 통해 서로 결합하여 micro fibril 형태로 식물체 내에 존재하게 된다. 여기에서, 분자 간 결합은 결정과
같은 결합특성을 보이는데, 이는 규칙적이고 반복적인 배열을 가지는 셀룰로오스 분자 구조의 특성상 분자들 상호 간 결합 역시 규칙적인 결합 순서와
반복되는 결합 위치를 가지게 되기 때문이다. 따라서 200 ℃ 이하의 낮은 온도구간에서
관찰되는 질량 감소 현상은 셀룰로오스 분자들 사이의 혹은 분자 내부에서의 수소결합이 깨지면서 일어나는 탈수소화 반응의 결과로 볼 수 있다.19
승온속도 5 ℃/min로 전처리한 라이오셀 섬유의 열중량 변화를 관찰한 결과 ACF30, ACF60이 290~300 ℃ 온도범위에서 열중량 변화가 발생하는 반면, 전처리 시간이 길었던 ACF180, ACF300 그리고
ACF600은 200~250 ℃ 온도 범위에서 열중량 변화가 시작되었다. 열분해 최종 온도인 450 ℃ 부분에서 전처리 시간이 길었던 ACF180, ACF300 그리고 ACF600의 최종 무게는 약 40%로 ACF 30과 ACF60보다 높게
나타났다. 이는 승온속도가 10과 20 ℃/min인 시험에서도
비슷한 결과가 도출되었다. 여기에서, 급격한 온도상승은 중량 변화에 큰 영향을 미치는 것으로 보인다. 대부분의 샘플에서 온도가 올라감에 따라 두드러진 중량 감소 경향이 관측되었다. 일부 샘플의 경우, 일정 시간
후 감소세가 둔화되는 경향을 보이기도 했다. 일례로 ACF180, ACF300 그리고 ACF600의 경우 온도가 상승할수록 중량 변화가 빠르게 이루어졌으나, 후에는 안정화되는 경향을
나타냈다. 이는 전처리 시간이 길어져 젖음성이 향상되어 더 많이 흡착된 H3PO4가 (HPO3)n
형태로 섬유 내·외부로 침투되어 가열 시 200~250 ℃에 분해되어
char를 생성함으로써 산소와 열을 차단해 난연효과가 발휘되었기 때문으로 보인다.20 또한 전처리 시간이 180분 이상이 되면
강산화제인 KMnO4는 섬유 표면의 붕괴를 일으키지만 점차 이온화 형태로 변화되어 젖음성이 증대된 섬유 내부로 침투한다. 여기에서,
섬유 내∙외적으로 첨착되는 KMnO4의 금속염으로 인해 섬유 전체의 열안전성이 높아질
수 있다.21
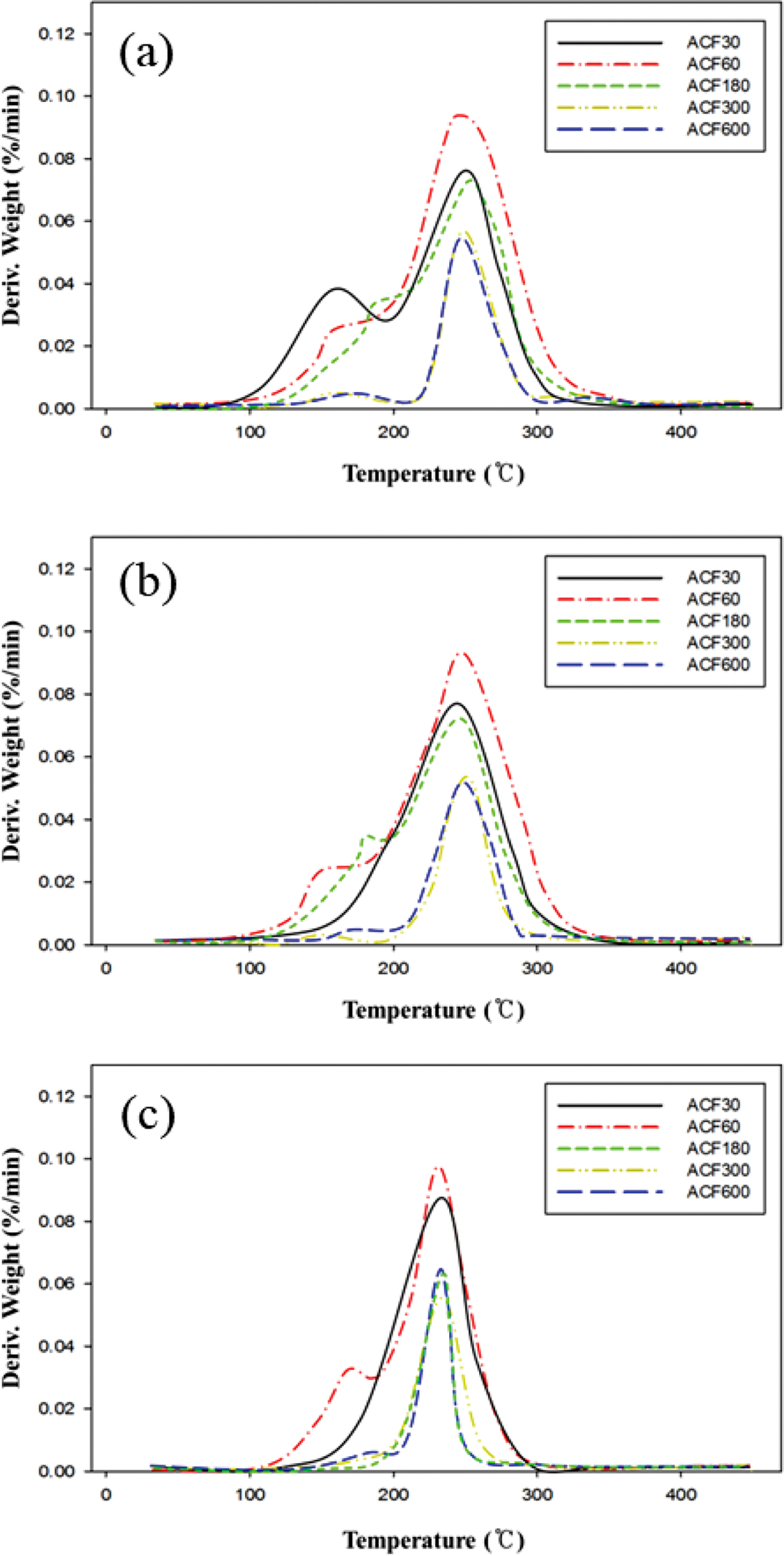
Figure 5는
라이오셀 섬유의 승온속도에 따른 미분 열중량 곡선을 나타내며, 200~400 ℃ 온도 구간에서 라이오셀 섬유의 주 성분인 셀룰로오스의 열분해에 따라 변화하는 곡선 형태를 확인할 수 있다.
270~320 ℃ 온도 구간에서는 샘플 내 셀룰로오스 성분의 열분해에 기인하는 Tpeak가
각기 다른 승온속도로 측정된 그래프에서 모두 관찰되었다. 이는 안정화가 진행될수록 라이오셀을 이루는 구성 단위들이 강한 가교결합으로 이루어진 방향족
고분자물질로 변해감으로써 열안정성이 확보되었기 때문이다. 여기에서, 전처리 시간이 길어질수록 Tpeak가 낮아지는
것 또한 확인할 수 있었다.
활성화 에너지에 의한 열분해 거동 변화 분석. 라이오셀 섬유의 열분해 거동변화를 알아보기 위한 전환율을 다음과
같이 정의하였다.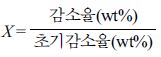 (1)
(1)
반응을 간단한 n차
반응으로 가정하면 다음과 같은 반응속도식을 얻을 수 있다.
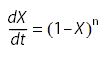 (2)
(2)
반응속도상수 k는
Arrehenius 식에 의해 식 (3)과 같이 나타낼 수 있다.
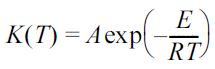 (3)
(3)
식 (2)와 식 (3)을 통해 식 (4)를 도출할 수
있다.
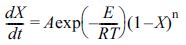 (4)
(4)
식 (4)에 가열속도(β)를
연관시켜 로그를 취하면 Friedman 식 (5)와22 같이 정리될 수 있다.
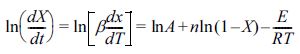 (5)
(5)
Friedman 분석방법은
임의의 전환율에 따른 kinetic 값을 통해 쉽게 활성화 에너지를 구할 수 있기 때문에 미분법 중 가장 많이 사용되는 방법이다. 그러나 이 방법은
등온 실험이기 때문에
최종 온도 450 ℃에 도달하였을 때, ln(dX/dt)의 값은 계속 변화하지만 1/T의
값은 일정하게 되므로 등온 상태에서 Friedman 분석방법의 기울기를 이용하여 활성화 에너지를 구하는 것은 쉽지 않다. 따라서 최종 온도에 도달한 이후의 활성화 에너지는 산출이 난해하기
때문에, 본 연구에서는 최종 온도 이전의 전환율에 대한 활성화 에너지로 한정하여 수행하였다.
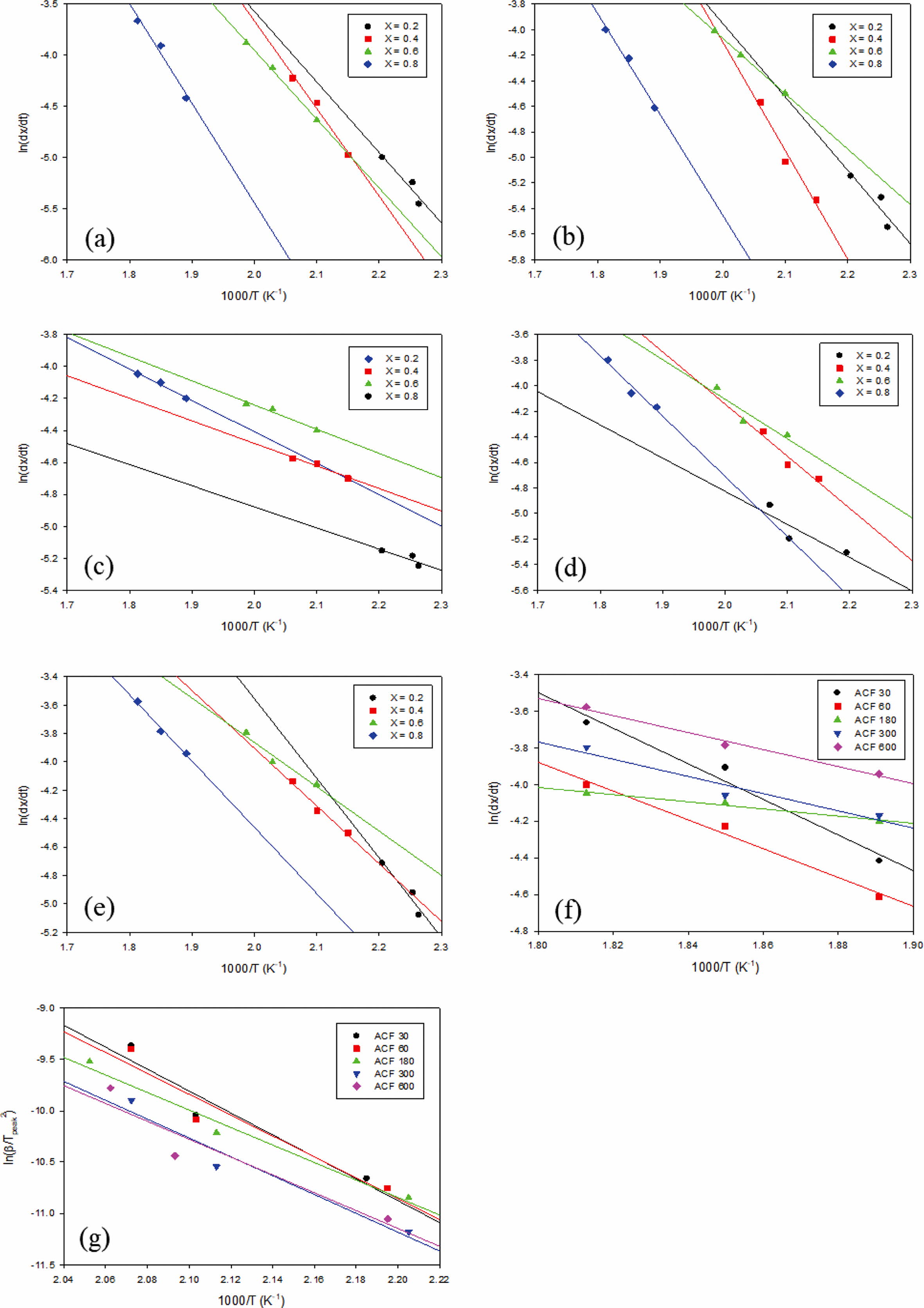
Figures
6(a)-(e)에 승온속도에 따른 중량 변화에 대한 최대 피크점을 이용하여 전환율을
달리하여 계산한 직선변화 기울기를 나타내었다. 전 그래프에서 전처리 시간이 증가할수록 기울기가 완만해짐을 확인할 수 있으며, 이는 시료의 반응
메커니즘이 TG 곡선에서 보여지는 것처럼 중량 감소가 큰 온도구간에서 승온속도가 증가함에 따라 고온에서 시료가 잔존할 수 있음을 보여준다. Figure
6(f)는 전환율이 0.8일 때의 기울기 값을 나타낸 것이며, 전환율이 증가할 수 전체 시료의 기울기 값이 평행에 가까워지는 것을 확인할 수
있다. 이는 안정화 시 라이오셀 섬유의 열안정성을 확인할 수 있는 지표로 활용될 수 있을 것으로 보인다. Kissinger23 분석방법은
승온속도와 DTG 곡선에서의 최대값 온도인 Tpeak 값을 이용하여 활성화 에너지를 구하는 방법으로 식 (6)과 같이 나타낼 수 있다.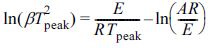 (6)
(6)
여기에서, β는
승온속도(℃/min)를 나타내며 다른 기호들은 식(4)와 동일하다.
위 식의 ln(dx/dt)와 1000/T를 각각 Y, X축으로 취하고 각 전환율 x에 따라 변화하는
값들을 연결한 추세선의 기울기를 이용하면 활성화 에너지를 구할 수 있다 (Figure 6(g)). 여기에서, 전처리 시간이 증가할수록 활성화 에너지 값은 감소하는 경향을 나타내었다.
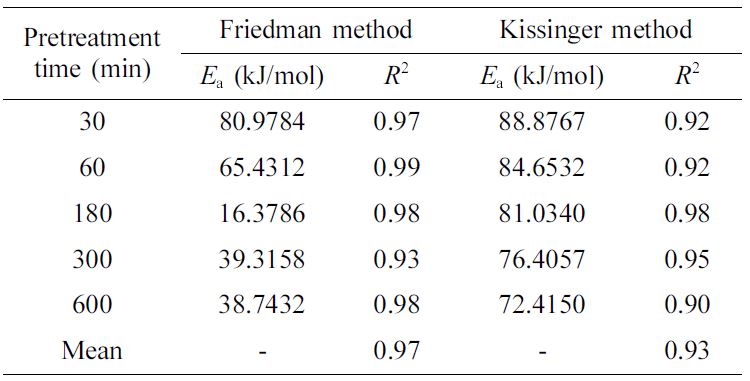
활성화 에너지 값의 추정과 결정계수. Table 2에 Friedman과 Kissinger 분석방법을
사용하여 라이오셀 섬유의 전처리 시간에 따른 활성화 에너지와 결정계수 간 상관관계를 나타내었다. Friedman 분석방법을 이용한 안정화 시료의
활성화 에너지 값은 ACF30이 80.9784 kJ/mol로 가장 높은 값을 보여주었고, 반대로 전처리 시간이 길었던 ACF180과
ACF300은 각각 16.3786, 39.3158 kJ/mol로 낮은 값을 나타내었다. 적용된 두 활성화 에너지 분석방법의 결정계수를 비교해 보면
Friedman 분석방법을 적용하였을 경우, 샘플의 평균 R2 값이 0.97을 나타내었고, Kissinger 분석방법
적용하였을 경우에는 샘플의 평균 R2 값이 0.93을 나타내었다. 상기 방법을 통해 도출된 활성화 에너지 값은 높은 유용성을
보여주었으며, Friedman 분석방법을
적용할 경우 Kissinger 분석방법보다 보다 높은 신뢰도의 활성화 에너지 값을 추정할 수 있음을 확인할 수 있었다. 두 분석방법 모두 전체적으로 샘플의 전처리 처리시간이 증가함에
따라 활성화 에너지 값이 감소하는 경향을 나타내었으며, 라이오셀 섬유는 전처리 시간이 길어질수록 낮은 온도에서의 다공액화 탄소구조 및 방향족 구조가
형성됨으로써 최종 잔존량의 면적이 커지므로 열안정성 또한 향상되었다고 판단된다.24
|
Figure 3 FTIR spectra of samples: (a) non-oxidized lyocell fiber; (b) oxidized lyocell fiber under 250 ℃; (c) oxidized lyocell fiber under 260 ℃; (d) oxidized lyocell fiber under 270 ℃. |
|
Figure 4 TGA thermograms of samples under (a) 5 ℃/min; (b) 10 ℃/min; (c) 20 ℃/min. |
|
Figure 5 DTG curves of samples under (a) 5 ℃/min; (b) 10 ℃/min; (c) 20 ℃/min. |
|
Figure 6 Friedman analysis of each sample: (a) ACF30; (b) ACF60; (c) ACF180; (d) ACF300; (e) ACF600. Sample slope (X = 0.8) and Kissinger analysis of samples by various time are depicted in (f) and (g), respectively. |
본 연구에서는 라이오셀에 기반한 ACF를 대상으로 H3PO4, NaCl 및 KMnO4의 혼합 수용액을 전처리한 후, 안정화 조건의 변화 특성을 고찰하였다. 여기에서, 주요 변화 요인은 전처리 시간 및 승온속도이다. 전처리 시간을 달리한 라이오셀 섬유는 함침시간이 길어질수록 섬유의 내열성이 향상되었고, 승온속도가 증가함에 따라 섬유의 Tpeak 값이 증가하였다. 마지막으로, Friedman 분석방법을 적용할 경우 Kissinger 분석방법보다 높은 신뢰도에 기반하여 활성화 에너지 값을 추정할 수 있음을 확인할 수 있었다. 본 연구의 열적 특성 분석은 유관분야의 섬유제조에 있어 최적의 안정화 조건을 수립할 수 있는 기초자료로의 활용이 가능할 것으로 기대된다.
향후 활성탄소섬유의 목적인 오염물질 제거에 대해 추가적인 연구를 진행할 예정이다.
- 1. S. M. Nabat Al-Ajrash and K. Lafdi, Ceramics, 2, 25 (2019).
-

- 2. N. Yusof and A. F. Ismail, J. Anal. Appl. Pyrol.,93, 1 (2012).
-

- 3. A. G. Dumanlı and A. H. Windle, J. Mater. Sci., 47, 4236 (2012).
-

- 4. T.T. Teeri, Trends Biotechnol., 15, 160 (1997).
-

- 5. A.J. Stamm, Ind. Eng. Chem., 48, 413 (1956).
-

- 6. T.Rosenau, A. Potthast, H. Sixta, and P. Kosma, Progr. Polym. Sci., 26,1763 (2001).
-

- 7. M.M. Tang and R. Bacon, Carbon, 2, 211 (1964).
-

- 8. S.S. Choi, J. H. Lee, Y. M. Jin, and S. H. Lee, Carbon Lett., link.springer.com/article/10.1007/s42823-019-00063-7.
-

- 9. F.Carrillo, X. Colom, J. J. Sunol, and J. Saurina, Eur. Polym. J., 40,2229 (2004).
-

- 10. Q.Wu and D. Pan, Textile Res. J., 72, 405 (2002).
-

- 11. H.Zhao, J. H. Kwak, Y. Wang, J. A. Franz, J. M. White, and J. E. Holladay, Carbohydr.Polym., 67, 97 (2007).
-

- 12. F.Carrillo, X. Colom, M. López-Mesas, M. J. Lis, F. González, and J. Valldeperas,Process Biochem., 39, 257 (2003).
-

- 13. S.A. Mortimer and A. A. Peguy, J. Appl. Polym. Sci., 60, 305(1996).
-

- 14. J.Praskalo, M. Kostic, A. Potthast, G. Popov, B. Pejic, and P. Skundric, Carbohydr.Polym., 77, 791 (2009).
-

- 15. S.Han, M. Lee, and B. K. Kim, J. Appl. Polym. Sci., 117, 682(2010).
-

- 16. É.Borbély, Acta Polytech. Hung., 5, 11 (2008).
- 17. J.Suñol, J. Saurina, F. Carrasco, X. Colom, and F. Carrillo, J. Therm. Anal.Calorim., 87, 41 (2007).
-

- 18. M.Cheng, Z. Qin, Y. Liu, Y. Qin, T. Li, L. Chen, and M. Zhu, J. Mater. Chem. A,2, 251 (2014).
-

- 19. G.Liang, L. He, H. Cheng, W. Li, X. Li, C. Zhang, and F. Zhao, J. Catal., 309,468 (2014).
-

- 20. H.Seddon, M. Hall, and A. R. Horrocks, Polym. Degrad. Stabil., 54,401 (1996).
-

- 21. Q.Wu, N. Pan, K. Deng, and D. Pan, Carbohydr. Polym., 72, 222(2008).
-

- 22. T.Ozawa, J. Therm. Anal. Calorim., 31, 547 (1986).
- 23. J.P. Elder, J. Therm. Anal. Calorim., 30, 657 (1985).
- 24. L.Zhang, W. Sun, D. Xu, M. Li, C. Agbo, and S. Fu, Carbohydr. Polym., 174,32 (2017).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2019; 43(6): 872-878
Published online Nov 25, 2019
- 10.7317/pk.2019.43.6.872
- Received on Jun 21, 2019
- Revised on Sep 16, 2019
- Accepted on Sep 16, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Hong Lee
-
Department of Environmental Engineering, Anyang University, Anyang 14028, Korea
- E-mail: leesh@anyang.ac.kr
- ORCID:
0000-0002-9585-3836










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.