- Preparation and Properties of Chitin and Cellulose Nanofibers and Their Applications in Polymer Films
Department of Advanced Organic Materials Engineering, Graduate School of Yeungnam University, Gyeongbuk 38541, Korea
*Dongnam Regional Division, Korea Institute of Industrial Technology, Busan 46938, Korea
**School of Chemical Engineering, Yeungnam University, Gyeongbuk 38541, Korea- 키틴과 셀룰로오스 나노파이버의 제조 및 특성과 고분자 필름에의 응용
영남대학교 대학원 유기신소재공학과, *한국생산기술연구원 동남지역본부, **영남대학교 화학공학부
Cellulose nanofiber (CNF) and
chitin nanofiber were prepared by using chemical pretreatments and mechanical
treatments such as ultrafine grinder and high-pressure homogenizer. The
fibrillation was promoted by the 2,2,6,6-tetramethylpiperidin-1-oxyl radical
(TEMPO) oxidation of cellulose and chitin, respectively. Hydroxypropyl cellulose
(HPC) film and sodium alginate (SA) film including these nanofibers were cast
using water as a solvent. The reinforcing effect of these nanofibers on the
tensile properties of HPC film and SA film was investigated by changing the
add-on amount of each nanofiber. The tensile strength of the HPC composite film
and SA composite film increased remarkably by adding a small amount of CNF and
chitin nanofiber, respectively. The film reinforcing effect of CNF was much
higher than that of chitin nanofiber. The optical transparency of both films
decreased with increasing content of nanofibers. The decreasing effect of CNF
on the transparency of the film was much lower than that of chitin nanofiber
화학적 전처리와 초미세분쇄기 및 고압균질화기와 같은 기계적
처리를 이용한 피브릴화를 통해서 셀룰로오스 나노섬유(CNF)와 키틴 나노섬유를 제조하였다. 셀룰로오스와 키틴 모두 TEMPO에 의한 산화처리에 의해서 피브릴화가
촉진되었다. 제조된 나노섬유들을 함유하는 히드록시프로필 셀룰로오스(HPC)
수용액과 알긴산 나트륨(SA) 수용액으로부터 HPC 필름과 SA 필름을 각각 제조하였으며, 나노섬유 첨가량 변화가 각 필름의
인장 특성에 미치는 효과를 평가하였다. HPC 복합필름 및 SA 복합필름의
인장강도는 각각 소량의 CNF 및 키틴 나노섬유 첨가만으로도 크게 증가하였다. 강도 보강효과는 CNF가 키틴 나노섬유보다 컸으며, 필름의 광학적 투과도는 나노섬유 첨가량 증가에 비례하여 모두 감소하였으나 키틴 나노섬유에 비하여 CNF의 감소효과가 훨씬 작았다
Cellulose nanofiber and chitin nanofiber were prepared by
using chemical pretreatment and mechanical fibrillation devices. The tensile
strength of hydroxypropyl cellulose film and sodium alginate film increased
remarkably by adding a small amount of each nanofiber, respectively.
Keywords: cellulose nanofiber, chitin nanofiber, nanofiber-reinforced film, tensile property, optical transparency
천연 고분자는 일반
고분자와 달리 생분해성, 생체적합성, 재생가능성 그리고 지속가능성과 같은 친환경적인 특성 때문에 주목을 받아왔다. 셀룰로오스는 식물세포벽으로부터
개별 셀룰로오스 피브릴을 추출하여 얻을 수 있다. 그러나 식물 세포벽의 셀룰로오스는 강한 수소결합으로 연결되어 있기 때문에 기계적 처리만으로는
셀룰로오스 섬유소를 개별화하기에 어려움이 있다.1,2 키틴은 갑각류의 껍질이나 연체동물의 골에서 단백질, 회분, 미네랄 등을
제거하고 부분적으로 탈아세틸화되어 있는 키틴의 단량체에서 아세틸기가 아미노기로 치환되어 D-글루코사민이 5000개 이상 반복적으로 결합한 형태를
가진다. 키틴 또한 셀룰로오스와 마찬가지로 많은 수소결합을 통해 강하게 결합되어 있기 때문에 키틴을 나노피브릴 수준으로 만드는 것이 쉽지 않다.3,4
나노파이버는 높은
표면적과 종횡비를 가지기 때문에 독특한 광학적 특성과 뛰어난 기계적 성질 등을 나타낼 수 있게 된다. 또 도막을 형성할 경우 기체 및 액체에 대한
차단 특성이 좋아서 나노파이버 분산액을 코팅재료로 이용하고자 하는 연구도5 진행되고 있다. 보다 용이하게 셀룰로오스와 키틴
나노파이버를 제조하기 위하여 기계적으로 피브릴화하기 전에 화학적 전처리를 거치게 되는데, 그 방법으로
2,2,6,6-tetramethylpiperidin-1-oxyl radical(TEMPO) 산화법,6,7 산 처리,8
카복시메틸화,9 morpholine 처리10 등이 있으며, 이 중 TEMPO 산화법을 많이 사용하고 있다.
TEMPO는 셀룰로오스와 키틴의 표면에서 nitrosonium ion으로 산화되어 C6의 수산기와 반응하며, 이 수산기를 카복실기로 치환한다.
TEMPO 처리 후 생성된 정전기적 반발력은 셀룰로오스와 키틴의 표면에서 음이온성 전하로 인해 발생하며, 이는 나노섬유로 분리하는데 큰 도움이
된다.
고분자 매트릭스 내에서
나노 보강재의 분산 상태 및 계면에서의 상호작용은11 기계적 특성과 물리적 성질에 영향을 미친다. 고분자 매트릭스 안에서 나노
필러 및 보강재를 고르게 분산시키는 것은 어렵기 때문에 수용성 고분자인 히드록시프로필 셀룰로오스(hydroxypropyl cellulose,
HPC)와 알긴산 나트륨(sodium alginate, SA)이 셀룰로오스 나노복합재료의 연구에 이용되고 있다.12-14
HPC 구조에 있는 히드록시 그룹은 셀룰로오스 나노파이버의 친수성 표면과 상호작용을 하여 강한 수소결합을 형성할 것으로 기대된다. 알긴산 나트륨은
갈조류나 해조류의 세포벽에서 추출되는 천연 고분자 재료이며, 우수한 생체적합성과 생분해성으로 인하여 일찍이 수술용 봉합사로 사용되어 왔다. 알지네이트
기반의 생분해성 물질은 의료용과 특수 포장용 분야 등에서 사용될 가능성이 높지만, 인장강도와 같은 기계적 특성이 대체로 부족하다. 이러한 알지네이트
기반의 생분해성 물질의 기계적 성질을 높이기 위해 셀룰로오스와 키틴 나노파이버는 알긴산 나트륨 필름의 보강재로 연구되어 왔다.15-17
본 연구에서는 HPC와
알긴산 나트륨 용액에 셀룰로오스 나노파이버와 키틴 나노파이버를 각각 첨가하여 제조한 필름의 특성들을 분석하고, 이들
나노파이버가 각 필름의 주요 특성에 미치는 영향을 평가함으로써 HPC 필름과 알긴산 나트륨 필름의 용도확대
가능성을 모색하였다.
재료 및 시약. 나노파이버를 제조하기 위하여 무림 P&P사에서
공급받은 eucalyptus kraft 펄프와 Tokyo Chemical사의 키틴 제품을 사용하였다. 화학적 처리를 위해 사용된
2,2,6,6-tetramethyl piperidin-1-oxyl radical(TEMPO), sodium hypo-chlorite는
Sigma-Aldrich사의 시약을 사용하였으며, sodium hydroxide와 sodium bromide는 Ducksan사의 제품을 사용하였다. HPC는
Sigma-Aldrich사, 알긴산 나트륨(sodium alginate, SA)은 Junsei Chemical사에서 제공받아 사용하였다. 초미세분쇄기(ultrafine
grinder)는 Masuko사(일본), 고압균질화기(high-pressure homogenizer)는 Microfluidics사(미국)의 장비를
사용하였다.
CNF와 키틴 나노파이버의 제조. 셀룰로오스와 키틴의 고형분 양을 1 wt%로 하는 수용액을 각각 제조하였다. 셀룰로오스와
키틴 수용액에 각각 sodium bromide 1 mmol과 TEMPO 0.1 mmol을 충분히 용해시킨 후 pH 10으로 맞춰진 sodium hypochlorite를 5 mmol 첨가하여 산화 반응을 시작한 후 sodium
hydroxide를 가하여 pH를 10으로 유지시켰다. 반응이 종료되면 세척 후 ultrafine grinder를 수회 통과시키고,
high-pressure homogenizer를 사용하여 나노파이버로 피브릴화하였다.
FTIR 분석. TEMPO 처리 후 순수한 셀룰로오스와 키틴 그리고
CNF와 키틴 나노파이버의 화학 구조적 특성을 확인하기 위하여 Fourier transform infrared
spectroscopy(FTIR)을 사용하여 스펙트럼을 분석하였다. 시료는 건조한 후 필름의 형태로 시편을 만들었고, 파장의 범위는
4000~500 cm-1이었으며 감쇄 전반사(attenuated
total reflection, ATR)법으로 측정하였다.
FE-SEM
분석. CNF와 키틴 나노파이버를 화학적 처리와 기계적으로 처리한
후 미세 형태 및 직경과 길이를 FE-SEM(field emission scanning electron microscope, S-4800,
Hitachi)으로 관찰하였다. 시편은 동결 건조한 후 금속이온 코팅기(E-1030, Ion-Sputter)를 사용하여 표면을 백금으로 진공 증착시켜
제조하였다.
HPC 용액과 알긴산 나트륨 나노파이버 복합용액의 제조. HPC 용액은 용매로 에틸알코올을 사용하여 10 wt%로 제조하였고, 알긴산 나트륨 용액은 3 wt% 수용액으로 제조하였다. 제조된 용액에 CNF와 키틴 나노파이버를
고분자 무게에 대하여 각각 1, 3, 5, 7% 첨가하고 충분히 교반시켜 HPC/CNF, HPC/chitin nanofiber, SA/CNF 및 SA/chitin
nanofiber 복합 용액을 각각 제조하였다.
나노파이버 복합용액의 점도 특성 분석. CNF와 키틴 나노파이버의 첨가가 복합 용액의 점도에
미치는 영향을 확인하기 위하여 cone and plate rheometer(Anton Paar, Austria)를 사용하여 복합 용액의 유변학적
성질을 측정하였다. 전단 속도의 변화에 따른 점도의 변화는 0.1-100 s 범위에서 수행하여 평가하였다.
나노파이버 복합필름의 제조. 복합 용액을 각각 필름메이커로 캐스팅하여 40±5 μm 두께로 제조하였다. 캐스팅한 나노 파이버 복합필름을 실온에서 24시간 건조한 후 25 oC, 상대 습도 55% 조건에서 컨디셔닝하였다.
SA 필름의 가교. SA 필름 표면에 1% CaCl2을
도포시켜 10분간 가교시킨 후 증류수로 충분히 세척하였다. 그 후 하루 동안 실온에서 완전히 건조하였다.
나노파이버 복합필름의 기계적 강도 측정. 제조된 나노파이버 복합필름을 10×50 mm 크기로 절단하여 온도 25 oC, 상대습도 55%에서 필름의 인장강도와 인장변형률을 측정하였다. 인장시험기(Instron-3345)를 사용하여
하중 속도 50 mm/min로 10개의 시편을 측정하여 구한 평균값을
비교 분석하였다.
SA/CNF와 SA/키틴 나노파이버 필름의 열중량 분석. 열안정성이 낮은 알긴산
나트륨 필름의 열분해 특성을 평가하기 위해 열중량 분석기(TG-DTA)(TA Instruments, SDT Q600)를 사용하여 나노파이버 첨가 및 가교반응의 효과를 확인하였다.
시료의 중량 감소율은 질소가 공급되는 환경에서 가열 속도를 10 oC/min으로 일정하게
유지하며 50~850 oC 온도 범위에서 측정하였다.
나노파이버 복합필름의 광투과도 분석. 나노파이버 복합필름의 광투과도를 측정하기 위하여
UV-vis spectrophotometer (Agilent Technologies, Cary 5000)를 사용하였다. 광투과도의 측정 파장은
가시광선의 전체 영역으로 하였다.
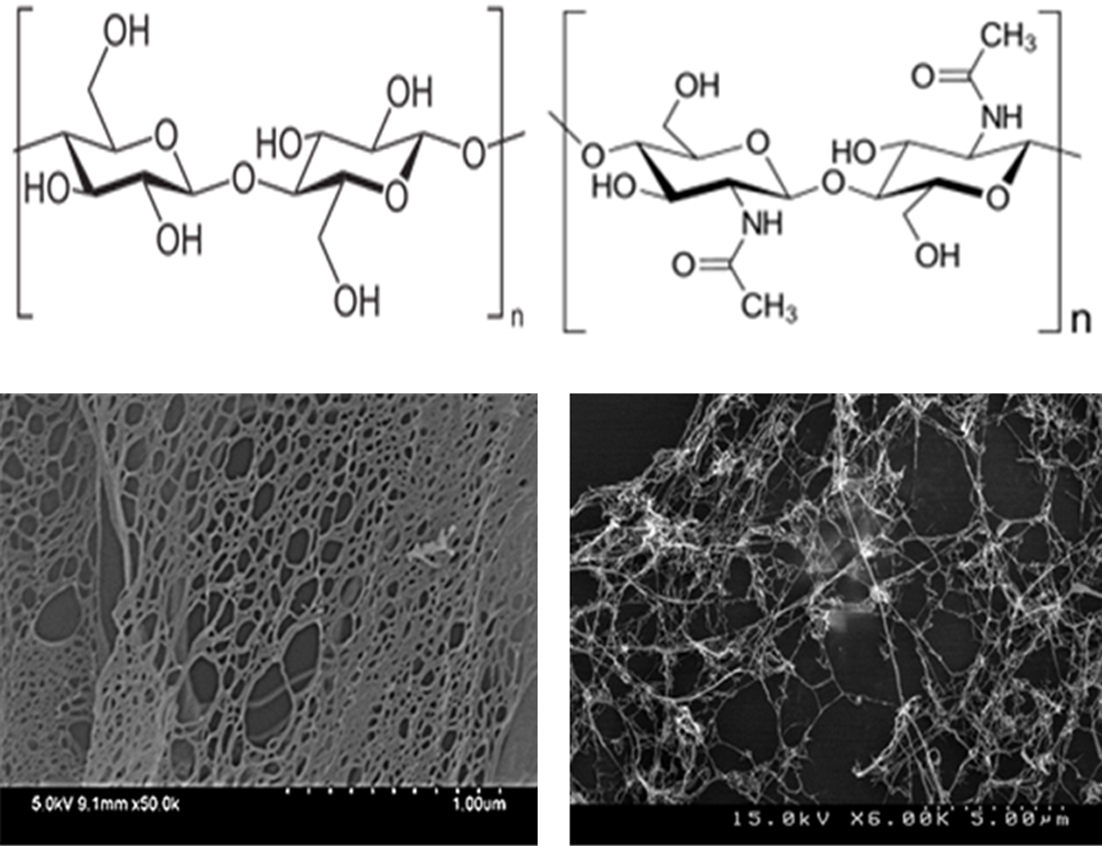
CNF와 키틴 나노파이버의 미세 형태. 셀룰로오스와 키틴을 TEMPO 처리 후 기계적으로 나노피브릴화한
나노파이버의 형태를 조사하기 위하여
주사전자현미경을 사용하였으며,
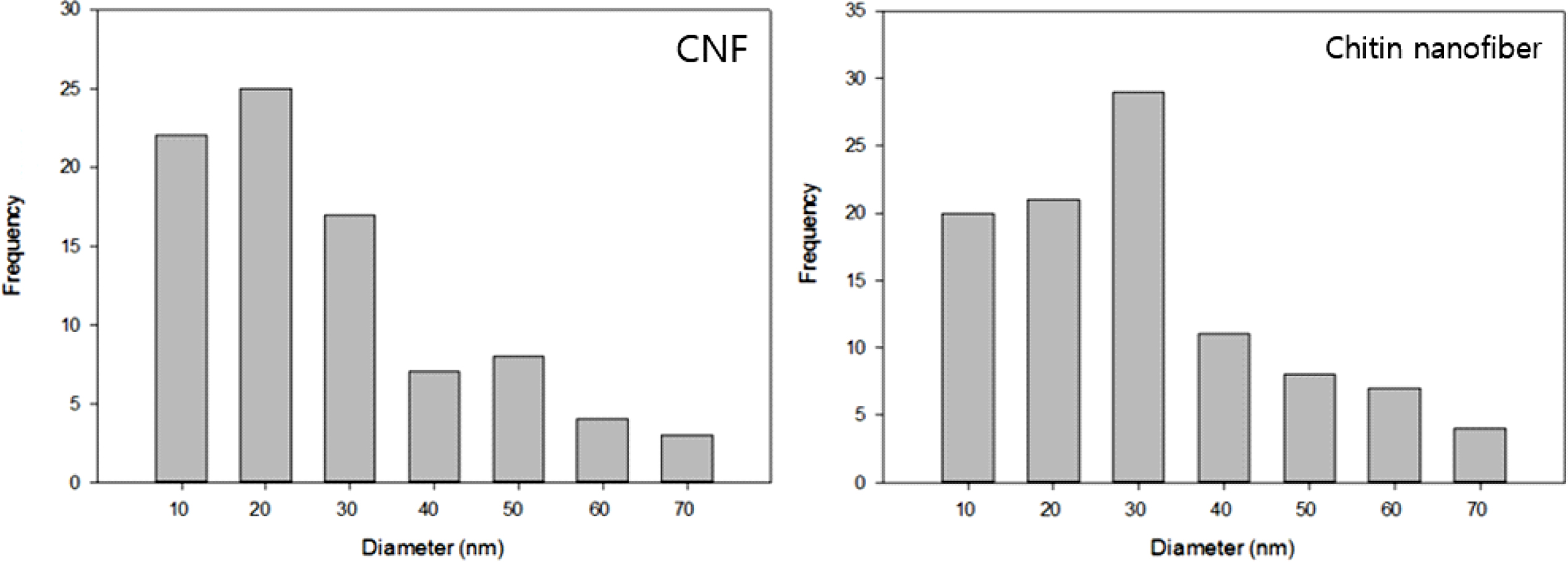
Figure 1은 나노파이버의 미세 형태 특성을 SEM을 이용하여 관찰한 이미지이다. 화학적, 기계적 처리 전 셀룰로오스의 직경은 50~100 μm이었으며 처리 후 CNF의 직경은 평균 25 nm로 매우 크게 감소한 것을 확인할 수 있었다. 화학적, 기계적 처리 전 키틴의 직경은 30~80 μm이었으며, 처리 후 키틴 나노파이버의 직경은 평균 35 nm로 역시 직경이 확연히 줄어든 것을 확인할 수 있었다. Figure 2에 CNF와 키틴 나노파이버의 직경
분포를 나타내었다. CNF와 키틴 나노파이버는 10~70 nm 사이의 분포를 보였으며, 각각 평균 25 nm와 35 nm로 CNF의 직경이 더 작았다.
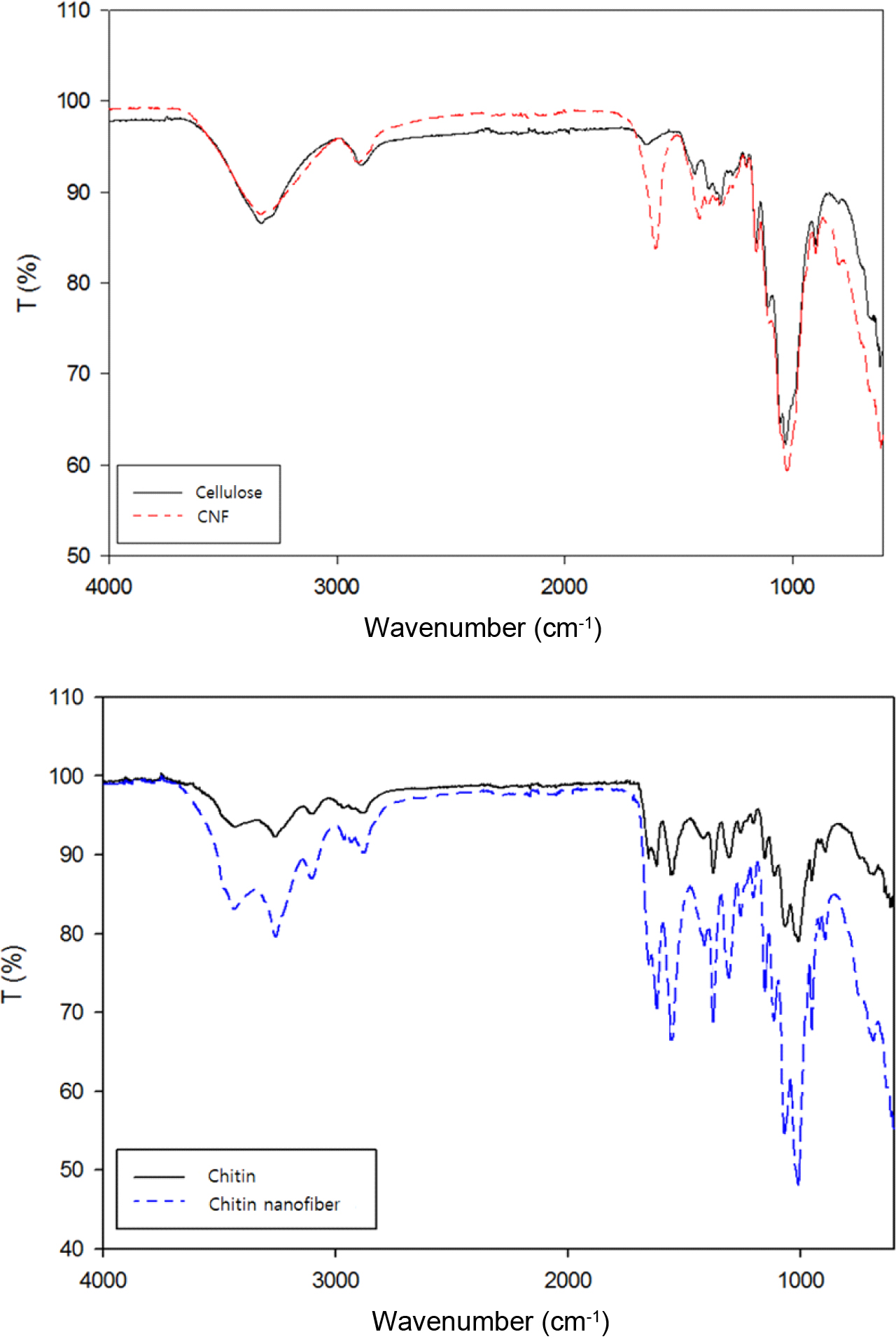
CNF와 키틴 나노파이버의 화학구조. Figure 3은 셀룰로오스와 CNF, 키틴과 키틴 나노파이버의
적외선 스펙트럼이다. 셀룰로오스 스펙트럼은 3340 cm-1에서 O-H 피크를 나타내었고, 1594 cm-1에서 N-H 신축 밴드, 1610 cm-1과 1740 cm-1에서 각각 COO 및
COOH의 피크를 나타낸다. CNF의 FTIR 스펙트럼에서는 TEMPO 처리 후 생성된 C=O기를 1644 cm-1에서 확인할 수 있었다.16 키틴의
스펙트럼에서 O-H 신축 진동의 경우 3440 cm-1에서 피크를 나타내었고, N-H 신축 진동으로 인한 3266 cm-1에서의 피크, C-H 신축
진동으로 인한 피크를 2970-2888 cm-1에서 볼 수 있다. 키틴 나노파이버의
스펙트럼에서는 1626 cm-1에서 새로운 피크를 확인할
수 있었는데, 이는 카복시산 나트륨의 형태로 존재하는 카보닐기로부터 기인한 것이다.18,19
HPC/CNF,
HPC/키틴 나노파이버, SA/CNF, SA/키틴 나노파이버 복합 용액의 투명도. 화학적, 기계적 처리 전후의 셀룰로오스와 키틴의 고형분
농도를 1 wt%로 조절하여 투명도를 육안으로 비교하였다.
Figure 4에서 화학적, 기계적 처리 전 셀룰로오스와 키틴과 비교하여 각각 CNF 및 키틴 나노파이버 분산액이 더 높은 투명도를 보이는 것을
확인할 수 있다. CNF와 키틴 나노파이버 분산액을 비교하였을 때에는 CNF가 조금 더 높은 투명도를 보이는 것을 알 수 있다.
HPC/CNF,
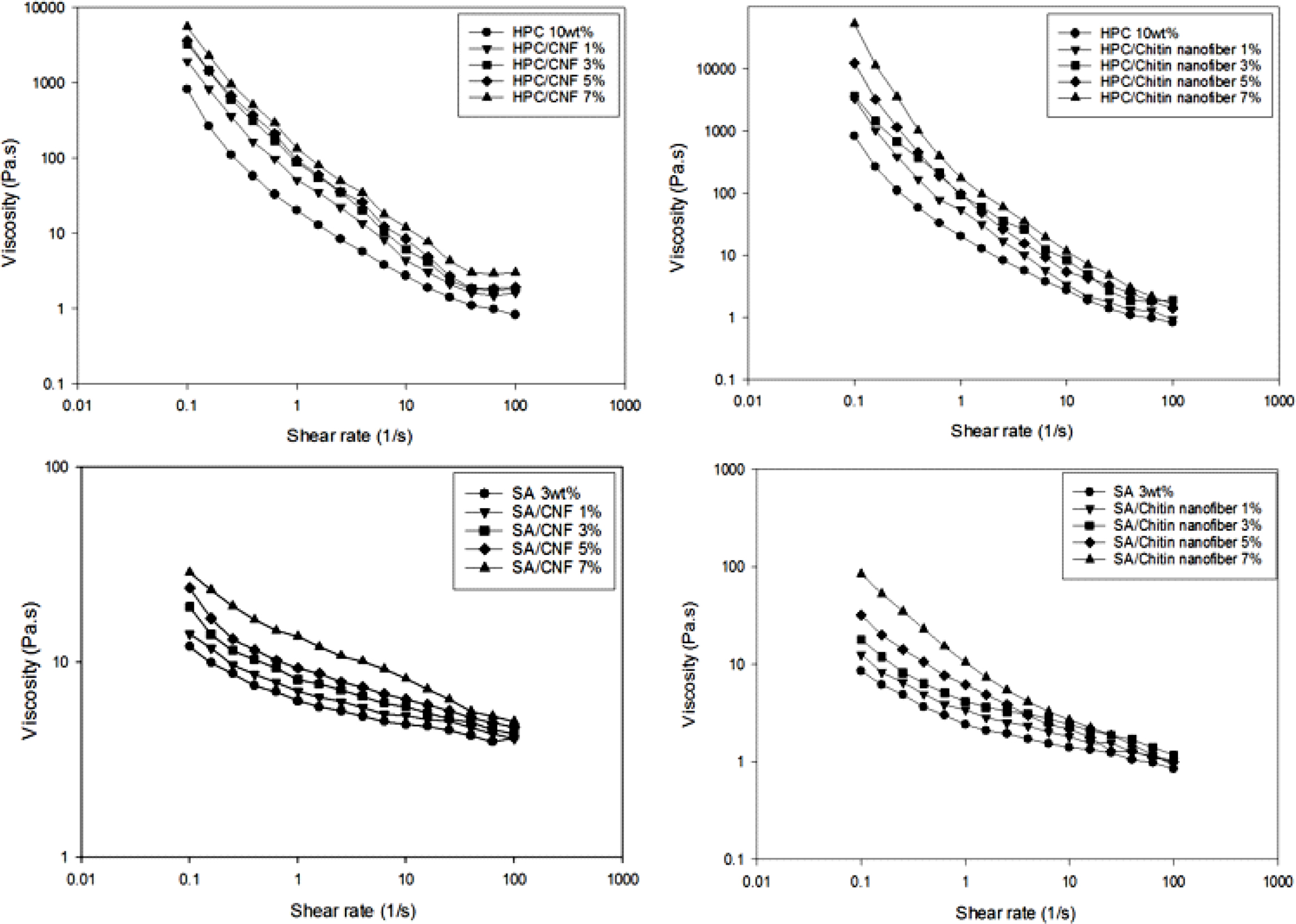
HPC/키틴 나노파이버, SA/CNF 및 SA/키틴 나노파이버 복합 용액의 유변학적 특성. 나노파이버의 첨가가 고분자 용액의 유변학적 성질에 미치는
영향을 알아보기 위해 레오미터를 사용하여 확인한 결과를 Figure 5에 나타내었다. 10 wt% HPC 용액에 CNF와 키틴 나노파이버 첨가량이
각각 1%에서 7%까지 증가할수록 점도가 증가하였으며, 전단속도가 증가함에 따라 점도가 낮아지는 shear thinning 거동을 보였다. 마찬가지로
3 wt% SA 용액에 CNF와 키틴 나노파이버 첨가량이
증가할수록 점도가 증가하였으며, 전단속도가 증가함에 따라 점도가 낮아지는 shear thinning 거동을 보였다.
HPC/CNF,
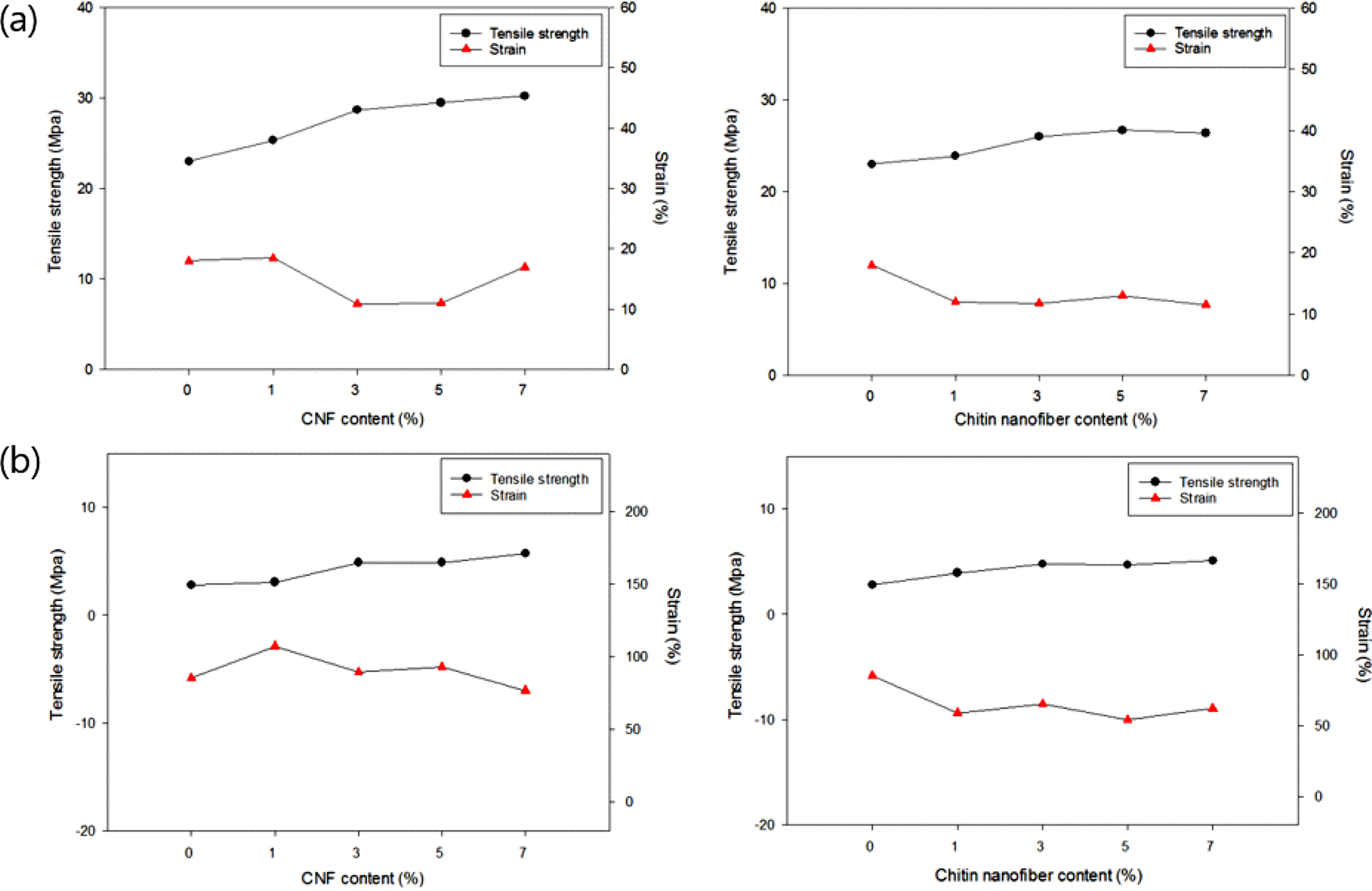
HPC/키틴 나노파이버, SA/CNF 및 SA/키틴 나노파이버 복합필름의 기계적 성질. Figure 6은 나노파이버를 1, 3, 5, 7%로 달리 첨가한 HPC 및 SA 필름의 인장강도와
인장변형률을 각각 나타낸 것이다. HPC/CNF 필름에서 CNF 첨가량이 많을수록 인장강도가 점차 증가하였고, HPC/키틴 나노파이버 필름에서도
마찬가지로 키틴 나노파이버를 많이 첨가할수록 인장강도가 증가하였다. 나노파이버 7% 첨가 기준 인장강도 증가율은 HPC/CNF가 31.4%로
14.8%까지 증가한 HPC/키틴 나노파이버 필름보다 높았다. SA/CNF 필름에서도 HPC/CNF 필름과 마찬가지로 CNF를 첨가할수록 인장강도가
점차 증가하였으며, SA/키틴 나노파이버 필름의 경우에도 키틴 나노파이버 첨가에 따른 인장강도의 증가 경향은 HPC/키틴 나노파이버 필름과 매우
유사하였다. 나노파이버 7% 첨가 기준 인장강도 증가율은 SA/CNF가 103.6%로 82.1%까지 증가한 SA/키틴 나노파이버 필름보다 크게
높았다. 이러한 결과는 셀룰로오스와 키틴이 모두 HPC와 SA의 화학구조에 있는 수산기와 강한 수소결합을 형성하고, 나노 크기의 셀룰로오스와 키틴의 표면적이 증가함에 따라 필름용
고분자와 접촉하는 계면적이 증가하는 것에 의하여 각 필름의 기계적 강도가 증가된 것으로 볼 수 있으며, CNF 나노파이버의 직경이
키틴 나노파이버의 직경보다 더 작아 그 효과가 더 크게 나타난 것으로 보인다.15 또 키틴에 비해서 셀룰로오스가 글루코스 단위당
히드록시기의 수가 더 많아서 수소결합 밀도가 높다는 점도 강도 향상에 기여할 것으로 생각된다.
SA/CNF,
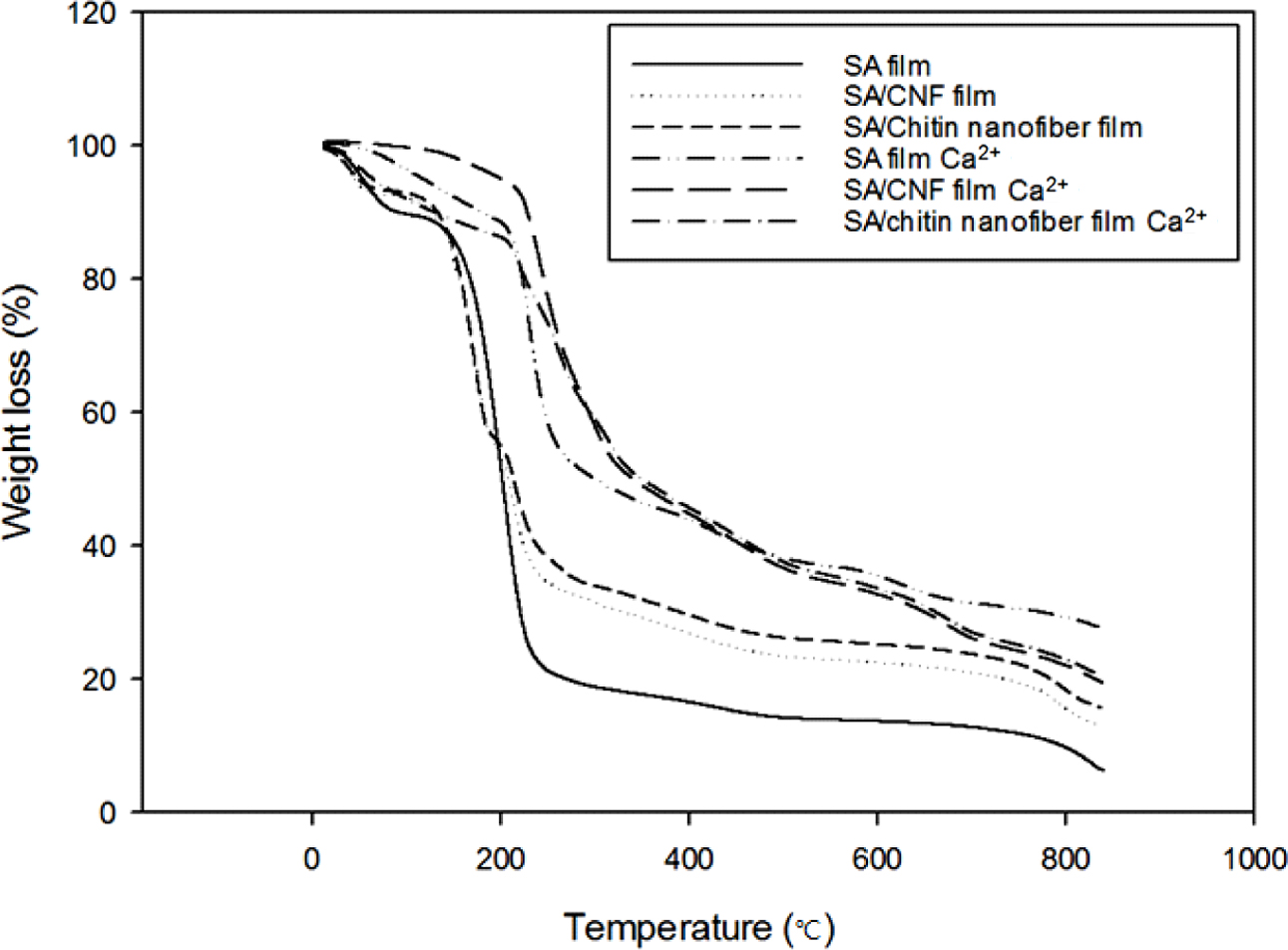
SA/키틴 나노파이버 복합필름의 열분해 특성. Figure 7에 나노섬유를 첨가한 SA 필름과 Ca2+
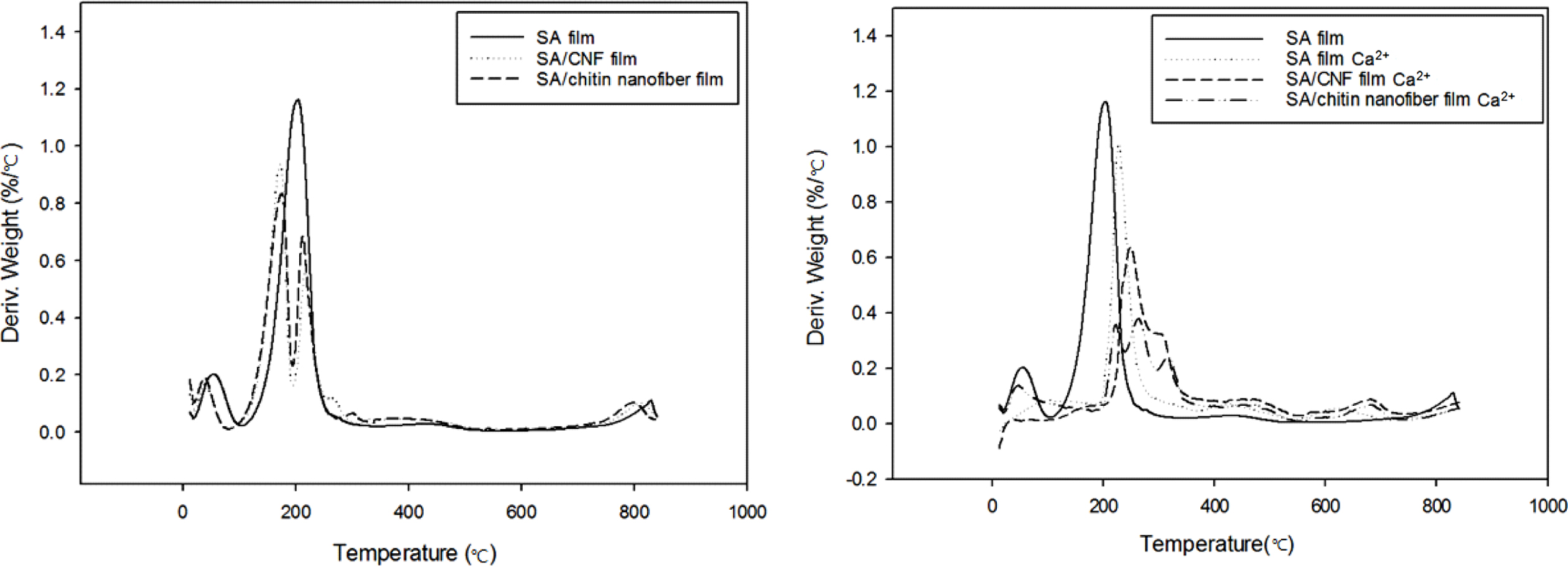
이온으로 가교한 SA 필름의 열중량 분석 곡선을 보이고, Figure 8에는 미분 열중량 분석(derivative
thermogravimetry, DTG) 곡선을 나타내었다. 40 oC에서 100 oC까지 범위의 중량 손실은 물의 증발에 의한 것이며, 200 oC 부근에서의 현저한 중량 손실은 알지네이트의 글리코시드 결합의 열분해에 의한 것이다.16,20
CNF와 키틴 나노파이버를 첨가한 필름에서는 200 oC 이상에서 나노파이버의
글리코시드 결합의 열분해로 인한 중량 감소 피크를 확인할 수 있다. 칼슘으로 가교된 SA 필름의 DTG 곡선에서는 가교하지 않은 SA 필름보다
높은 온도인 250 oC 부근에서 중량 손실이 일어남을 볼 수 있다. 이는 알지네이트 하이드로젤에 대한 열중량 분석에서도18
확인된 바 있다. 나노파이버를 첨가한 후 SA 필름에서 200 oC 부근의 두 번째 중량
감소단계는 알지네이트의 글리코시드 결합의 열분해로 인한 것이고, 230 oC에서 380 oC의 온도 범위에서의
중량 감소는 나노 셀룰로오스와 키틴의 글리코시드 결합 절단으로 인한 것이다.15 나노파이버를 첨가한 후 가교결합시킨 SA 필름의
DTG 곡선에서 220 oC에서의 알지네이트의 글리코시드 결합의 절단으로 인한 중량 감소와 240 oC에서 360 oC 사이에서 셀룰로오스와
키틴의 글리코시드 결합의 분해로 인한 중량 감소를 확인할 수 있다.14,20
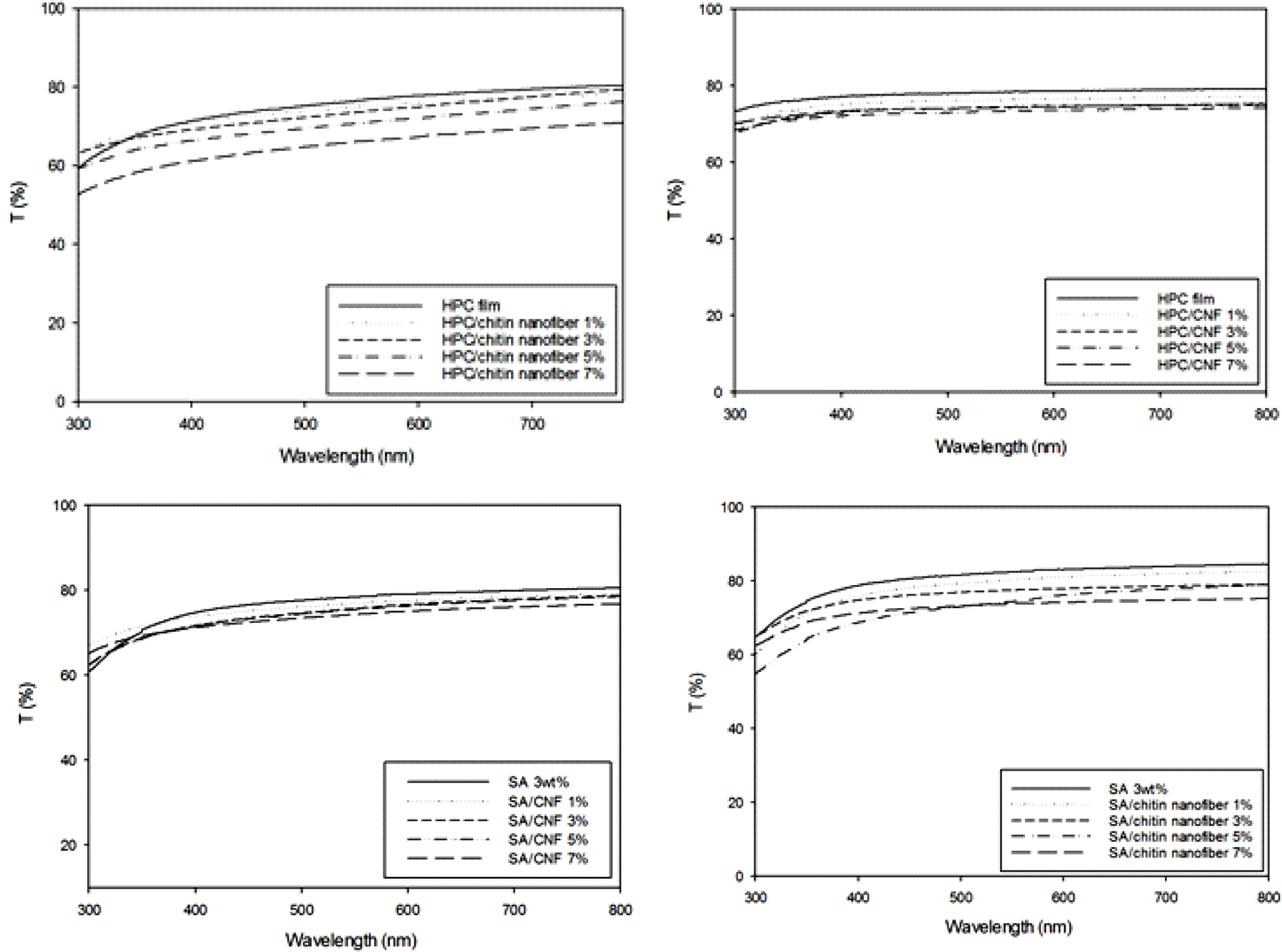
나노파이버 복합필름의 광투과도. Figure 9에 나노파이버 첨가량에 따른 복합필름의
광투과도 변화를 나타내었다. CNF와 키틴 나노파이버의 함량이 증가할수록 HPC 나노파이버 복합필름의 광투광도는 비례하여 감소하였으며, 키틴 나노파이버를
첨가하였을 때 더 큰 감소율을 나타내었다. 이는 키틴 나노파이버가 CNF보다 평균 직경이 더 크기 때문인 것으로 볼 수 있다. HPC 나노파이버
복합필름과 마찬가지로 나노파이버의 함량이 증가할수록 SA 나노파이버 복합필름의 광투광도는 감소하였으며, HPC 복합필름과 마찬가지로 키틴 나노파이버를
첨가하였을 때 CNF 첨가 시 보다 더 큰 감소율을 나타내었다. 모든 필름 시료에서 나노파이버의 첨가량이 1% 이내일 경우에는 광투과도의 감소가
크지 않았다.

|
Figure 1 SEM images of (a) cellulose pulp; (b) TEMPO-treated CNF; (c) chitin flake; (d) TEMPO-treated chitin nanofiber. |
|
Figure 2 Diameter distribution of CNF and chitin nanofiber by high pressure homogenizer treatment. |
|
Figure 3 FTIR spectra of cellulose chitin and their nanofibers. |

|
Figure 4 Comparative optical transparency of (a) cellulose before chemical and mechanical treatments (1 wt%); (b) CNF after chemical and mechanical treatments (1 wt%); (c) chitin before chemical and mechanical treatments (1 wt%); (d) chitin nanofiber after chemical and mechanical treatments (1 wt%). |
|
Figure 5 Viscosity of polymer/nanofiber composite solution with shear rate change. |
|
Figure 6 Tensile strength and strain of (a) HPC; (b) SA films according to CNF and chitin nanofiber content. |
|
Figure 7 TG thermograms of the sodium alginate, cross-linked sodium alginate, and SA/nanofiber films. |
|
Figure 8 DTG thermograms of the SA/nanofiber and cross-linked SA/nanofiber films. |
|
Figure 9 Optical transmittance of HPC and SA films with different amount of CNF and chitin nanofiber. |
셀룰로오스와 키틴을
화학적 처리 후 기계적으로 나노피브릴화하여 셀룰로오스 나노파이버(CNF)와 키틴 나노파이버를 제조하였으며, 하이드록시프로필 셀룰로오스(HPC)와
알긴산 나트륨(SA) 필름에 나노파이버를 첨가하여 제조한 복합필름들의 특성을 평가하여 다음과 같은 결론을 얻었다.
1. 셀룰로오스 섬유와
키틴 플레이크의 TEMPO 산화처리 후 카보닐기의 생성 및 증가가 확인되었으며, TEMPO 처리 후 피브릴화를 위한 기계적 처리를 거듭할수록
CNF와 키틴 나노파이버의 평균직경은 감소하여 각각 25 nm와 35 nm 수준까지 제조할 수 있었다.
2. 나노파이버 첨가량을
달리한 HPC/CNF, HPC/키틴 나노파이버, SA/CNF 및 SA/키틴 나노파이버 혼합액의 점도는 모두 shear thinning 거동을 나타내었다.
3. HPC 필름에 CNF 및
키틴 나노파이버를 각각 첨가하였을 때 필름의 인장강도는 나노파이버 첨가량에 비례하여 증가하였으며, 최대 증가율은 7% 첨가 시 31.4%이었다.
4. SA 필름에도 CNF 및
키틴 나노파이버를 각각 7%까지 첨가하였을 때 인장강도는 나노파이버 첨가량에 비례하여 증가하였으나 그 절댓값은 크지 않았으며, 같은 첨가량에서는
두 종류의 필름 모두 CNF의 증가효과가 키틴 나노파이버보다 더 컸다.
5. 나노파이버의
첨가에 의해 SA 필름의 열안정성 증가효과는 거의 없었으나, Ca2+ 이온으로 가교된
알긴산 나트륨 필름의 열분해 온도는 가교하지 않은 필름보다 약 50 oC 높았다.
6. CNF 또는
키틴 나노파이버의 첨가량이 높아질수록 모든 복합필름의 광투과도는 감소하였으며, 두 필름 모두 키틴 나노파이버를 첨가하였을 때 더 큰 광투과도 감소율을
보였다.
- 1. K. Uetani and H. Yano, Biomacromolecules, 12, 348 (2011).
-

- 2. A. Isogai and Y. Kato, Cellulose, 5, 153 (1998).
-

- 3. Y. Lu, Q. Sun, X. She, Y. Xia, Y. Liu, J. Li, and D. Yang, Carbohyd. Polym., 98, 1497 (2013).
-

- 4. S. Ifuku and H. Saimoto, Nanoscale, 4, 3308 (2012).
-

- 5. H. W. Kwak, J. E. Heo, K. Her, H. Lee, H.-J. Jin, and B. S. Shim, Polym. Korea, 43, 32 (2019).
-

- 6. T. Saito, S. Kimura, Y. Nishiyama, and A. Isogai, Biomacromolecules, 8, 2485 (2007).
-

- 7. K. Sim, H. J. Youn, and Y. Jo, J. Korea TAPPI, 72, 42 (2015).
-

- 8. Z.-D. Qi, Y. Fan, T. Saito, H. Fukuzumi, Y. Tsutsumi, and A. Isogai, RSC Adv., 3, 2613 (2013).
-

- 9. H. A. Ambjörnsson, K. Schenzel, and U. Germgäard, Bioresources, 8, 1918 (2013).
-

- 10. M. L. Hassan, N. F. Kassem, and M. E.-Sakhawy, Egypt. J. Chem., 58, 299 (2015).
-

- 11. A. J. Onyianta, M. Dorris, and R. L. Williams, Cellulose, 25, 1047 (2018).
-

- 12. S.-Y. Lee, S.-J. Chun, I.-A. Kang, and J.-Y. Park, J. Ind. Eng. Chem., 15, 50 (2009).
-

- 13. J. P. Borges, M. H. Godinho, A. F. Martins, D. F. Stamatialis, M. N. De Pinho, and M. N. Belgacem, Polym. Compos., 25, 102 (2004).
-

- 14. R. Pereira, A. Carvalho, D. C. Vaz, M. H. Gil, A. Mendes, and P. Bártolo, Int. J. Biolog. Macromol., 52, 221 (2013).
-

- 15. J. A. Sirviö, A. Kolehmainen, H. Liimatainen, J. Niinimäki, and O. E. O. Hormi, Food Chem., 151, 343 (2014).
-

- 16. X.-J. Shen, P.-L. Huang, J.-H. Chen, Y.-Y. Wu, Q.-Y. Liu, and R.-C. Sun, Bioresources, 12, 8180 (2017).
- 17. B. Deepa, E. Abraham, L. A. Pothan, N. Cordeiro, M. Faria, and S. Thomas, Materials, 9, 50 (2016).
-

- 18. X. Sun, J. Zhu, Q. Gu, and Y. You, Colloid Surf. A, 555, 103 (2018).
-

- 19. Y. Fan, T. Saito, and A. Isogai, Carbohyd. Polym., 77, 832 (2009).
-

- 20. A. R. Fajardo, M. B. Silva, L. C. Lopes, J. F. Piai, A. F. Rubira, and E. C. Muniz, RSC Adv., 2, 11095 (2012).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(1): 13-20
Published online Jan 25, 2020
- 10.7317/pk.2020.44.1.13
- Received on Jul 29, 2019
- Revised on Oct 23, 2019
- Accepted on Oct 23, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Joon Ho Kim
-
School of Chemical Engineering, Yeungnam University, Gyeongbuk 38541, Korea
- E-mail: joon@yu.ac.kr
- ORCID:
0000-0002-9106-6886










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.