- Investigation of Overall Migration from Polyolefin and Polyester Packaging Materials into Cosmetic Simulants
Miso Kim, Dongwon Lee, Suyeon Yun, Seung-il Yoon, Yunhee Lee*, Doohyeon Lim*, Seung-Wook Ham, Sangdoo Ahn†
 , and Hyoyeon Yu†
, and Hyoyeon Yu†
Department of Chemistry, Chung-Ang University, Seoul 06974, Korea
*Global Regulatory Affairs Team, COSMAX, Gyeonggi-do 13486, Korea- 폴리올레핀 및 폴리에스터계 포장 용기에서 화장품 모사품으로의 이행에 관한 연구
중앙대학교 화학과, *코스맥스 글로벌규정연구팀
Migration can occur when
plastic packaging materials contact with contents such as food, medicine, and
cosmetics. As a result, the organoleptic, physical, and chemical changes of the
product can arise and some toxic migrants can produce a risk for human health.
In this study, overall migration was studied from PP, LDPE, HDPE, and
PET(transparent & colored) packaging into 6 different cosmetic simulants
(aqueous, acidic, basic, and fat-soluble solution) through incubation at 40 oC
for 10 days. Under these conditions, it was confirmed that all plastic
packaging complied with EU regulations, but some migrants such as antioxidants
and oligomers were carried over from polyolefin packaging to 95% ethanol
aqueous solution.
플라스틱 포장재는 식품,
의약품, 화장품 등의 내부 물질과 접촉하게 되면 이행이 발생할 수 있다. 이러한 이행은 제품의 관능, 물리적, 화학적 변화를 야기할 뿐만 아니라 독성을 가지는 화합물로 인하여 인체에 부작용을 끼칠 수 있다. 본 연구에서는 EU의 용기 이행 시험 표준에 근거하여 화장품 1차 포장재로 널리 사용되는 PP, LDPE, HDPE, PET(transparent
& colored) 용기 5종에 대하여
overall migration 시험을 수행하였다. 수성,
산성, 지용성, 염기성 화장품을 대표할 수 있는 6종의 모사품을 사용하였고, 시료들을 40 oC에서 10일간 보관 후에 분석하였다. 시험에 사용한 모든 용기들이 시험조건에서 EU 기준을 충족하는 것을
확인하였고(10 mg/dm2 또는 60 mg/kg
이하), 일부 폴리올레핀계 용기에서는 규제치 이하지만 산화방지제 등의 첨가제와 올리고머가
이행되는 것을 확인하였다
Overall migration was studied from polyolefin and polyester primary packaging for cosmetics into various cosmetic simulants. It was confirmed that all plastic packaging complied with EU regulations, but some migrants such as antioxidant and oligomers were carried over from polyolefin packaging to 95% ethanol aqueous solution.
Keywords: cosmetic plastic packaging, migration, overall migration, cosmetic simulant, migrant
이 논문은
2018년도 중앙대학교 CAU GRS 지원과 코스맥스㈜ 산학협동연구 지원에 의하여 작성되었음.
포장은 생산부터 소비까지
일련의 과정 동안 제품의 보관, 운송 등을 가능하게 하는 수단이다. 특히 식품, 제약 및 화장품 포장 분야에서 제품과 직접 접촉하는 1차 포장재의
주요 기능은 제품의 품질 저하를 유발할 수 있는 기후 조건, 생물학적, 물리적, 화학적 위험으로부터 제품을 보호하는 것이다. 따라서 제품의 안정성을 보장하기 위하여 1차 포장재는 유리,
금속, 플라스틱 등 활성이 적은
소재가 사용된다. 특히 플라스틱 포장재는 가볍고, 내구성이 좋으며, 가공이 용이하다는 점에서 경제적인 소재로 널리 사용되고 있다. 식품, 의약품,
화장품 등 여러 분야에 걸친 수요를 충족시키기 위하여 지난 수십 년 동안 플라스틱 포장재의 개발은 눈부시게 이루어졌고, 현재 PP, PE, EVA, EAA 등을 포함한 폴리올레핀계, PTFE, PVC, PVDC, PS, PC, 폴리아미드계,
폴리에스터계 등 수십 가지가 넘는 다양한 소재가 상용되고 있다.1-5
유리 및 금속과 비교하였을
때, 플라스틱 포장재는 상대적으로 비활성 상태가 아니므로(not inert), 내부 제품과 플라스틱 포장재가 직접 접촉하게 되면 화합물의 이동이
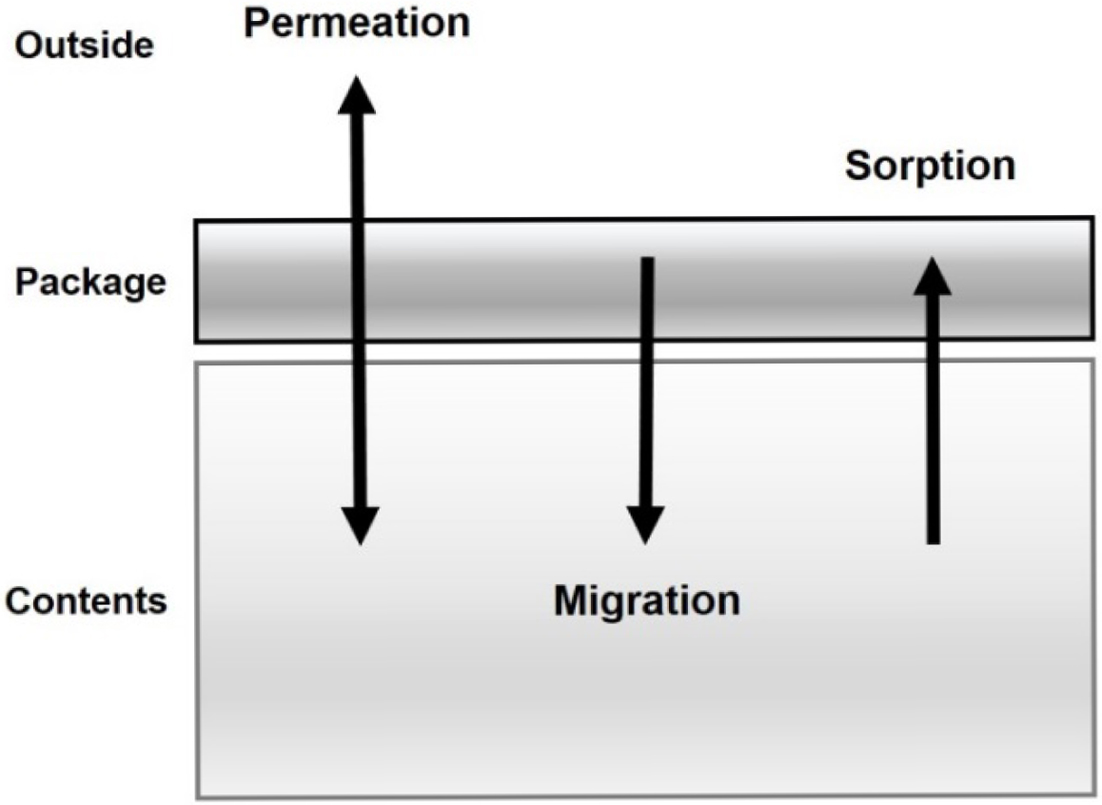
발생할 수 있다. 플라스틱 포장재와 제품 간의 대표적인 상호 작용은 Figure 1에 도시한 것과 같이 투과(permeation), 흡착(sorption),
이행(migration)이 있다. 특히 이행은 플라스틱 포장재에서 제품으로 물질이 이동하는 것인데, 고분자에 포함된 저분자 물질들은 이동성을 가지기
때문에 포장재에서 제품으로 비교적 쉽게 이동할 수 있다.6-9
일반적으로 첨가제,
단량체, 올리고머, 고분자 분해 산물, 촉매 잔사를 비롯한 중합에 사용된 잔류 화합물 등이 이행 물질(migrant)이 될 수 있다. 이행이 발생하면
제품의 관능, 물리, 화학적 특성에 영향을 줄 수 있을 뿐만 아니라, 일부 소재는 독성을 가지는 화합물을 함유하고 있는 것으로 알려져 있어 인체
건강에 잠재적으로 부작용을 끼칠 수 있다.10-15 프탈레이트 가소제, Bisphenol-A가 가장 대표적인 독성 물질로 알려져
있고, 그 외에도 스티렌, e-카프로락탐, 알파-올레핀 등의 단량체, 첨가제 이행에
대한 연구가 수행되었다.16-18
많은 국가에서 이행으로
인한 독성으로부터 소비자를 보호하기 위해 자체 지침 및 규정을 마련하고 있다. 유럽 연합에서는 regulation(EC) No 1935/2004을
통하여 모든 식품 접촉 물질에 대한 안전 및 비활성의 일반 원칙을 정하고 있으며, 물질에 따라 세부 규정을 구분하고 있다. Commission regulation(EU) No
10/2011은 플라스틱 포장재에 대한 규정으로, 이행으로 인하여 식품의 구성 성분에 허용할 수 없는 변화가 발생하지 않는 것을 전제로 하여 사용 가능한 단량체, 첨가제 및 가공조제(processing aid) 등
물질의 종류를 제한하고 이행 시험
방법에 대한 기준을 제시하고 있다.19,20 이 기준은 이행 물질의 총 질량을 제한하는 방법(overall
migration limit,
OML)과 특정 화학 물질에 대한 이행 질량을 제한하는 방법(specific migration limit, SML)으로 나눌 수 있다. OML은
포장재에서 모사품(simulant)으로 방출되는 비휘발성(non-volatile) 물질의 최대 허용량으로, 접촉 표면적에 대하여 10 mg/dm2
또는 모사품에 대하여 60 mg/kg으로 규제한다.
또한, 물질의 위험 평가(risk assessment)에 따라 SML이 지정되는 경우도 있다. 일반적으로 SML은 모사품으로 이행되는 특정 물질의
최대 허용량(mg/kg)으로 나타낸다.21
이행은 고분자 소재의
종류, 내부 접촉 물질의 농도 및 화학적 특성, 온도, 접촉 시간 등 많은 인자에 영향을 받는다. 따라서 이행 시험 조건은 실제 제품의 사용 환경을
적절하게 반영하는 것이 매우 중요하다. 그러나 실제 제품-포장 시스템에 대한 재현은 매우 복잡하기 때문에 시스템을 단순화하여 시험한다. 포장재는
균질한 것으로 가정하고 식품은 적합한 모사품으로 대체하고 제품이 사용되는 온도 및 시간에 대한 조건을 가속화하여 이행 시험에 적용한다. 특히 모사품은
이행 시험 결과에 막대한 영향을 줄 수 있으므로, 제품과 유사한 거동을 나타내는 물질로 선택해야 한다. 식품 포장재의 경우, overall
migration(OM)을 분석하기 위하여 4가지 모사품이 일반적으로 사용되는데, 수성, 산성 또는 알코올성 식품에서는 증류수(Simulant
A), 아세트산(3% acetic acid aqueous solution(pH<4.5), Simulant B), 에탄올 수용액(10%
v/v aqueous solution, Simulant C)이 대표적으로 사용되고, 지용성 식품에서는 올리브 오일(Simulant D)이 사용된다.
올리브 오일의 경우, 지용성 식품에 대한 포장재 시스템을 매우 잘 모사하여 실제에 근접한 결과를 도출할 수 있지만, 오일 성분의 비휘발성으로 인하여
시험 절차가 복잡하다는 단점을 가지고 있다. 따라서 n-heptane이나 isooctane 등의 유기 용매를 지용성 식품의 대체 모사품으로 활용하고 있다. 모사품의
종류는 규제 당국에 따라 조금씩 차이가 있지만 제품의 화학적 특성을 잘 반영하기 위하여 다양하게 변화하는 추세이고, 여러 종류의 모사품에 대하여
종합적으로 시험하기도 한다.14,22,25
화장품 산업에서도
전 세계적으로 소비자들이 안전하게 화장품을 소비할 수 있도록 제조업자와 유통 업자를 규제하려는 노력을 기울이고 있다. EU의 경우
Directive 76/768/EEC를 34년 만에 regulation(EC) No. 1223/2009으로 통합하여 2013년 7월부터 시행하였는데, 이는 지침에서 규정으로 개정하여
강제성을 부여한 것으로 1300여 개의 화합물에 대하여 사용을 금하거나 제한된 범위 내에서 사용하도록 하고 있다.26 포장재와 관련된 내용은 cosmetic
product safety report에 포함되는데, 포장재의 특성, 특히 순도 및 안정성과 관련된 사항 등이 기술되어야 한다. 실제 적용에 대한
가이드라인은 commission implementing decision 2013/674/EU에 제시되어 있는데, 이행과 관련하여서는 화장품에 대한
별도의 표준 절차 없이 식품 접촉 물질에 대한 규정 regulation(EU) No 1935/2004를 참조하도록 명시되어있다.27
이는 화장품에 의도적으로 첨가되지는 않았으나 안정성에 영향을 줄 수 있는 물질이 포함되어 있는지를 평가하는 것으로, 불가피한 미량의 불순물이라도
제품에 큰 영향이 없는 수준에서만 허용하고 있다. 따라서 화장품 포장재로부터 발생할 수 있는 이행에 대하여 점검하고 제품 안정성에 영향을 미치는지를 평가하여야 하는데, 이를 위해서는
포장 재료의 구성 및 이행에 대한 구체적인 정보가 필요하다.
본 연구에서는 EU의
식품 플라스틱 포장재 이행 시험 표준인 The European Standard EN 1186을 근거로
하여 OM 시험을 수행함으로써, 일반적으로 사용되는 화장품 용기의 이행 정도와
안정성에 대한 평가를 수행하고자 하였다.28-30 화장품에 보편적으로 사용되는 PP, LDPE, HDPE, PET(transparent & colored) 등 5종의 플라스틱
용기에 대하여 시험을 진행하였고, 화장품의 다양한 화학적 특성에 대한 전반적인 평가를 위하여 수성, 산성, 염기성, 지용성 모사품 6종을
이용하였다. 또한 일반적인 보관 조건을 고려하여 용기를 40 oC에서 10일간 모사품에 노출시키는 실험 조건을 적용하였다.24,31
이러한 조건에서 OM 양을 측정하여 EU 기준을
충족하는 가를 확인하였고, 이행이 발생한 소재에서는 GC 및 GC/MS 기법으로 이행된 물질의 성분을 확인하였다.
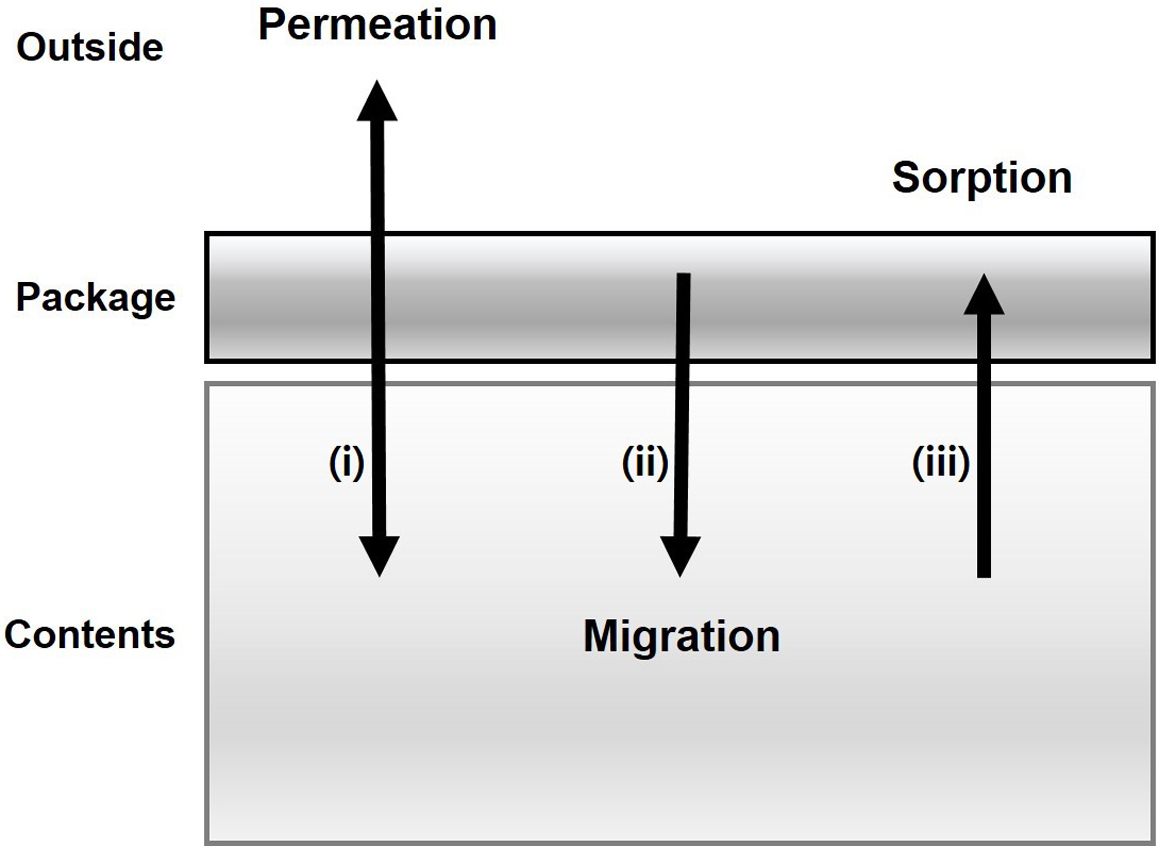
|
Figure 1 Interaction between plastic packaging and contents; (i) Permeation of gas, organic vapor, water vapor through the package, (ii) Migration of chemicals from the package into the contents, and (iii) Sorption of components from the food into the package. |
시약 및 재료. 모사품 제조에 사용된 시약은 ethyl alcohol (Daejung, 99.9%), acetic
acid(Junsei, min 99.7%), ammonia solution(Junsei, 28.0~30.0%)으로 모두 guaranteed grade이다.
GC/FID 및 GC/MS 측정에 사용된 chloroform(J. T. Baker)은 HPLC grade이고 별도의 정제 과정 없이 사용되었다.
이행 시험에 사용된
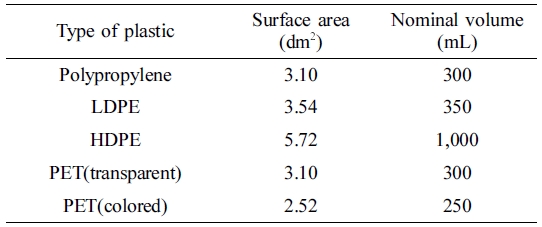
화장품 포장 용기는 Table 1에서와 같이 polypropylene(300 mL), LDPE(350 mL),
HDPE(1000 mL), 투명 PET(300 mL), 불투명
PET(300 mL) 등 총 5종이며,
이들의 표면적은 직접 측정하였다.
분석 저울 설치. OM 시험에 사용되는 저울은 표준 EN 1186-1에 따라 0.1 mg의 무게 변화를
감지할 수 있어야 한다. 본 연구에
사용된 저울은 Mettler-Toledo사의 ML204t/00 모델로, 최대 용량은 220 g, 해독도(readability)는 0.1 mg이다. 수분이나
먼지 등의 외부 오염 요인을 최소화하기 위하여 데시케이터 내부에 저울을 설치하였고 전원 공급은 배터리를 이용하였다. 데시케이터 및 외부에서 발생할
수 있는 진동의 영향을 줄이기 위하여 석정반 위에 저울을 설치하였다.
화장품 모사품(Cosmetic Simulant). 10, 50, 95% ethanol (v/v) 수용액, 3, 40% acetic acid(w/v) 수용액, ammonia 수용액(pH
10)을 모사품으로 사용하였다. Ammonia 수용액은 증류수를 첨가하여 pH를 맞추는 방법으로 제조하였다. 그 외 모사품은 부피 플라스크(volumetric
flask)를 사용하여 증류수로 농도를 맞추었다. 제조한 모든 모사품은 사용 전에 0.2 μm pore-size nylon filter를 통과시켜 불순물을 필터링하였다.
무게 측정을 위한 용기 준비 및 안정화. OM 시험에서는 포장 용기에 담았던 모사품의 일정량을
무게 측정에 적합한 용기로 옮겨서 증발시킨 후에 남아있는 비휘발성 이행 물질의 무게를 측정한다. 따라서 최종적으로 무게를 측정하는 용기의 선택
및 중량 안정화 과정이 중요하다. 분석 표준에 따르면 모사품의 증발 및 이행 물질의 무게 측정을 위한 용기로 스테인리스, 니켈, 백금, 유리 등의
다양한 소재를 사용할 수 있다. 그러나 총 중량 100 g을 넘지 않아야 하고 모사품 증발 전후에 용기의 중량 안정화 과정을 거친 후, 무게 변화가 0.5 mg 이내가 되어야 한다.
이를 위하여 용기의 중량 안정화는
105~110 oC로 설정된 오븐에서 30±15분간 보관한 후, 데시케이터에서 상온까지 식힌 뒤에 무게를 측정하는 과정을 반복한다. 본 연구에서는 바이알(wheaton
science, borosilicate glass, USP Type 1, ASTM E438 Type 1)을 모사품 증발 및 이행 물질 무게 측정
용기로 사용하였다. 또한 정확한 측정을 위하여 무게의 변화가 0.2 mg 이내가 될 때까지 안정화 과정을 반복하였다.
OM(Overall
Migration) 시험. Lint-free 와이퍼를 이용하여 플라스틱 포장재 표면의 먼지 등 오염을 제거하였다. 시험에 영향을 주지 않도록 물 등의 용매로 추가적인
세척을 하지 않았다. 이행 시험을 시작하기 전, 모사품을 시험 온도 40 oC (tolerance±1 oC)로 설정된 오븐에
미리 보관하여 모사품의 온도가 시험 온도와 동일하게 될 수 있도록 준비하였다. 시험 온도에 도달하면 모사품을 오븐에서 꺼내 포장 용기의 용량(nominal
volume) 만큼 채웠다. 한 종류의 모사품과 용기에 대하여 3개의 반복 시료를 준비하였다. 또한 모사품 자체에서 증발되지 않고 남는 물질의
무게를 보정하기 위하여 바탕(blank) 시험도 동시에 진행하였다. 모사품을 채운 플라스틱 용기와 바탕 시험에 사용될 모사품을 오븐에 넣고
10일 동안 보관하였다. 이행 시간이 완료되면 플라스틱 용기에 담겨 있던 모사품 중 200 mL를 무게 측정 바이알에 나눠 옮긴 후에 질소 농축기(EYELA,
MGS-2200)를 이용하여 모사품을 서서히 증발시켰다. 바탕 시험을 위해서도 플라스틱 용기와 접촉하지 않은 모사품을 동일한 방법으로 증발시켰다.
증발이 완료되면 바이알의 중량 안정화 과정을 진행한 후 최종 무게를 기록하였다. 이렇게 측정한 최종 무게에서 바이알 자체의 무게와 바탕 시험에
의한 모사품 잔류물 무게를 빼 줌으로써 플라스틱 용기에서 이행된 물질만의 무게를 산출하였다.
GC/FID, GC/MS 측정. GC/FID 측정에는 automatic liquid sampler가 장착된 Agilent GC7820A 기기를 사용하였다. 이동상 가스로 질소를 사용하였고,
유량은 1.2 mL/min,
inlet 온도는 300 oC로 설정하였다. GC/FID 분석에 사용된 시료는 chloroform에 녹인 후, 0.45 μm pore-size PTFE syringe filter를 이용하여 전처리하였다. 주입 부피는 0.2 μL, split ratio는 1/20로 주입하였고 분석에 사용된 GC column은 HP-5 ms (30 m, 0.32 mm i.d.,
0.25 μm film thickness)이다. 초기 오븐 온도는 50 oC로 설정하여 3분
동안 등온으로 유지한 후,
10 oC/min으로 300 oC까지 승온시키고
15분간 유지하였다.
GC/MS 측정은
automatic liquid sampler가 장착된 Agilent GC7890B/5977A inert MSD 기기를 사용하였다. 이동상 가스로
헬륨을 사용하였고, 유량은 1.0 mL/min,
Inlet 온도는 280 oC로 설정하였고, EI mode로 결과를 분석하였다. GC/MS 분석에 사용된 모든 시료는 0.45 μm pore-size PTFE syringe filter를 이용하여 전처리 하였다. 주입 부피는 0.2 μL, split ratio는 1/20로 주입하였고 분석에 사용된 GC column은 HP-5 ms(30 m, 0.25 mm i.d.,
0.25 μm film thickness)이다. 초기 오븐 온도는 50 oC로 설정하여 3분
동안 등온으로 유지한 후,
10 oC/min으로 280 oC까지 승온 시키고
20분간 유지하였다.
|
Table 1 Surface Area, Nominal Volume, and Type of Plastic Packaging Used in the Migration Test |
바탕 모사품(Blank Simulant) 증발 전·후의 무게 변화. OM을 산출하기 위해서는 용기에 노출시킨 모사품
200 mL를 증발시킨 후
남은 잔여물의 무게에서 바탕 모사품 200 mL을 증발시키고 남은 잔여물을 무게를 빼주어야 한다. 규정에서는
2개의 바탕 모사품의 무게 변화 결과를 이용하여 OM을 산출하도록 되어 있지만, 실제 실험 과정에서 발생할 수 있는 오차 범위를 예측하기 위하여
5개의 바탕 모사품을 제작하여 시험 조건에 동일하게 방치한 뒤, 증발 전·후의 무게 변화를 측정 및 비교 분석하였다. 200 mL 바탕 모사품의 증발이 완료된 후에 바이알의 외벽에 육안으로 확인 가능한
잔여물이 존재하였고, 무게 변화는
모사품의 종류에 따라 0.5~1.0 mg 수준의 차이가 있었다(Table 2). 이러한 무게 변화는
용매에 존재하는 미량의 불순물이나 끓는점이 높은 다량의 수용액을 증발시키는 과정에서 발생하는 오염으로 판단된다.
OM 시험. EU 규제 표준에서 OM(M, mg/dm2)은
용기 표면적에 대한 이행 물질의 양으로 나타낸다.29

수식에서 ma는
용기 시료에 노출시킨 모사품을 증발시킨 후에 남은 잔여물의 무게(g), mb는 바탕 모사품 증발시킨 후 남은 잔여물의 무게(g), S는 시료의 표면적(dm2)을
나타낸다. 용기의 용량이
200~500 mL인 경우에는,
용기에 노출시킨 모사품 중 200 mL만 취하여 증발시키고
남은 잔여물의 무게를 측정한다. 따라서 이를 보정한 식 (2)을 이용하여 OM을 산출한다.29
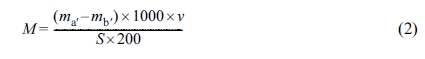
식 (2)에서 v는
플라스틱 용기를 채우는데 사용된 모사품의 부피(mL)로 용기의 용량을 나타낸다. ma'는 시료에
노출시킨 모사품 200 mL를 증발시킨 후에
남은 잔여물의 무게(g), mb'는 바탕 모사품 200 mL를 증발시킨 후
남은 잔여물의 무게(g)를 의미한다.
그러나 플라스틱 용기의
용량이 500 mL 이상에서 10 L 이하인 경우 또는 시료의 표면적을 측정할 수 없는
경우에 한하여 모사품 부피에 대한 이행 물질의 총양으로 나타낸다.29

ML은 모사품으로 이행되는 모든 물질의 총합(mg/kg), ma는
시료에 노출시킨 모사품을 증발시킨 후에 남은 잔여물의 무게(g), mb는 바탕 모사품 증발시킨 후 남은 잔여물의
무게(g), V는 플라스틱 용기의 용량(L)을 나타낸다. EU 규제 표준에 의하여 모사품의 종류에 관계없이 1 L는 1 kg과 같다고 가정한다.29 특히, 용기의
용량이 500 mL 이상, 10 L 이하인 경우에는 용기에 노출시킨 모사품 중 200 mL만 취하여 증발시키고
남은 잔여물의 무게를 측정한다. 따라서 이를 보정한 식 (4)를 이용하여 OM을 산출한다.29

식 (4)에서 ma'는 시료에
노출시킨 모사품 200 mL를 증발시킨 후에
남은 잔여물의 무게(g), mb'는 바탕 모사품 200 mL를 증발시킨 후
남은 잔여물의 무게(g)를 의미한다. 따라서 HDPE(1000 mL) 용기만 식 (4)를 활용하고, 용량이 적은 나머지
용기들은 모두 식 (2)를 활용하여 각각의 OM을 산출하였다.
40 oC에서 10일간 보관한 5종의 플라스틱 용기의 OM 시험 결과, Table 3에 정리된 것과 같이, 모든 모사품에
대하여 이행이 거의 일어나지 않거나 미량의 이행만 발생한 것을 확인할 수 있었다. PP, LDPE, HDPE 등 폴리올레핀계 플라스틱 용기의 경우에
95% ethanol 수용액에서 상대적으로 많은 이행이 일어났지만 EU의 이행 한계 기준값(접촉 표면적에 대하여 10 mg/dm2)을
초과하지는 않았다. 이를 통해 화장품의 일반적인 사용 조건에서는 폴리에스터계 고분자인 PET가 폴리올레핀계 고분자보다 대상 모사품에 대하여 활성이
더 적다는 것을 확인할 수 있었다. 선행 연구에 따르면 PET는 소량의 dimer에서 pentamer에 이르는 올리고머를 함유하고 있고, 이런
물질들에 의한 이행이 일어날 수 있다. 이러한 PET의 이행은 수용성 모사품보다는 지용성 모사품에서 잘 일어나고, 상온보다는 장기간 가열 조건에
노출될 경우에 많이 발생하는 것으로 알려져 있다17,32-34
이행 물질의 정성 분석. 이행 물질의 정성 분석을 위하여 잔여물을
chloroform에 용해시킨 후 GC/FID 및 GC/MS 분석을 수행하였다. 1.0 mg/dm2 또는 mg/kg 이하의 OM이 일어난 용기의 잔여물에서는 유의미한 피크는 검출되지 않았고, 바탕 모사품에서와 유사한 패턴의 크로마토그램을 얻을
수 있었다. 이러한 결과는 이행에 의한 잔여물보다는 모사품 자체에 존재할 수 있는 미량의 불순물이나 증발 과정에서 발생할 수 있는 잔여물이 주성분이라는
것을 보여준다.
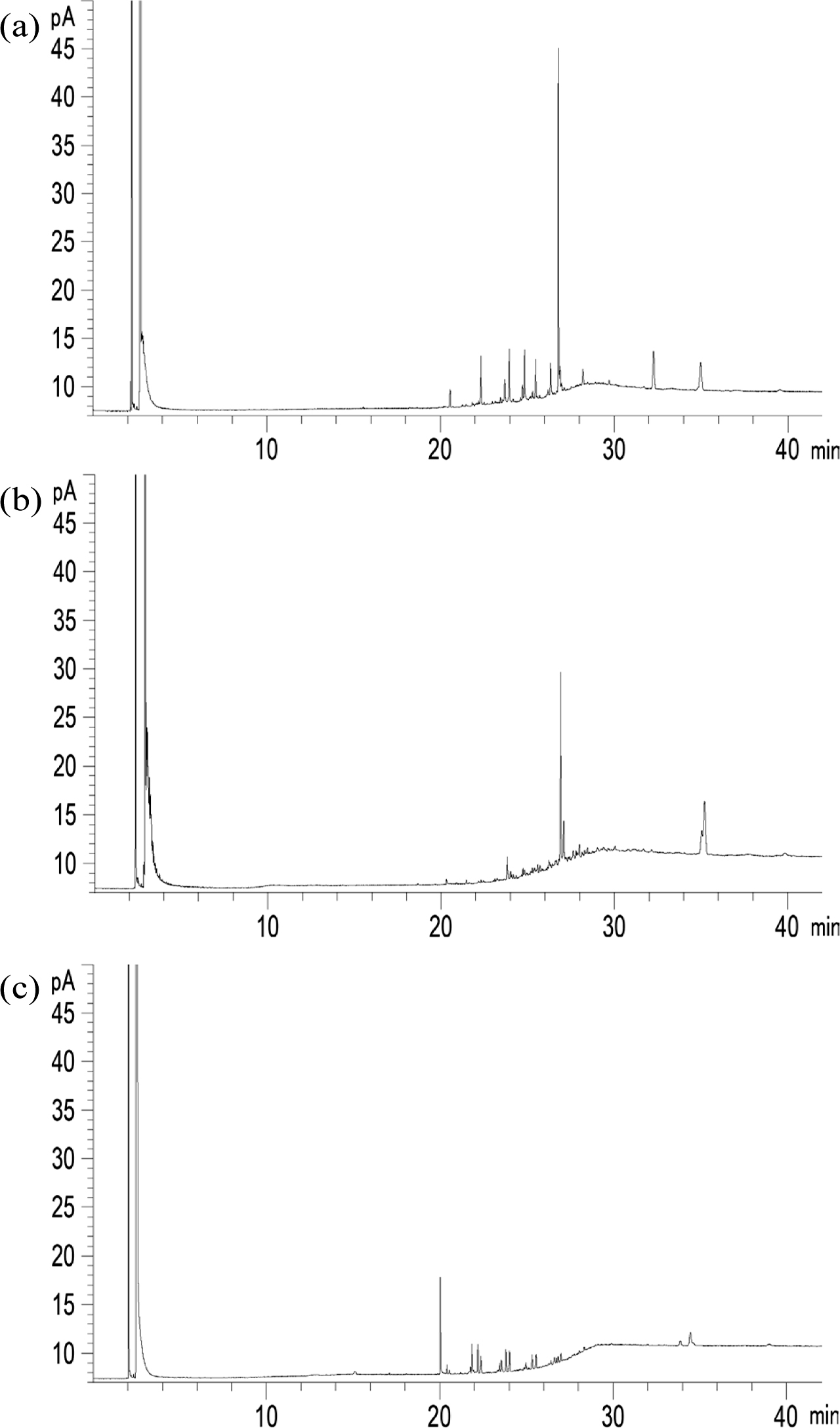
그러나
Figure 2에 도시한 것과 같이 95% ethanol 수용액의 경우, 이행이 비교적 많이 일어난 폴리올리핀계 플라스틱 용기의 잔여물에서는 여러 신호가 검출되었다. 이들
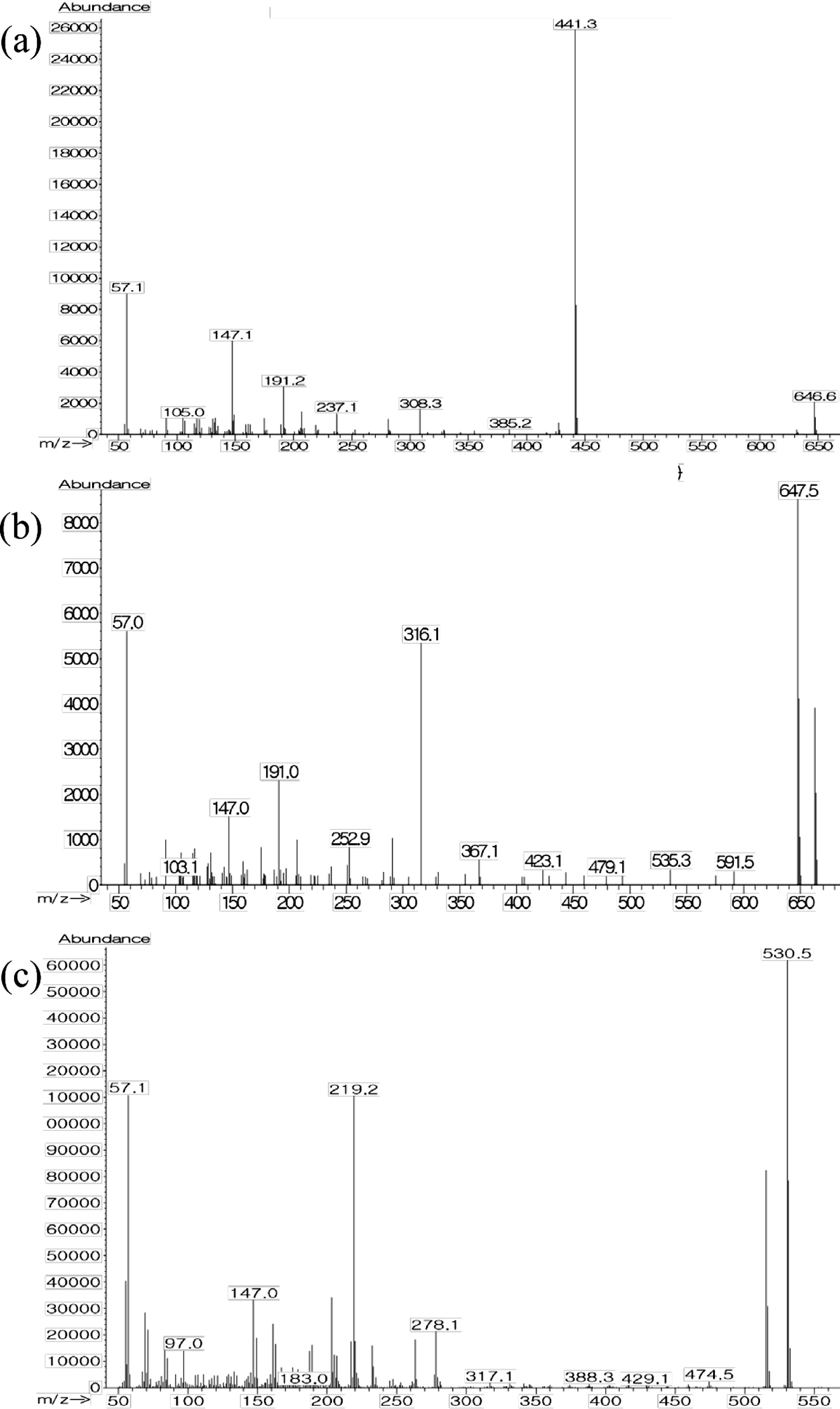
신호의 정성 분석을 위하여 GC/MS를 측정한 결과, 일부 신호의 정성 분석이 가능하였다. 이 중 주요한 신호는 Figure 3에서 확인할 수 있는 것과 같이
Irganox 1076이나 Irgafos 168 등의 산화방지제였고, 그 외의 신호들은 중합체의 분해(degradation)에 의해 발생한 올리고머로 판단된다.35
PP, PE 등의 폴리올레핀 용기로부터의 산화방지제 이행은 식품 용기에서도 쉽게 일어나 관련 연구가 많이 이루어졌다.36-40 Irganox 1076의 경우에는 commission regulation(EU) No
10/2011에서 SML 6 mg/kg으로 규제되고
있으므로 지용성 제품의 포장 용기로 사용할 경우 주의가 필요하다.20
|
Figure 2 GC/FID chromatograms of migration residues from (a) PP; (b) LDPE; (c) HDPE into 95% ethanol simulant after evaporation. |
|
Figure 3 Mass spectra of migration residues in 95% ethanol simulant: (a) Irgafos 168 from PP; (b) oxidized form of Irgafos 168 from PP and LDPE; (c) Irganox 1076 from LDPE and HDPE. |
|
Table 2 Weight of Residue after Evaporation of 200 oC Blank Simulant |

aEach value is the mean for five samples ± standard deviation. |
|
Table 3 Overall Migration of Plastic Articlesa |
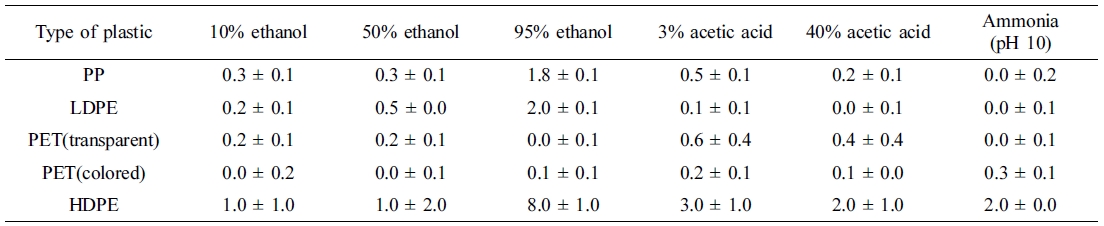
aNote the OM values for PP, LDPE and PET were calculated in mgm g/dm2, while for HDPE was calculated in mg/kg.29 |
본 연구에서는 화장품의
1차 포장재로 많이 사용되는 PP, LDPE, HDPE, PET(transparent & colored) 5종류의 플라스틱 용기에 대하여
EU의 식품 용기 이행 시험 표준에 근거하여 OM 시험을 진행하였다. 화장품의 일반적인 보관 조건을 반영하기 위하여 이행 시험 조건은 40 oC에서 10일간 보관하는 것으로 하였고, 화장품 제형의 다양한 화학적 특성에 대한 전반적인 평가를 위하여 수성,
산성, 염기성, 지용성을 대표할 수 있는 모사품 6종에 대하여 시험을 진행하였다. 위와 같은 이행 시험 조건에서 5종의 시험 용기는 EU에서 제시한
OML 기준(접촉 표면적에 대하여 10 mg/dm2 또는 모사품에 대하여
60 mg/kg)을 충족하였다.
특히 식품 규정에는 없는 염기성 모사품에 대한 이행 시험 결과를 통해 모발 관리 제품이나 세정제와 같은 알칼리 제형에 대한 용기의 안정성을 확인할
수 있었다.
그러나 PP,
LDPE, HDPE를 비롯한 폴리올레핀 계열의 경우, 지용성 모사품인 95% ethanol 수용액에서 규제치 이하이지만 비교적 이행이 많이 일어난
것을 확인하였다. 이를 GC/MS 정성 분석한 결과 주요 이행 물질은 올리고머 및 산화방지제 등의 첨가제로 검출되었다. 따라서 폴리올레핀 포장재의
사용에 있어서는 반드시 화장품 특성을 고려해야 한다.
- 1. M. Kunal C, D. Akhilesh, and B. S. Kumar, Int. J. Pharm. Chem. Sci., 1, 1282 (2012).
- 2. J. Lange and Y. Wyser, Packag. Technol. Sci., 16, 149 (2003).
-

- 3. O. G. Piringer and A. L. Baner, Plastic Packaging Materials for Food: Barrier Function, Mass Transport, Quality Assurance, and Legislation, John Wiley & Sons, USA, 2008.
-

- 4. N. P. Mahalik and A. N. Nambiar, Trends Food Sci. Technol., 21, 117 (2010).
-

- 5. A. L. Andrady and M. A. Neal, Phil. Trans. R. Soc. B, Biol. Sci., 364, 1977 (2009).
-

- 6. O. G. Piringer and A. L. Baner, Plastic Packaging: Interactions with Food and Pharmaceuticals, John Wiley & Sons, USA, 2008.
-

- 7. R. C. Thompson, C. J. Moore, F. S. vom Saal, and S. H. Swan, Phil. Trans. R. Soc. B, Biol. Sci., 364, 2153 (2009).
-

- 8. H. Hotchkiss, Food Addit. Contam., 14, 601 (1997).
-

- 9. C. H. Mannheim and N. Passy, Packag. Technol. Sci., 3, 127 (1990).
-

- 10. H. M. Koch and A. M. Calafat, Phil. Trans. R. Soc. B, Biol. Sci., 364, 2063 (2009).
-

- 11. C. E. Talsness, A. J. M. Andrade, S. N. Kuriyama, J. A. Taylor, and F. S. vom Saal, Phil. Trans. R. Soc. B, Biol. Sci., 364, 2079 (2009).
-

- 12. O. W. Lau and S. K. Wong, J. Chromatogr. A, 882, 255 (2000).
-

- 13. S. Arvanitoyannis and L. Bosnea, Crit. Rev. Food Sci. Nutr., 44, 63 (2004).
-

- 14. K. Bhunia, S. S. Sablani, J. Tang, and B. Rasco, Compr. Rev. Food Sci. Food Saf., 12, 523 (2013).
-

- 15. D. Meeker, S. Sathyanarayana, and S. H. Swan, Phil. Trans. R. Soc. B, 364, 2097 (2009).
-

- 16. M. S. Tawfik and A. Huyghebaert, Food Addit. Contam., 15, 592 (1998).
-

- 17. T. H. Begley, M. L. Gay, and H. C. Hollifield, Food Addit. Contam., 12, 671 (1995).
-

- 18. B. Marcato, S. Guerra, M. Vianello, and S. Scalia, Int. J. Pharm., 257, 217 (2003).
-

- 19. Regulation (EU) No 1935/2004 of the EUROPEAN PARLIAMENT AND OF THE COUNCIL of 27 October 2004 on materials and articles ntended to come into contact with food and repealing Directives 80/590/EEC and 89/109/EEC.
- 20. Commission Regulation (EU) No 10/2011 of 14 January 2011 on plastic materials and articles intended to come into contact with food.
- 21. European Standard EN 13130-1:2004, Materials and articles in contact with foodstuffs – Plastics substances subject to limitation – Part 1: Guide to test methods for the specific migration of substances from plastics to foods and food simulants and the determination of substances in plastics and the selection of conditions of exposure to food.
- 22. E. L. Bradley, L. Castle, S. M. Jickells, K. A. Mountfort, and W. A. Read, Food Addit. Contam., 26, 574 (2009).
-

- 23. V. Gnanasekharan, J. D. Floros, and J. R. Glacin, Crit. Rev. Food Sci. Nutr., 37, 519 (1997).
-

- 24. K. Grob, Food Control, 19, 263 (2008).
-

- 25. Y. W. Kim, D. H. Kim, and J. Y. Bae, Polym. Korea, 42, 654 (2018).
-

- 26. Regulation (EC) No 1223/2009 OF THE EUROPEAN PARLIAMENT AND OF THE COUNCIL of 30 November 2009 on cosmetic roducts.
- 27. Commission implementing decision of 25 November 2013 on Guidelines on Annex I to Regulation (EC) No 1223/2009 of the European arliament and of the Council on cosmetic products
- 28. BS EN 1186-1:2002, Materials and articles in contact with foodstuffs – Plastics – Part 1 : Guide to the selection of conditions and test methods or overall migration.
- 29. BS EN 1186-9:2002, Materials and articles in contact with foodstuffs – Plastics – Part 9 : Test methods for overall migration into aqueous food imulants by article filling.
- 30. BS EN 1186-14:2002, Materials and articles in contact with foodstuffs – Plastics – Part 14 : Test methods for substitute tests for overall migration into iso-octane and 95% aqueous ethanol.
- 31. E. Fasano, F. Bono-Blay, T. Cirillo, P. Montuori, and S. Lacorte, Food Control, 27, 132 (2012).
-

- 32. Shiono, Anal. Chem., 51, 14 (1979).
- 33. R. Ashby, Food Addit. Contam., 5, 1 (1988).
- 34. L. Castle, A. Mayo, C. Crews, and J. Gilbert, J. Food Prot., 52, 337 (1989).
-

- 35. Al-Malaika, Adv. Polym. Sci., 169, 121 (2004).
- 36. A. Garde, R. Catala, and R. Gavara, J. Food Prot., 61, 8 (1988).
- 37. A. Garde, R. Catala, R. Gavara, and R. J. Hernandez, Food Addit. Contam., 18, 750 (2001).
-

- 38. M. S. Dopico-García, J. M. López-Vilariñó, and M. V. González-Rodríguez, J. Agric. Food Chem., 55, 3225 (2007).
-

- 39. Y. Gao, Y. Gu, and Y. Wei, J. Agric. Food Chem., 59, 12982 (2011).
-

- 40. G. Beldì, S. Pastorelli, F. Franchini, and C. Simoneau, Food Addit. Contam. Part A Chem. Anal. Control Expo. Risk Assess., 29, 836 (2012).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(2): 170-176
Published online Mar 25, 2020
- 10.7317/pk.2020.44.2.170
- Received on Oct 29, 2019
- Revised on Dec 26, 2019
- Accepted on Dec 26, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Sangdoo Ahn, and Hyoyeon Yu
-
Department of Chemistry, Chung-Ang University, Seoul 06974, Korea
- E-mail: sangdoo@cau.ac.kr, hyoyeonyu@gmail.com
- ORCID:
0000-0003-3803-9210, 0000-0002-1094-5564








 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.