- Preparation and Thermoresponsive Properties of 2-Hydroxy-3-butoxypropyl Hydroxyethyl Cellulose and Its Hydrogel Crosslinked with Epichlorohydrin
Department of Organic Materials and Fiber Engineering, Soongsil University, Seoul 06978, Korea
- 2-히드록시-3-부톡시프로필 히드록시에틸 셀룰로오스 및 이를 에피클로로히드린으로 가교시킨 수화젤의 제조와 열감응 특성
숭실대학교 유기신소재·파이버공학과
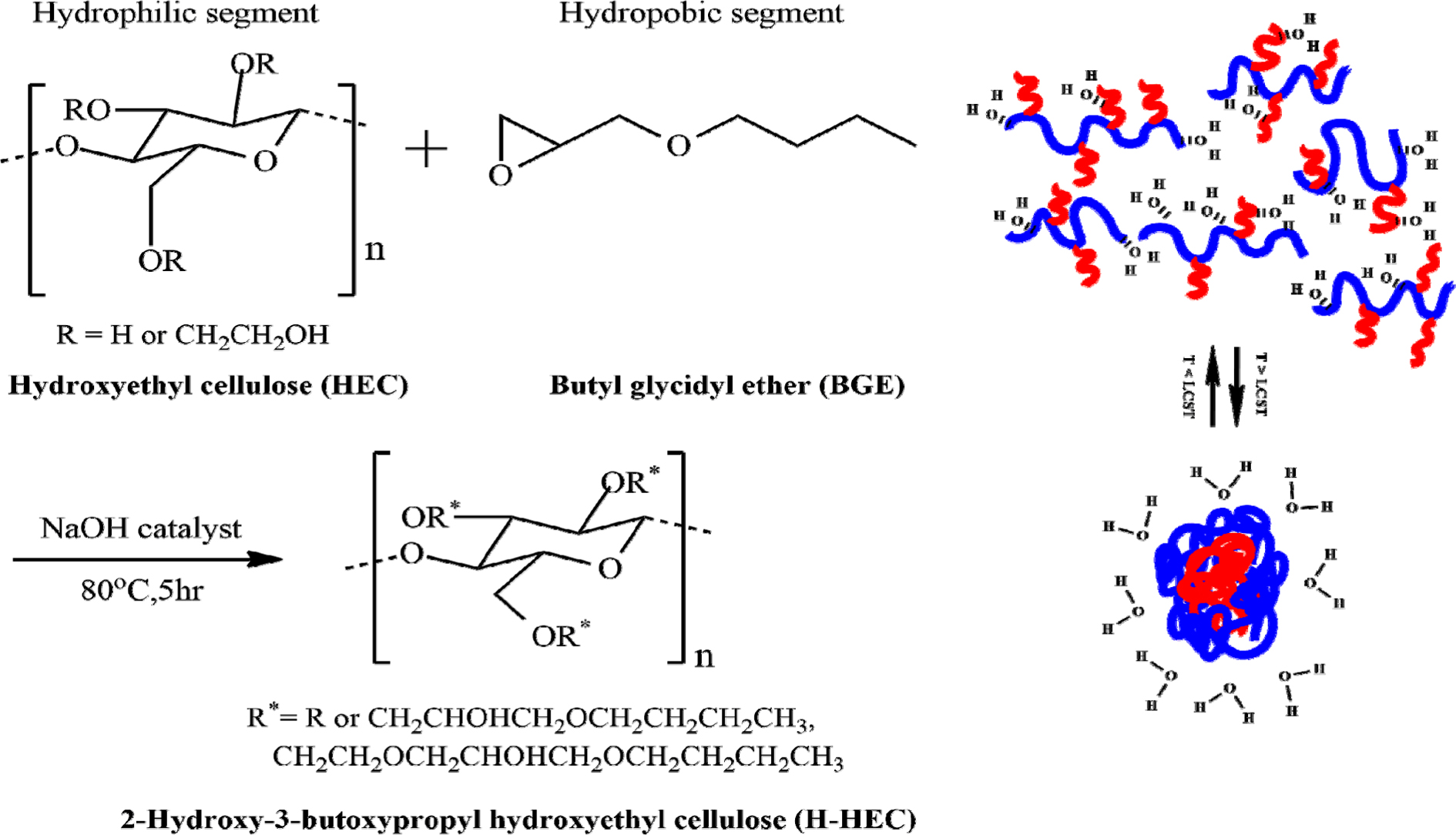
Hydroxyethyl cellulose (HEC)
with hydroxyethyl group substitution degree (DS) 1.0 and molar substitution
degree (MS) 2.0 was reacted with butyl glycidyl ether (BGE) to synthesize
2-hydroxy-3-butoxypropyl hydroxyethyl cellulose (H-HEC). The properties of
H-HEC prepared by varying BGE concentrations were analyzed using 1H
NMR, FTIR, and UV-Vis spectrophotometer. The aqueous solution of H-HEC showed a
lower critical solution temperature (LCST), indicating that H-HEC is a
thermoresponsive polymer. As the concentration of reacting BGE during H-HEC
synthesis increased, the MS of hydroxy-butoxypropyl group increased linearly
and LCST decreased linearly. H-HEC was crosslinked with epichlorohydrin (ECH)
to prepare a thermoresponsive hydrogel. Measurement of the swelling property in
distilled water showed a maximum swelling ratio when H-HEC was crosslinked at a
certain ECH concentration. H-HEC retained the Cellulose II crystal structure,
but the hydrogel obtained by crosslinking with ECH showed no crystal structure.
히드록시에틸기의 치환도(DS)가 1.0이고 몰 치환도(MS)가
2.0인 히드록시에틸 셀룰로오스(HEC)에 부틸글리시딜에테르(BGE)를 반응시켜 2-히드록시-3-부톡시프로필
히드록시에틸 셀룰로오스(H-HEC)를 합성하였다. BGE 농도를
달리하여 제조된 H-HEC의 치환도에 따른 특성을 1H NMR, FTIR, UV-Vis 분광광도계 등을 이용하여 분석하였다.
H-HEC의 수용액은 하한임계 용해온도(LCST)를 나타내어 H-HEC가 열감응형 고분자임을 보여주었다. H-HEC 합성시 반응시키는 BGE의 농도가 커짐에 따라 히드록시-부톡시프로필기의 몰 치환도는
직선적으로 증가하면서 LCST는 직선적으로 감소하였다. H-HEC를
에피클로로히드린(ECH)으로 가교시켜 열감응성 수화젤을 제조하였으며,
이들의 증류수에서의 팽윤성을 측정한 결과 특정 ECH 농도로 가교시킨 경우 최대팽윤비를
나타내었다. H-HEC는 셀룰로오스 II 결정구조를 유지하였지만, ECH로 가교시킨 수화젤은 결정구조를 나타내지 않았다.
2-Hydroxy-3-butoxypropyl hydroxyethyl cellulose (H-HEC)
was synthesized by reacting hydroxyethyl cellulose with butyl glycidyl ether
and its thermoresponsive properties such as LCST were investigated. The
swelling and shrinking of the H-HEC hydrogel obtained by crosslinking H-HEC
with epichlorohydrin according to temperature change were also studied.
Keywords: 2-hydroxy-3-butoxypropyl hydroxyethyl cellulose, butyl glycidyl ether, epichlorohydrin, hydrogel, thermoresponsive property
이 연구는 산업통상자원부
및 산업기술평가관리원(KEIT)의 연구비 지원으로 수행되었으며(과제번호 10060069), 이에 감사드립니다.
선형 폴리사카라이드로
자연에서 가장 풍부한 천연 고분자인 셀룰로오스는 강한 수소결합이 존재하기 때문에 결정성이 높고 용융되기 전에 분해되며 물이나 다른 유기용매에 대한
용해도가 낮아 그 활용이 매우 제한적이라는 단점이 있다. 이러한 한계점을 보완하기 위해 에스테르화(esterification), 에테르화(etherification)
등의 화학적 개질을 통해 셀룰로오스 에스테르, 셀룰로오스 에테르, 질산 셀룰로오스 등의 다양한 종류의 셀룰로오스 유도체들이 합성되어 사용되고 있다.
셀룰로오스 유도체들은 치환기의 종류, 분자량, 치환도 등에 따라 다양한 성질을 나타내는데, 특히 친수성기가 포함되면 수용성 고분자로 되기 쉽다.
이들은 대부분 환경 친화적이고 무독성이며, 생분해가 가능하고 생체 적합성이 매우 우수하다는 특성이 있어 섬유, 필름, 포장 용기, 의약품, 식품
등 다양한 분야에 사용되고 있다.1,2
이들 중에서 히드록시에틸
셀룰로오스(HEC)는 셀룰로오스의 히드록시기(-OH)에 에틸렌 옥사이드나 클로로에탄올을 반응시켜 합성되는1,3 비이온성 셀룰로오스
에테르이다. 셀룰로오스도 친수성을 나타내지만 HEC는 친수성이 더 커지며 히드록시에틸기의 치환도에 따라 물에 대한 용해도가 커져 수용성화되며,
증점제로 식품, 화장품, 수용성 페인트 분야에 사용된다.1,3-6
한편, 수화젤은
3차원 네트워크 구조를 가지며 다량의 수분을 함유할 수 있는 친수성 고분자 소재로, 수용성을 나타내는 고분자를 가교시켜 제조된다. 건조된 상태의
수화젤은 종류에 따라 자신 무게의 몇 십배~천배 이상의 수용액을 흡수할 수 있어 화장품, 바이오 재료, 약물전달 시스템 등 다양한 분야에 활용된다.
가교결합에 의해 생성된 3차원 네트워크 구조는 공유결합, 수소결합 또는 물리적 응집 등에 의해 형성된다. 고분자의 화학구조나 가교도 등에 따라
팽윤도의 조절이 가능하여 다양한 형태와 성질을 가진 수화젤을 제조할 수 있으며, 열이나 pH, 또는 화학약품 등 외부자극에 응답하는 자극 응답형
및 지능형 고분자를 이용한 수화젤에 대한 연구도 많이 진행되고 있다.7-11 수화젤에 사용되는 대표적인 고분자로는 폴리(비닐
알콜)(PVA)과 폴리(N-이소프로필 아크릴아마이드)(PNIPAAm) 등이 있다. 셀룰로오스, 키토산, 알긴산, 히알루론산, 덱스트란
등의 천연고분자를 기반으로 하는 수화젤은 생물학적 조직과 유사하다는 특성이 있어 생체적합성이 뛰어나고 네트워크 내에 약물을 쉽게 분산시키고 방출할
수 있어 그 이용성이 증가하고 있으며, 특히 바이오메디컬 분야에서 많이 연구되어지고 있다.7,12-19
수화젤의 출발 원료로
셀룰로오스도 많이 사용되는데 셀룰로오스는 결정구조를 가지고 있기 때문에 형태를 잘 유지할 수 있는 수화젤을 제조할 수 있지만, 물이나 유기용매에
잘 용해되지 않기 때문에 팽윤 특성에 한계가 있고 수용성 활성 물질을 담지하는데 장애가 된다는 단점이 있다. 따라서 최근에는 셀룰로오스에 셀룰로오스
유도체를 혼합시켜 수화젤을 제조하거나15 HEC와 같은 수용성 셀룰로오스 유도체 만을 사용한 수화젤을 제조하여 셀룰로오스 수화젤의
단점을 보완하는 연구가 이루어지고 있다.16,20
몇몇 셀룰로오스 유도체는
온도, 전기장, 자기장 등의 물리적 자극이나 pH, 이온 등의 화학적 자극 등의 외부 신호자극에 반응하는 고분자이다. 이러한 자극응답형 고분자는
약물전달 시스템, 티슈 엔지니어링, 바이오센서 등의 분야에서 많이 연구되어지고 있는데, 이 중에서 히드록시프로필 셀룰로오스(HPC) 같은 열감응성
고분자는 온도 변화에 의해 수용액 상에서 상전이가 이루어진다.21-24 열감응성 고분자는 분자 내에 친수성기와 소수성기가 적절히
존재하여야 하며, 특정 온도 이하에서는 높은 용해도를 보이다가 특정 온도 이상에서 상분리가 되는 하한임계 용해온도(LCST, lower
critical
solution temperature) 거동을 보이는 것과, 특정 온도 이하에서 상분리가 되다가 특정 온도 이상에서 높은 용해도를 보이는 상한임계
용해온도(UCST, upper critical solution temperature) 거동을 보이는 고분자로 나뉘어진다. 이러한 열감응성을 나타내는 셀룰로오스 유도체로부터 수화젤을
제조하면 어떤 온도 이하에서는 팽윤되지만 어떤 온도 이상에서는 수축하는 상전이 특성을 나타내지만, 셀룰로오스 유도체 수화젤들은 친수성이 아주 큰
고분자로부터 제조한 수화젤에 비해 팽윤 특성은 좋지 않다.
본 연구에서는 이소프로필
알콜(IPA) 수용액을 반응매개체로 하여 친수성 HEC에 소수성기를 갖는 부틸글리시딜에테르(BGE)를 반응시켜 다양한 온도 범위의 LCST를 나타내는
열감응성 고분자인 2-히드록시-3-부톡시프로필 히드록시에틸 셀룰로오스(이하 H-HEC로 약하여 나타냄)를 합성하였다. 1H NMR 분석으로 여러 조건에서 합성된 H-HEC의 몰
치환도(molar substitution, MS)를 구하였으며, FTIR, UV-Vis 분광광도계 등을 사용하여 LCST 거동을 분석하였다. 또한
합성된 H-HEC를 에피클로로히드린(ECH)으로 가교시킨 수화젤을 제조하였다. 이때 가교제인 ECH 농도가 얻어진 수화젤의 팽윤 거동에 미치는
영향에 대해 조사하였으며, 2-히드록시-3-부톡시프로필기의 몰 치환도가 일정한 H-HEC를 여러 가지 농도의 ECH로 가교시킨 수화젤들의 팽윤
거동과 기타 특성들을 분석하였다.
본 연구는
H-HEC 및 이를 ECH로 가교시킨 수화젤을 제조하는 방법과 그 특성들을 분석한 것이지만, 이들에 대한 것들이 최종 목적이 아니라 이후 카복시메틸
셀룰로오스(CMC)와 같이 이온성을 갖는 셀룰로오스 유도체와 본 연구에서 합성된 H-HEC를 함께 사용한 혼성수화젤을 제조하여 열과 pH와 같은
다중자극에 응답하는 셀룰로오스계 수화젤을 제조하는 연구에 대한 선행 연구결과로 제시된 것이다.
시료 및 시약. HEC는 무수글루코스 단위(AGU)에 존재하는 3개의
히드록시기(-OH)에 대한 히드록시에틸기 치환도(DS)가 1.0이고 몰 치환도(MS)가 2.0이며 수평균 분자량이 약 250000 g/mol인 분말상의 Sigma Aldrich사 제품을,
XRD 비교용으로 사용한 셀룰로오스 I(a-cellulose)도 Sigma Aldrich사 제품을
사용하였다. BGE(분자량 130.19 g/mol)는 순도 98.0% 이상인 TCI사 제품을, 에피클로로히드린(ECH), 이소프로필 알콜(IPA),
NaOH, HCl, 아세톤 등은 삼전정밀화학사 제품을, 디메틸술폭사이드(DMSO)-d6는 Cambride
Isotope Laboratories사 제품을 사용하였으며, 이들은 모두 정제하지 않고 그대로 사용하였다.
2-히드록시-3-부톡시프로필 히드록시에틸 셀룰로오스(H-HEC)의 합성. 여러 LCST를 갖는 H-HEC를 합성하기 위해 교반기,
온도계, 온도 조절기, 냉각기, 적하 깔때기, 질소 유입구가 장착된 250 mL의 4구 플라스크에서 반응을 진행하였다. 질소 기류
하에서 용매인 50%(v/v) IPA 수용액에 대해 HEC가 10%(w/v)가 되게 하고, 계산된 양의 BGE를 첨가하여 교반시키며 용해시킨 후
알칼리 촉매인 NaOH를 HEC에 대해 20%(w/wpolymer) 투입하여 80 oC에서 5시간 동안 교반시키면서 반응시켰다. 반응물을
상온으로 냉각시킨 뒤 5 M (18.25%(w/v)) HCl로 중화시키고 다량의 아세톤에
침전시켜 여과한 후, 아세톤 용매로 다시 수차례 수세하여 미반응 BGE 및 NaOH를 제거하였다. 이들을 감압여과한 후 진공오븐에서 24시간 건조하여
여러 히드록시-부톡시프로필기 치환도를 가지는 H-HEC를 얻었다. 이때의 반응식은 Scheme 1과 같다. 이후에서 2-히드록시-3-부톡시프로필 히드록시에틸 셀룰로오스는 “H-HEC”로 표기하였으며,
특별히 2-히드록시-3-부톡시프로필기의 치환도가 x인 화합물은 “Hx-HEC”라고 나타내었다(치환도를
구하는 방법은 뒤에서 설명).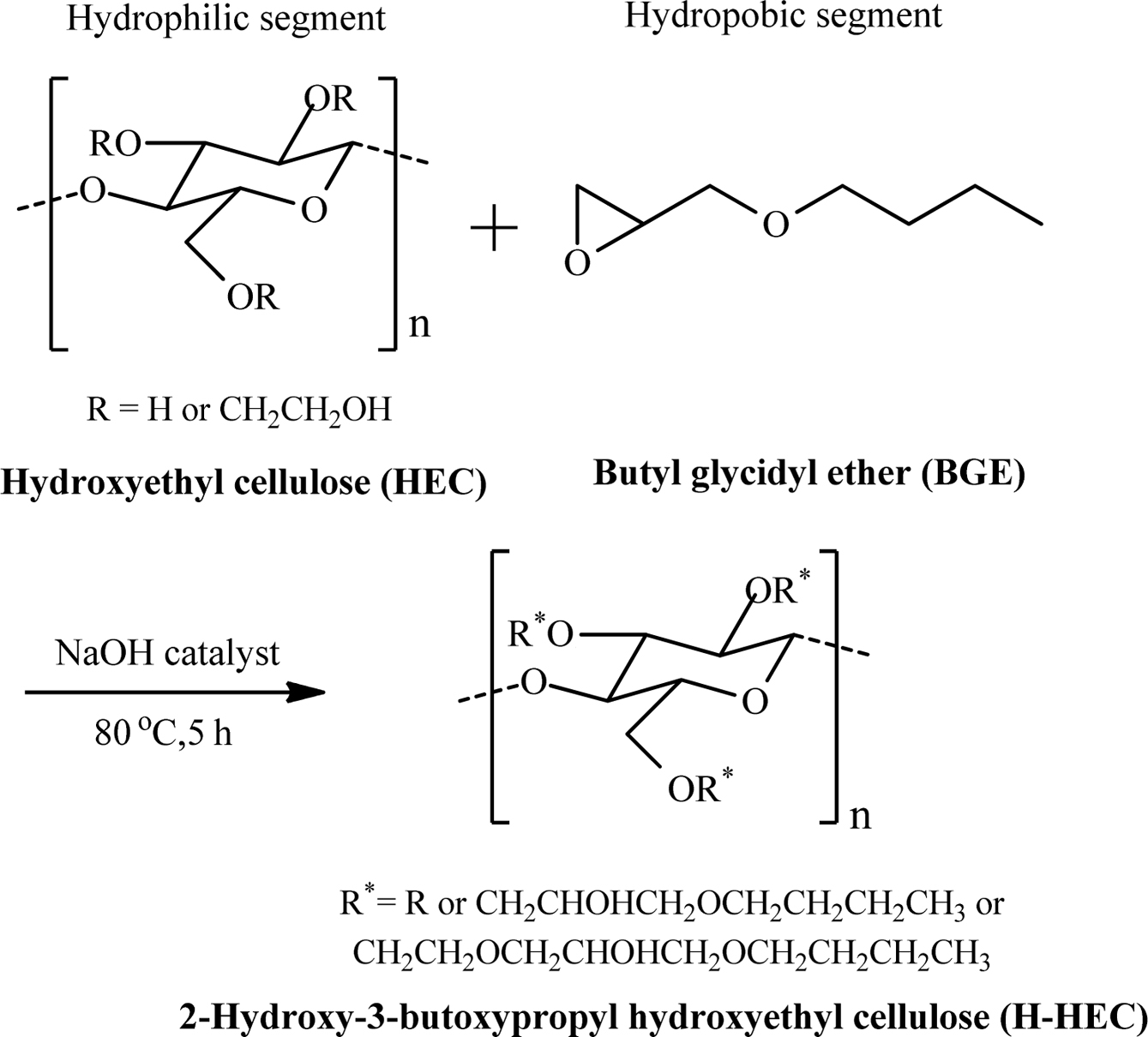
Scheme 1. Scheme for the synthesis of 2-hydroxy-3-butoxypropyl hydroxyethyl cellulose (H-HEC) by reacting hydroxyethyl cellulose (HEC) with butyl glycidyl ether (BGE).
CE-H-HEC
수화젤의 제조. H-HEC를 상온에서 10 mL의 5 M(20%(w/v)) NaOH 용액에서 1시간 동안 교반하여
용해시킨 후, 가교제인 ECH를 첨가하고 충분히 혼합시킨 후 80 oC에서 24시간 동안 반응시켰다. ECH는 사용하는 셀룰로오스 유도체의 AGU 당 0.2~2.0 몰비 농도로
변화시켜 첨가하여 반응시켰다. 얻어진 수화젤은 다량의 증류수에서 일주일 이상 수세하여 미반응 NaOH 및 ECH를 제거하고 열풍건조기에서 무게
변화가 없을 때까지 건조시킨 후 이후의 실험 및 분석에 사용하였다. 이때 Hx-HEC를 ECH로 가교반응시켜 얻은
수화젤은 “CE-Hx-HEC 수화젤”로 표기하였으며, 특별히 ECH 농도를 AGU에 대한 몰비 y로
하여 가교시켜 얻은 수화젤은 “CEy-Hx-HEC 수화젤”로 나타내었다.
수화젤의 팽윤비 및 수축비 측정. 건조시킨 CE-H-HEC 수화젤을 20~50 oC의 다양한 온도의 증류수에서 24시간 동안 팽윤시켜
팽윤평형에 도달시켰다. 여과지를 이용하여 표면의 용액을 제거하여 팽윤 무게(Ws)를 측정하고, 이를 진공 건조시켜
건조 무게(Wd)를 측정하여 식(1), (2)에 의해 팽윤비(Seq)와 수축비(DR,
deswelling ratio)를 계산하였다. 이때 수화젤은 일정한 무게(약 0.5 g)로 절단하여 사용하였다.

여기서, Weq는
팽윤 평형에 도달한 수화젤의 무게(g)이고, Wt는 팽윤된 상태의 무게(g)이며, Wd는
건조된 수화젤의 무게(g)이다.
동결 건조 및 FE-SEM 측정. 10 oC와 50 oC에서 각각 증류수에 침지시켜 팽윤 평형에 도달시킨 수화젤을
액체 질소에 급냉시킨 뒤 동결건조기(FD8508,
Ilshinbiobase 사)를 사용하여 48시간 이상 동결 건조하였다. 동결 건조된 시료의 단면을 금으로 코팅한 후, Carl Zeiss 사의
GeminiSEM 300, field emission scanning electron microscope(FE-SEM)를 사용하여 관찰하였다.
기타 측정. Bruker 사(독일)의 FTIR(Vertex 70)을
사용하여 분말 및 필름 상태의 시료를 ATR 법으로 600-4400 cm-1 범위에서 스캔 수 128회, 분해능 2 cm-1로 하여 FTIR 스펙트럼들을
얻었다. 얻어진 FTIR 스펙트럼들은 상대 비교를 위하여 측정 범위의 전체 면적을 1로 하는 표준화(normalization)를 시킨 것들로 변화시켜
분석에 사용하였다. Bruker 사(독일)의 NMR(Advance 400 NMR)을 사용하여 시료들을 DMSO-d6에
용해시키고 스캔 수 32로 하여 1H NMR 스펙트럼을 얻었으며, 시료를 10 g/L 농도로 증류수에 용해시킨 뒤 Scinco 사(일본)의 UV-Visible
spectrophotometer를 사용하여 파장 590 nm에서 용액의 빛 투과도를 측정하였다. CuKa X-선(파장 1.5 Å)을 사용하는 Bruker 사(독일)의 D2 Phaser
X-ray diffractometer를 사용하여 팽윤 평형에 도달시킨 후 동결건조시킨 수화젤을 0.0167°/s로 적도 방향으로 0.02° 크기로
스텝 스캔하여 광각X-선회절(WAXD) 곡선을 얻었다.
H-HEC의 합성 및 몰 치환도 분석. 본 연구에서 출발 물질로 사용한 HEC 자체가 셀룰로오스
유도체이며, 여기에 BGE를 반응시켜 얻은 H-HEC도 셀룰로오스 유도체이기 때문에 이들 치환도에 대한 용어를 먼저 정의하고자 한다. 먼저 셀룰로오스
유도체의 치환도는 단순 치환도(DS, degree of substitution)와 몰 치환도(MS, degree of molar
substitution)가 있다. 단순 치환도는 셀룰로오스의 AGU에 있는 3개의 히드록시기 중에서 몇 개의 히드록시기가 치환되었는지를 나타내는
것이다. 그러나 어떤 반응은 AGU에 있는 하나의 히드록시기와 반응하더라도 반응된 유도체에 존재하는 히드록시기에 다시 반응할 수 있으며, 이 경우에는
단순 치환도보다 많은 치환체가 존재하기 때문에 AGU에 치환된 전체 치환체의 개수를 나타내기 위해 단순 치환도 대신 몰 치환도를 사용한다. 본
연구에서는 HEC의 히드록시에틸기 치환도를 나타내기 위해서는 그냥 단순 치환도와 몰 치환도라는 용어를 그대로 사용하였고, BGE와 반응시켜 얻은
H-HEC에 있는 2-히드록시-3-부톡시프로필기의 단순 치환도와 몰 치환도는 “HBP 치환도” 및 “HBP 몰 치환도”라는 용어를 사용하여
HEC 치환도와 서로 구분하였다. 한편, 셀룰로오스 및 셀룰로오스 유도체에 어떤 약제를 반응시킬 때 사용하는 약제 농도는 일반적인 단순 % 농도나
몰 농도보다는 사용한 시료의 AGU 단위에 비해 몇 배의 비율로 사용하였는 가로 나타낸다. 이렇게 표기하는 것이 셀룰로오스에 있는 반응성기인 히드록시기
당량별 약제 비율을 알기 쉽기 때문이다. 이에 따라 본 연구에서도 반응시키는 약제의 농도는 AGU에 대한 비율(몰비)로 표기하였다.
본 연구에서
HEC의 히드록시기를 활성화시켜 주기 위해서 NaOH를 촉매로 사용하고, 여러 가지 HBP 치환도를 가지는 H-HEC를 얻기 위해 HEC에
BGE 농도를 달리하여 Scheme 1의 Williamson 에테르화 반응을1 통해 H-HEC를 합성하였다. 이때 사용한
HEC는 히드록시에틸기의 단순 치환도가 1.0이고 몰 치환도가 2.0인 것이기 때문에 AGU 당 2개의 기존 히드록시기가 잔존한다. 따라서 이
잔존 히드록시기 및 히드록시에틸기에 있는 히드록시기 모두에 BGE가 반응될 수 있다. 따라서 H-HEC에서 HBP 치환도를 분석할 때는 단순 치환도보다
몰 치환도를 사용하여야 한다.
한편, 예비실험 결과
BGE를 수계에서 반응시켰을 때보다 IPA 수용액을 반응매개체로 사용하여 반응시켰을 때 반응이 훨씬 잘 일어났다. 이는 BGE의 물에 대한 용해도가
20 oC에서
2%(w/v)로25 상당히 작아서 물을 반응매개체로 사용하면 반응이 잘 일어나지 않기 때문이다. BGE는 IPA에 잘 용해되지만
100% IPA를 반응매개체로 하여 셀룰로오스 또는 그 유도체와 반응시키면 불균일 반응이 되고 시료가 심하게 상해를 받기 쉽기 쉽다. 이에 따라
본 연구에서는 50% IPA 수용액을 반응매개체로 사용하였다. 또 계의 반응 온도를 80 oC보다 낮게 하였을 때는 BGE가 반응하는데 긴 시간이
필요하였으며, 80 oC보다 높은 온도에서 반응시키면 반응물이 분해되는 현상이
관찰되었기 때문에 반응온도를 80 oC로 설정하였다. 반응시키는 시간도 여러 예비실험을 거쳐
5시간으로 고정하였다.
H-HEC가 제대로
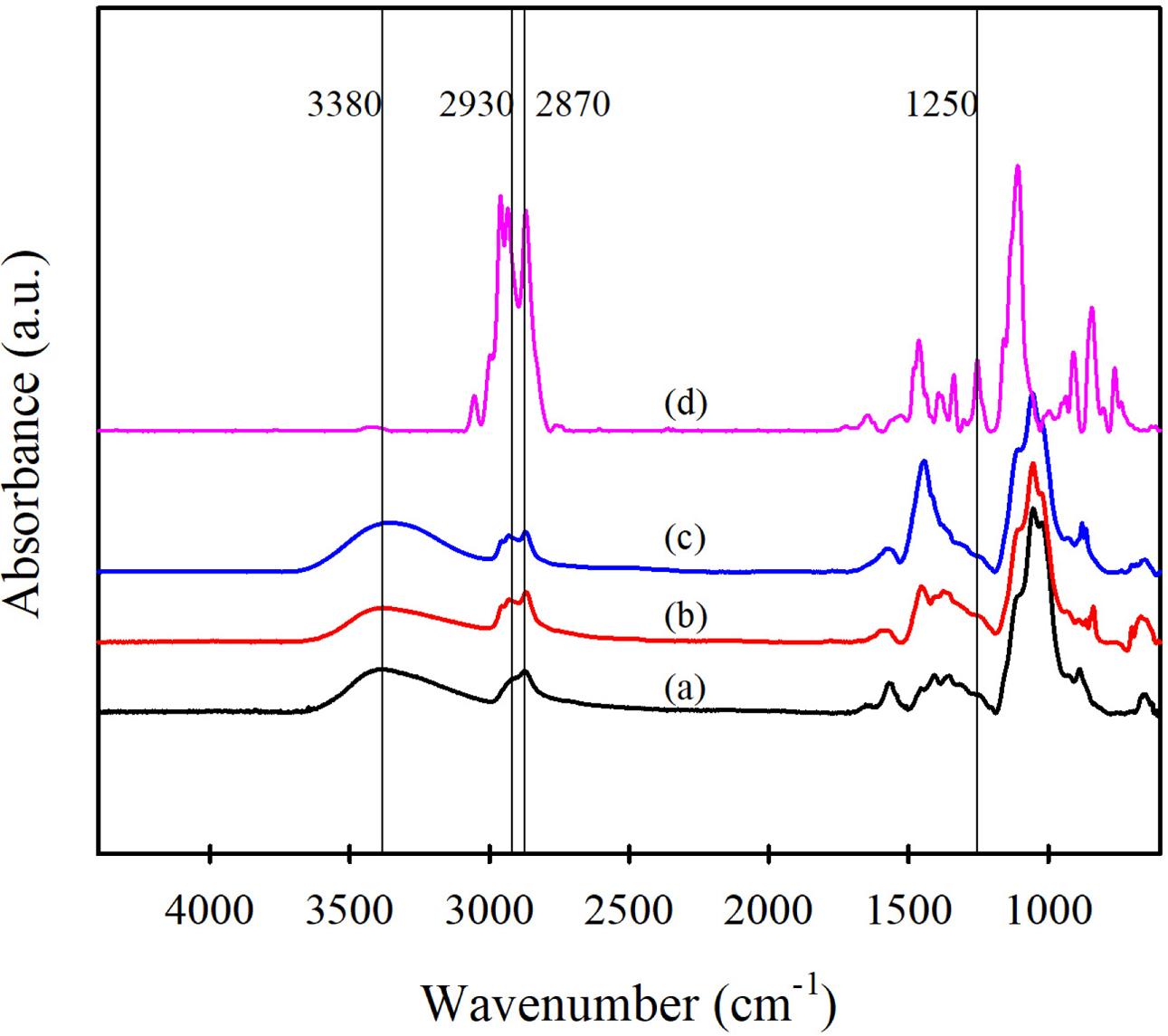
합성되었는지 확인하기 위하여 먼저 FTIR 분석을 진행하였다. Figure 1은 출발 물질인 HEC와 BGE, 몰 치환도가 각각 0.33,
0.58인 시료를 건조시켜 미세 분말로 만든 후 ATR 법으로 측정한 FTIR 스펙트럼이다. HEC의 스펙트럼을 보면, 3400~3350 cm-1에서 -OH기 신축진동,
2950~ 2850 cm-1에서 -CH 및 -CH2
신축운동, 1110 cm-1에서 -C-C 신축운동, 1055 cm-1에서 -C-O 신축 운동 밴드가
나타났으며, BGE 스펙트럼에서는
2800~3000 cm-1에서 C-H 밴드와 함께
1250 cm-1에서 에폭시 환에 의한 밴드가
나타났다. 한편, H-HEC의 FTIR 스펙트럼에서는 HEC를 주사슬로 하기 때문에 HEC 스펙트럼에 BGE 밴드가 더해져서 나타나고 있으며,
몰 치환도가 증가함에 따라 2950~2850 cm-1에서의 -CH 및 -CH2 신축 진동밴드와 1454 cm-1에서 -CH3
굽힘운동 밴드의 흡광도가 커지고 있으며, 1250 cm-1에서 BGE의 반응기인 에폭시 환에 해당하는 신축진동 밴드가 없어져 HEC에
BGE가 반응하였음을 알 수 있다.
합성된 H-HEC는
친수성인 히드록시기와 소수성인 부톡시프로필기가 함께 존재하여 열감응 특성을 나타내며 2-히드록시-3-부톡시프로필기의 몰 치환도(HBP 몰 치환도)에
의해 LCST가 변한다. 따라서 HBP 몰 치환도는 H-HEC의 특성을 나타내는 데 매우 중요한 요소이다. 본 연구에서는 HBP 몰 치환도가 x인
시료를 Hx-HEC라 명명하였다. 제조된 H-HEC 시료에서 반응이 얼마나 일어날 지는 HEC의 무게와 반응물의
몰비로부터 예측하여 계산할 수 있지만, 실제로는 시료 제조 시의 부반응, 침전 및 수세 과정에서의 손실 등이 있기 때문에 정확한 HBP 몰 치환도를
계산으로부터 구하기는 곤란하다.
FTIR 스펙트럼
분석으로는 정확한 H-HEC의 구조와 반응된 치환도를 알 수 없었기 때문에, 1H NMR 스펙트럼 분석을 통하여 HBP 몰 치환도를 구하였다.
1H NMR 스펙트럼 분석을 통하여 셀룰로오스 유도체의 몰 치환도를 구하는 방법은 여러 문헌에 제시되어 있으며20,26,27
H-HEC의 HBP 몰 치환도(MS)를 구하는 식은 다음과 같다.
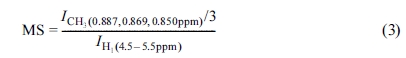
여기서, IH1은 AGU의 anomeric proton의 적분비를,
ICH3는
H-HEC의 부톡시프로필기에 존재하는 메틸기의 적분비를 의미한다.
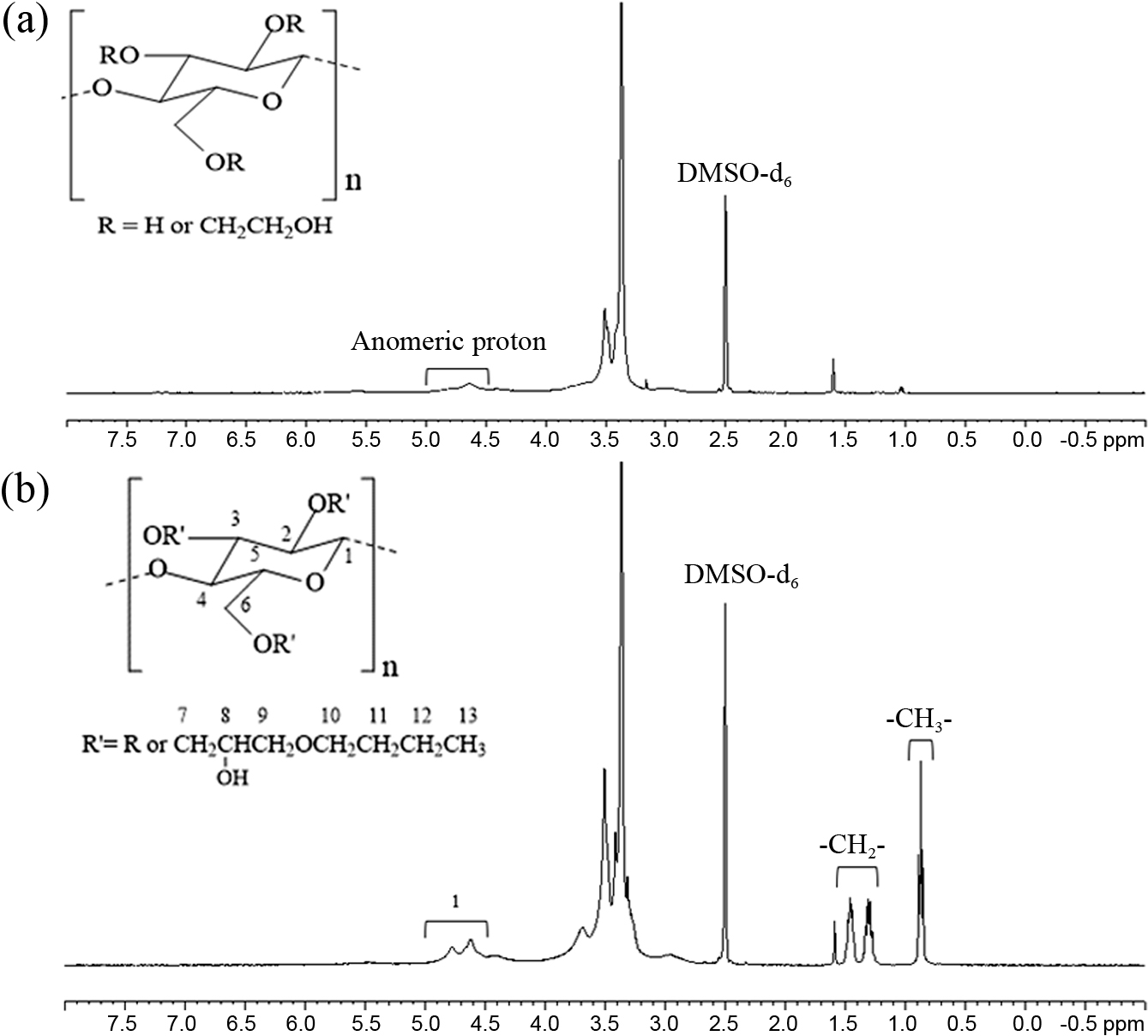
Figure 2는
HEC 및 H0.58-HEC의 1H NMR 스펙트럼을 나타낸 것이다. 이들 스펙트럼에서
4.5~5.5 ppm에서 나타나는 피크는 무수글루코스 단위(AGU)의
anomeric proton에 기인한다.20,26,27 한편, H0.58-HEC의 NMR 스펙트럼의 경우
0.887, 0.869, 0.850 ppm에서 부톡시프로필기의 -CH3, 1.476, 1.459, 1.441, 1.330,
1.311, 1.293, 1.275, 1.258 ppm에서 부톡시프로필기의 -CH2가 나타나고 있다.20,26,27
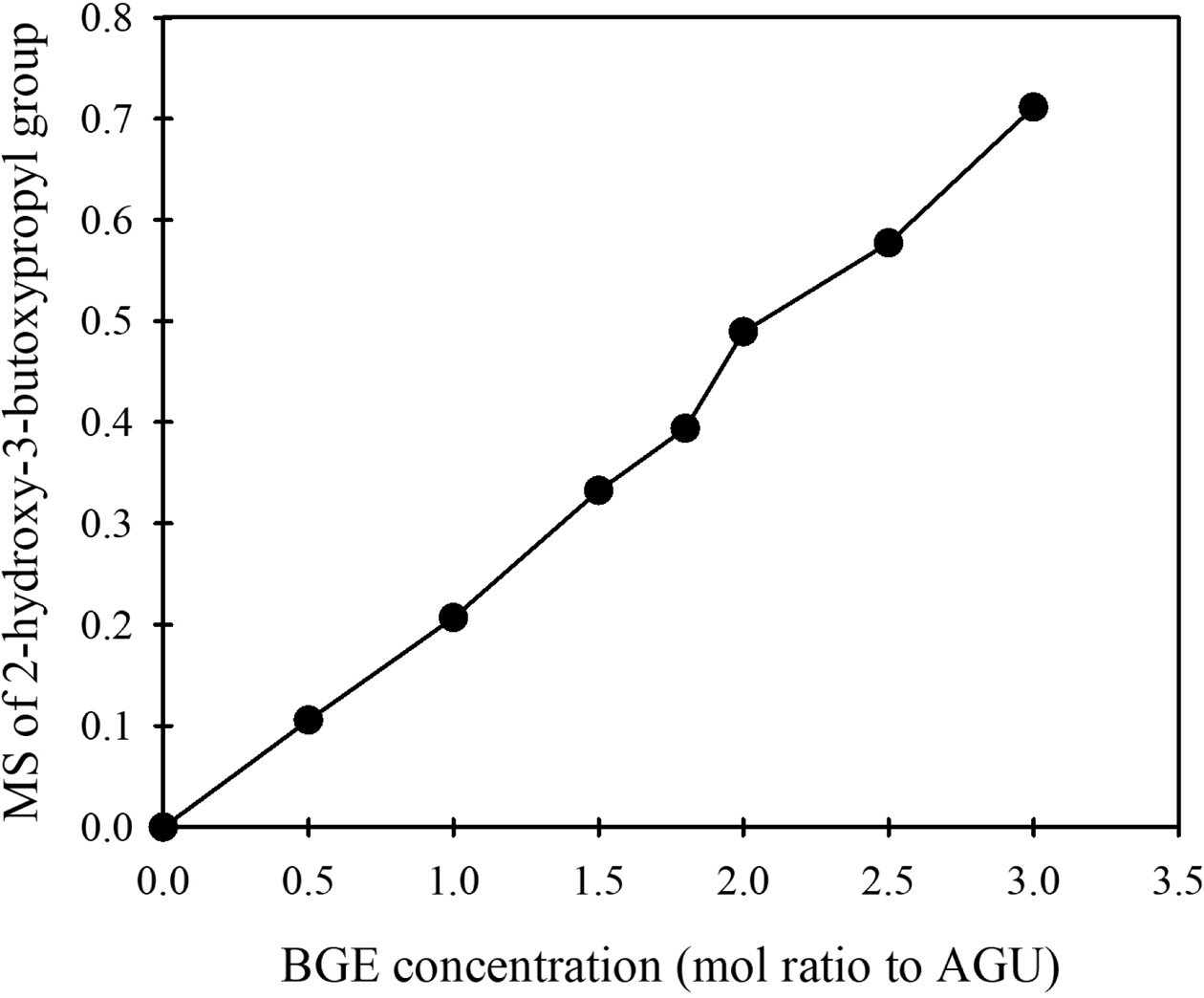
이를 통해서도 HEC에서 에테르화 반응이 성공적으로 진행되어 H-HEC가 합성되었다는 것을 알 수 있다. 여러 가지 BGE 농도로 반응시킨 H-HEC의 HBP
몰 치환도를 NMR 스펙트럼과 식 (3)으로부터 구하여 Figure 3에 나타내었다. 이를 보면 BGE 농도가 커짐에 따라서 HBP 몰 치환도가
거의 직선적으로 증가하는 경향을 나타내었다. BGE 농도를 3.0 몰비 AGU로 사용하였을 때 0.71 정도의 HBP 몰 치환도를 나타내, 대략
8%(0.71/3×3=0.079) 정도가 실제 반응되었음을 알 수 있다.
H-HEC의
HBP 몰 치환도가 커지면 소수성기가 많아지기 때문에 LCST가 낮아진다. LCST 온도 변화는 약물전달계와 같은 응용 분야에서 매우 중요한 요인으로
작용한다. 본 연구에서는 반응 시 알칼리 촉매의 양을 일정하게 하였기 때문에 BGE 농도가 더 증가하면 HBP 몰 치환도가 일정해지는 경향을 보일 것으로 예상되었지만,
AGU 당 BGE를 3 몰비까지 하여 얻은 H-HEC 수용액의 LCST가 상온보다 낮아졌기 때문에 더 큰 농도의 BGE로 반응시킨 시료는 제조하지
않았다.
H-HEC의 LCST 거동 분석. 열감응성 고분자의 경우 고분자 내에 존재하는 친수성기와
물 사이의 수소결합에 의해 물에 용해되게 되는데, 어느 온도 이상으로 되면 가해진 열 에너지에 의해 수소 결합이 파괴되어 침전됨으로써 LCST
거동을 나타낸다. 따라서 친수성 고분자에 적당한 양의 소수성기를 결합시켜 열감응성 고분자를 합성하면, 분자 내 및 분자간 수소결합의 방해로 인해 차가운 물에 대한
용해성이 향상되고 분자 내 친수성과 소수성의 균형을 조절하여 원하는 온도에서 LCST가 나타나도록 조절이 가능하다.
HBP 몰 치환도가
다른 H-HEC의 LCST 거동을 분석하기 위해, H-HEC 시료들을 증류수에 10 g/L 농도로 용해시킨 후 여러 온도에서 590 nm 파장에서의 빛 투과도를 측정하였다. H-HEC는
어떤 온도 이하에서는 친수성 부분인 HEC에 의해 물에 용해가 잘 되지만, 어떤 온도 이상에서는 소수성 부분인 부톡시프로필기에 의해 물과의 수소결합이
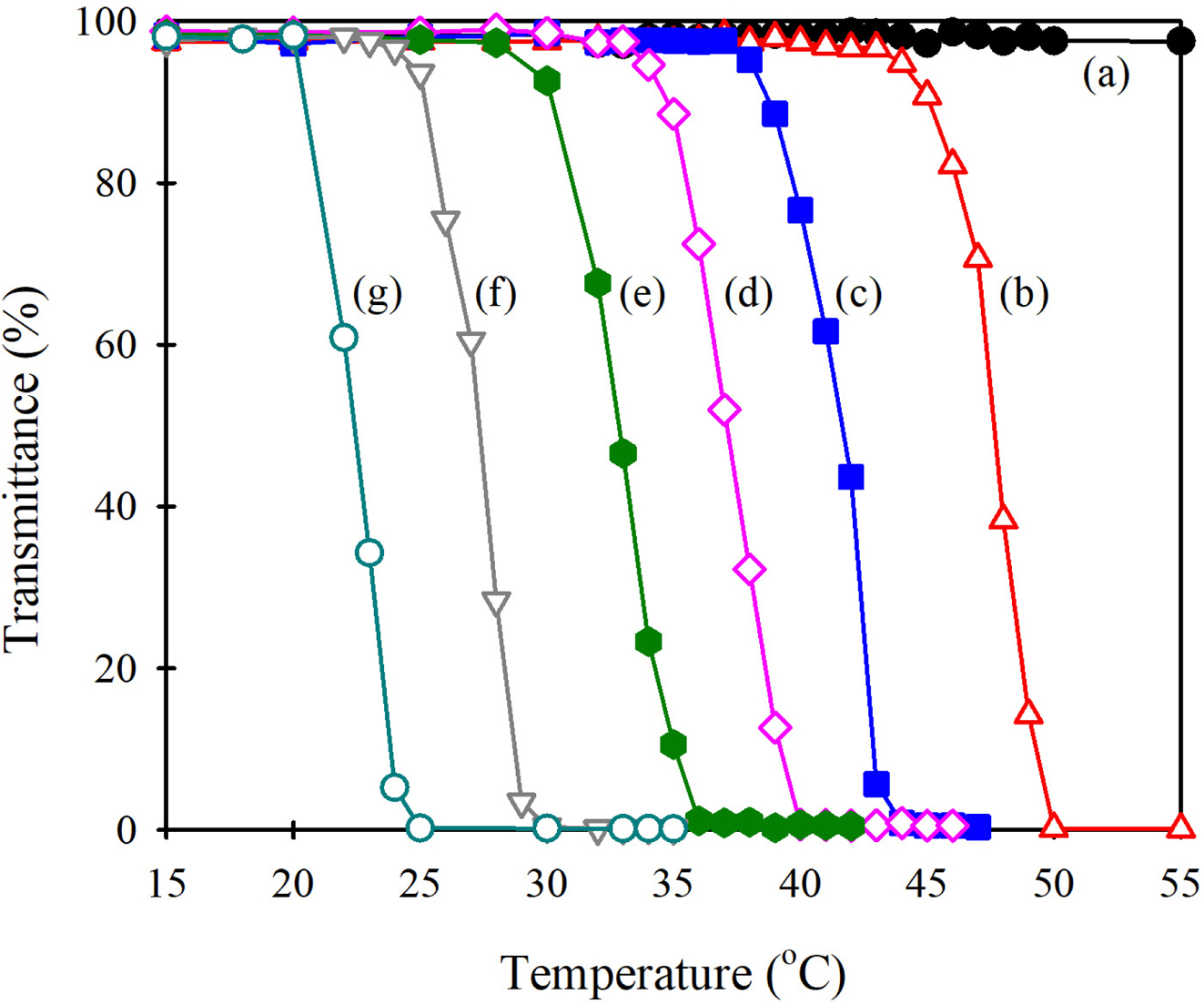
파괴되고 고분자간 상호작용이 강해져 물에 용해되지 않게 된다. Figure 4는 HBP 몰 치환도가 다른 H-HEC 수용액들의 온도에 따른 빛
투과도 변화를 나타낸 것이다. AGU 당 BGE를 0.5 몰비로 사용하여 얻은 (a) H0.11-HEC는 치환된 히드록시-부톡시프로필기가
매우 적기 때문에 친수성이 커서 50 oC 이상의 온도에서도 LCST 거동을 나타내지 않고 투명한 용액 상태를 유지하였다. AGU 당 BGE를
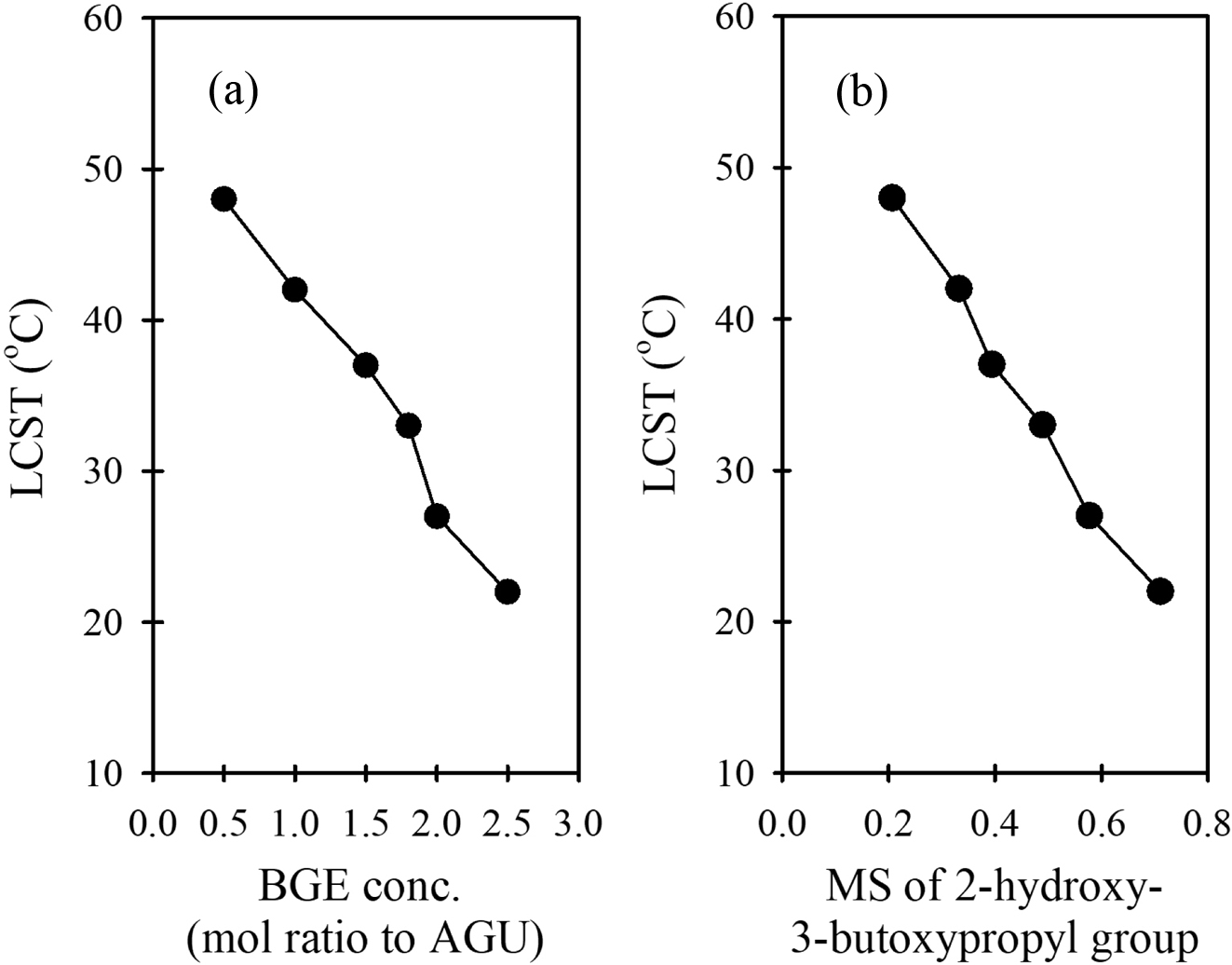
1 몰비 이상 사용했을 때부터, 낮은 온도에서는 100%에 가까운 투과도를 보이다가 특정 온도에서 투과도가 급격히 감소하는 LCST 거동을 나타내었다. Figure 5는 BGE 농도를 달리하여 합성한
H-HEC의 LCST 변화를 BGE 농도 및 HBP 몰 치환도에 대해서 나타낸 것이다. Figure 3에서 BGE 농도가 증가하면 HBP 몰 치환도가
거의 직선적으로 증가하였기 때문에, 이 두 그래프는 사실상 같은 경향을 나타내는 것이다. Figure 5를 보면, HBP 몰 치환도가 0.11에서
0.71까지 증가함에 따라 LCST가 48 oC에서 22 oC까지 직선적으로 감소하여 26 oC의 넓은 온도 범위에서 LCST가 변하였다. AGU 당 BGE 3 몰비를 사용한 H0.71-HEC는
상온 이하인 22 oC에서 LCST를 나타내었다. 이는 H-HEC의 몰 치환도가
커지면 소수성기가 많아져 상대적으로 낮은 온도에서 LCST가 나타나기 때문이다.
일반적으로
PNIPAAm과 같은 열감응성 고분자의 LCST를 조절하기 위해서는 다른 고분자를 공중합시키는데 이때의 LCST 온도 변화 범위는 상당히 좁게
나타난다.8,9 그러나 본 연구에서 합성한 H-HEC는 몰 치환도에 따라 22~48 oC의 거의 30 oC에 가까운 범위에서 LCST가 변하기 때문에 HBP
몰 치환도를 조절함에 따라 매우 넓은 범위에서 LCST를 조절할 수 있음을 알 수 있다. 한편, 이후의 분석 및 ECH로 가교시킨
CE-H-HEC 수화젤을 제조할 때에는 사람의 체온과 비슷한 37 oC의 LCST를 갖는 H0.39-HEC를 사용하였다. 이는 수화젤의 LCST를 이용하는
약물 전달계에서는 사람 체온과 비슷한 온도에서 팽윤-수축하는 것이 중요하기 때문이다.
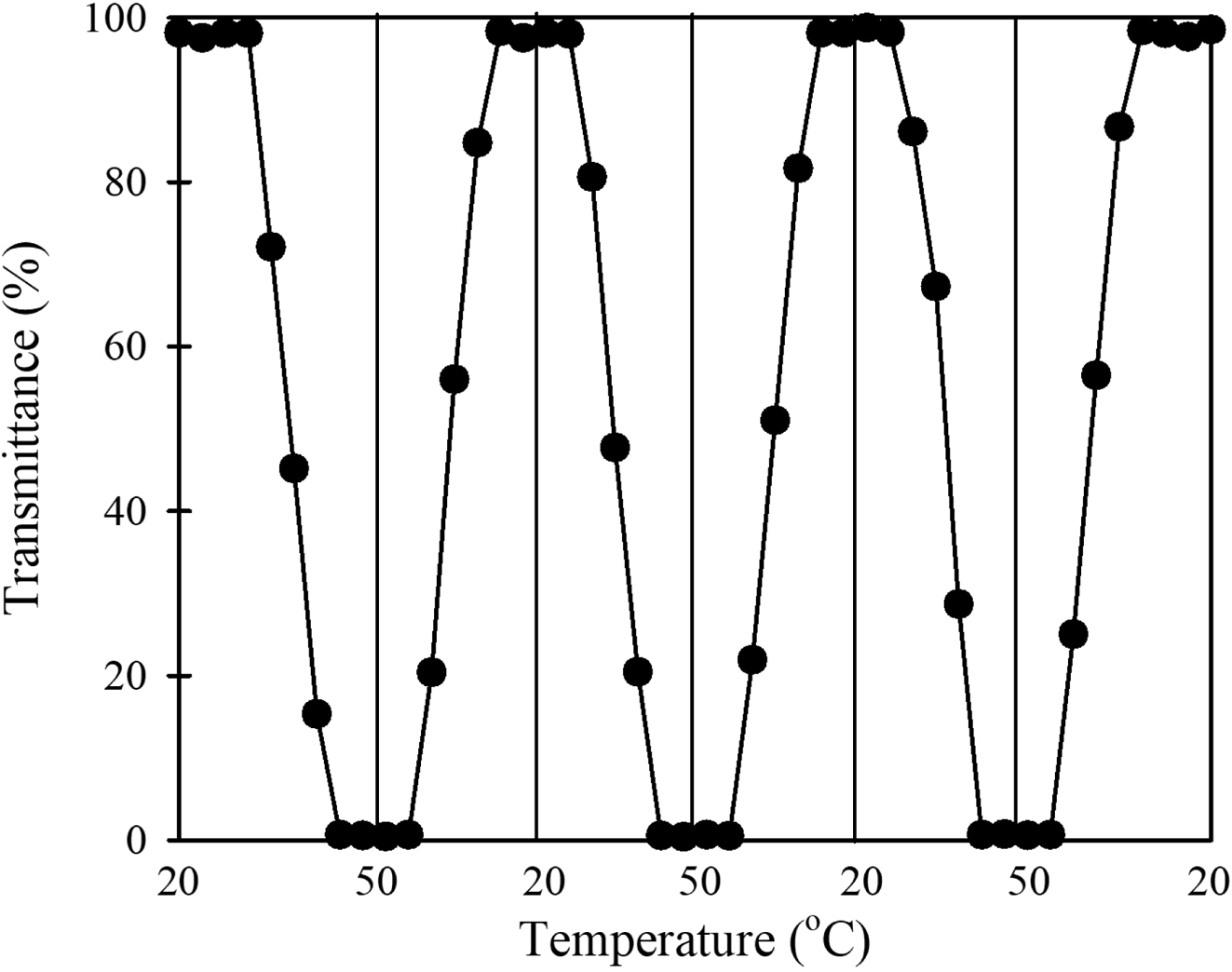
Figure 6은
H0.39-HEC 수용액(10 g/L)에 대해 승온과 강온을 반복했을 때의 상전이 곡선을 나타낸 것이다. 여러 번 되풀이 되는 강온-승온
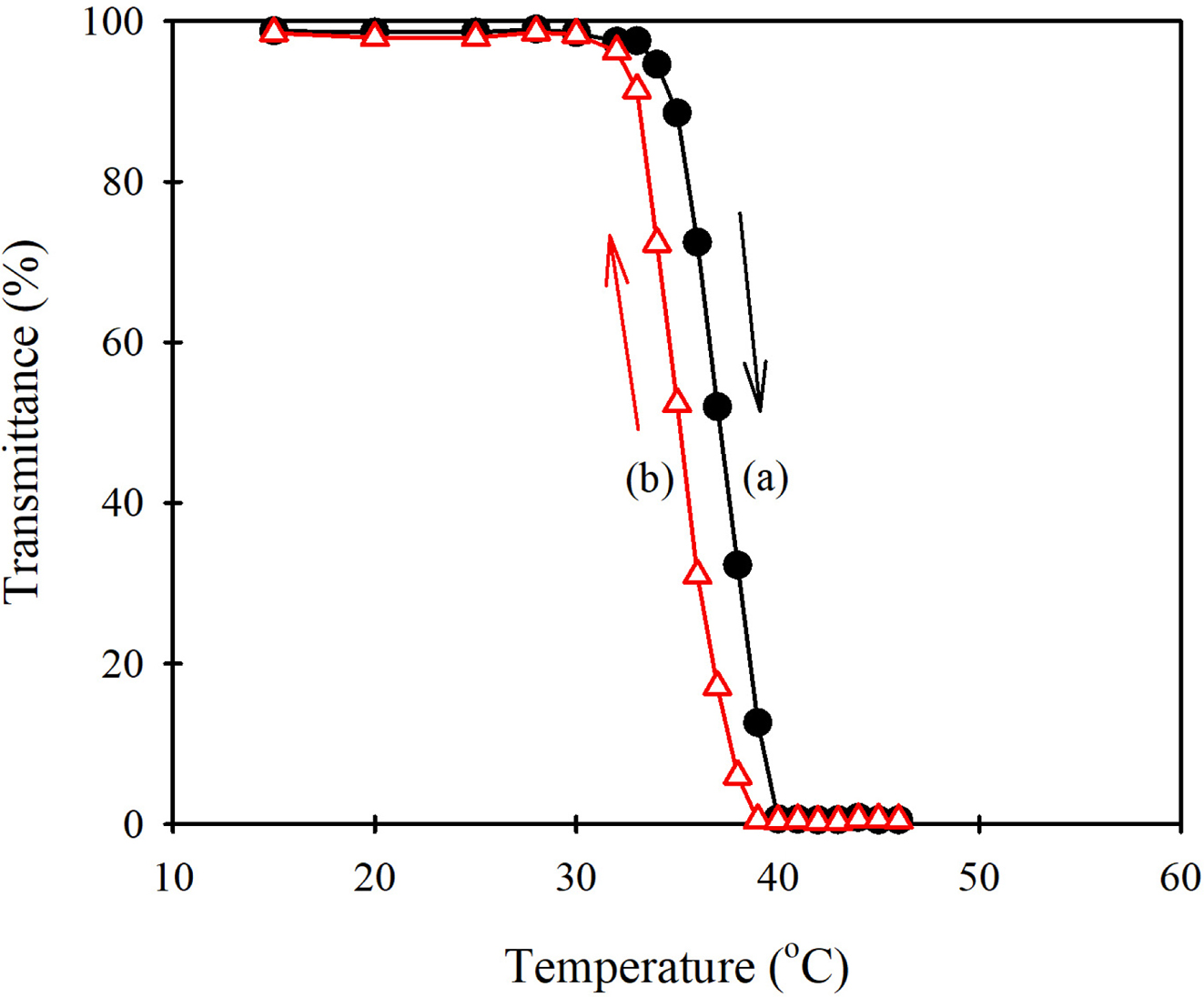
과정에서 H-HEC는 매우 민감하게 LCST 거동에 의한 상전이가 가역적으로 일어나는 것을 알 수 있다. 한편, H0.39-HEC 수용액(10 g/L)을 승온했을 때의 빛 투과도와 강온했을 때의 빛
투과도를 나타낸 Figure 7을 보면, 승온 과정에서의 LCST는 약 37 oC이었지만 강온 과정에서의 LCST는 약 35 oC인 히스테리시스 현상이 나타났다. 이는 LCST 이상에서
생성된 H0.39-HEC의 집합체(aggregate) 내에 분자내 및 분자간 수소결합이 존재하기 때문에, 강온 과정에서 집합체
내에 물 분자가 접근하는 것이 제한되어 물과 고분자 사이에 수소결합이 다시 형성되는데 시간이 걸리기 때문이다.24
CE-H-HEC
수화젤의 팽윤 거동과 기타 특성. 수화젤은 다공성 구조를 가지며 이 기공은 수분 및 용액을
보유할 수 있는 역할을 하기 때문에 기공의 크기 및 공극의 정도는 수화젤의 활용에 있어 매우 중요한 요소이다. 수화젤이 용액에 침지되면 가교된
고분자 사슬이 늘어나면서 팽윤되는데, 팽윤 정도는 가교제의 종류 및 가교밀도에 의해 영향을 받는다. 본 연구에서는 ECH를 가교제로 사용하였는데, ECH는 셀룰로오스나 전분의 가교제로 많이 사용된다. 특히
면섬유의 가교제로 사용되어 면섬유 제품의 구김방지 및 주름유지성을 갖는 DP(durable press)성을 부여한다. ECH에 의한 셀룰로오스
또는 전분의 가교결합은 알칼리 분위기 하에서 ECH가 반응할 때 에폭시기가 히드록시기와 반응하고, 이어서 말단의 염소기가 알칼리에 의해 다시 에폭시
환을 생성한 후 히드록시기와 반응하여 생성된다.1 따라서 ECH의 양 쪽이 모두 반응하면 가교결합이 생성되지만 한 쪽만 반응하는 경우에는 히드록시프로필기를 형성하여 친수성을
향상시키는데 기여한다.1
H-HEC와 ECH를
반응시켜 수화젤을 제조하면 ECH 농도와 처리 조건에 따라서 가교밀도가 달라지게 되고, 이는 수화젤의 팽윤성 및 팽윤-수축하는 상전이 온도에 영향을
미친다. 가교제 ECH 농도가 CE-H-HEC 수화젤의 특성에 미치는 영향을 알아보기 위해서, H0.39-HEC를 사용하면서
ECH 농도를 ECH/AGU = 0.25~2 몰비로 변화시켜 수화젤을 제조하였다. 이들
CE-H0.39-HEC 수화젤을 H0.39-HEC의 LCST보다 낮은 온도(25 oC) 및 LCST보다 높은 온도(50 oC)의 증류수에 팽윤시켜 측정한 팽윤비를 ECH 농도에
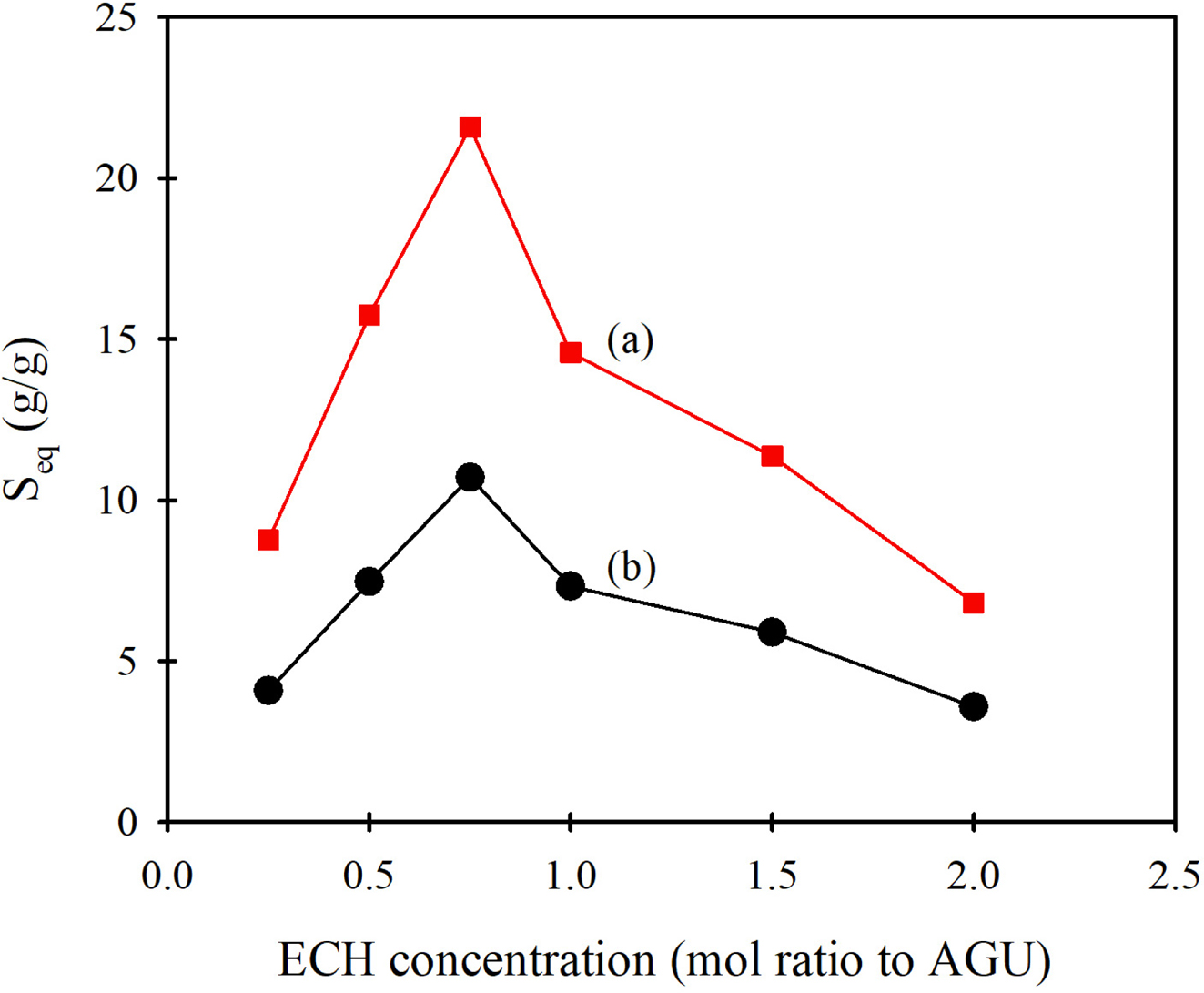
대해서 나타낸 것이 Figure 8이다. LCST 이하의 온도(Figure 8(a))에서는 전체적으로 ECH/AGU 몰비 농도 0.75까지는 팽윤비가
크게 증가하다가 그 이상의 ECH 농도에서는 감소하는 경향을 나타내었다. 이는 가교제 양이 너무 적으면 고분자들 사이에 가교가 거의 생성되지 않아
수용성 고분자인 H0.39-HEC가 물에 용해되지만, ECH 농도가 0.75 AGU 몰비가 될 때까지는 아직 가교제 양이 충분하지
않은 상태에서 가교제가 많아지기 때문에 점차 가교된 양이 많아져 물에 용해되는 양보다 팽윤되는 비율이 많아지기 때문이다. 즉, 가교되는 양이 많아짐에
따라 물에 녹는 고분자가 줄어들고 팽윤되는 비율이 증가한다. 그러나 ECH 농도가 1.0 AGU 몰비 이상으로 되면 가교된 양이 너무 많아지게
되고, 가교밀도 증가에 따라 미세공극의 팽윤이 제한되어 팽윤비가 감소하게 된다. CE-H0.39-HEC 수화젤의 경우 친수성기와
소수성기가 동시에 존재하지만 이온을 띠는 친수성기는 없기 때문에 조밀한 젤 구조가 형성되고 이는 사슬 사이의 반발력을 제한시켜 팽윤비가 22 이하로
작게 나타났다.
ECH 농도 변화에
따른 팽윤비 변화 거동은 LCST 이상에서의 팽윤비를 나타낸 Figure 8(b)에서도 동일하게 나타났다. LCST 이상의 온도에서 열감응성 수화젤은 수축된 상태를 나타내는데, Figure 8(b)를
보면 LCST 이하 온도에서의 팽윤비보다 매우 작은 값은 11 이하의 값들을 나타내 심하게 수축이 일어났음을 알 수 있다. 그러나
ECH/AGU 몰비 농도 0.75에서 가장 큰 팽윤비를 나타내고 그 이상의 농도에서 감소하는 것은 LCST 이하 온도에서와 동일하였다. 이러한
Figure 8의 결과들로 볼 때 H-HEC를 사용한 수화젤 제조 시 적절한 가교제 농도가 존재하며, ECH로 가교시킬 때는 ECH/AGU 0.75 몰비가 적당하다고
결론 내릴 수 있다.
온도에 따른 수화젤의
상전이 거동을 알아보기 위하여, ECH 농도를 0.75 AGU 몰비로 일정하게 하여 제조한 CE0.75-H0.39-HEC
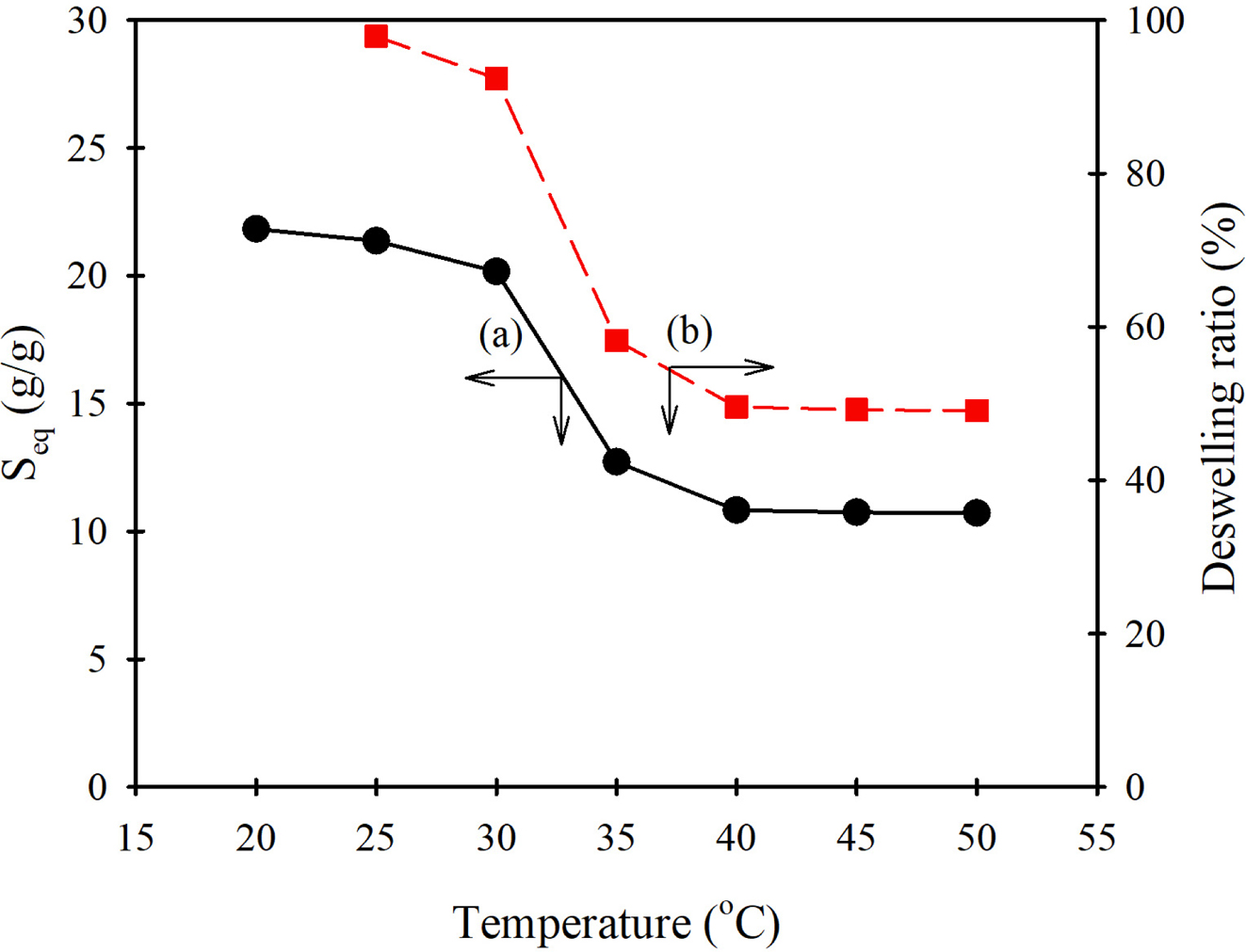
수화젤을 여러 온도의 증류수에서 팽윤비(Seq)를 측정하여 Figure 9(a)에 나타내었다. 물에 용해되었다가
침전되는 H-HEC의 LCST 만큼 뚜렷하지는 않지만, 수화젤에서도 30~35 °C에서 팽윤-수축되는 상전이 거동이 나타남을 볼 수
있다. Figure 9(b)는 상전이 온도 이하인 25 oC에서의 팽윤비를 100%로 하였을 때 각 온도의 증류수에서 팽윤비가 상대적으로 어떤 비율로 수축되었는 지를
나타낸 그래프이다. 30 °C 이하에서는 90% 이상의 수축률을 나타내었지만,
온도가 높아짐에 따라 수축되는 비율이 점차 줄어들어 40 °C 이상에서는 수축률이 35% 정도로 감소하였다.
CE-H-HEC 수화젤의
형태를 알아보기 위하여 FE-SEM을 사용하여 0.75 AGU 몰비 농도의 ECH로 가교시킨 CE0.75-H0.39-HEC
수화젤의 팽윤 상태(25 oC)와 수축 상태(50 oC)에서의 이미지를 얻어 Figure 10에 나타내었다.
이 때 수화젤들의 팽윤 및 수축 상태를 유지시키기 위해서 액체 질소로 급냉시키고 동결 건조시킨 시료들을 사용하였다. LCST 이하인 25 oC에서 팽윤시킨 수화젤의 단면을 보면 분리된 다공성 구조를
나타내고 있다. 다만, PVA나 PNIPAAm 수화젤에서 나타나는 격벽 형태의 core-shell 구조는 관찰하기 힘들었다. 이는
위에서 설명한 바와 같이 H-HEC로부터 제조된 수화젤들의 팽윤비가 일반 수화젤보다는 현격히 작기 때문이다. H0.39-HEC의
LCST 이상인 50 oC에서 수화젤을 수축시킨 시료의 FE-SEM 이미지에서는
팽윤 상태에 비해 기공 크기가 매우 작아지면서 분리된 기공 상태가 거의 없어졌음을 볼 수 있다. 그림에서 작은 틈새가 존재하는 것은 ECH로 가교된 수화젤이 완전히 수축되지 못하여 나타나는 현상이다.
즉, 가교되지 않은 고분자들은 LCST 이상에서 완전히 수축되는데 비하여, 가교된 수화젤들은 서로 연결되어 있기 때문에 어느 정도 이상으로 수축할
수 없기 때문이다.
한편,
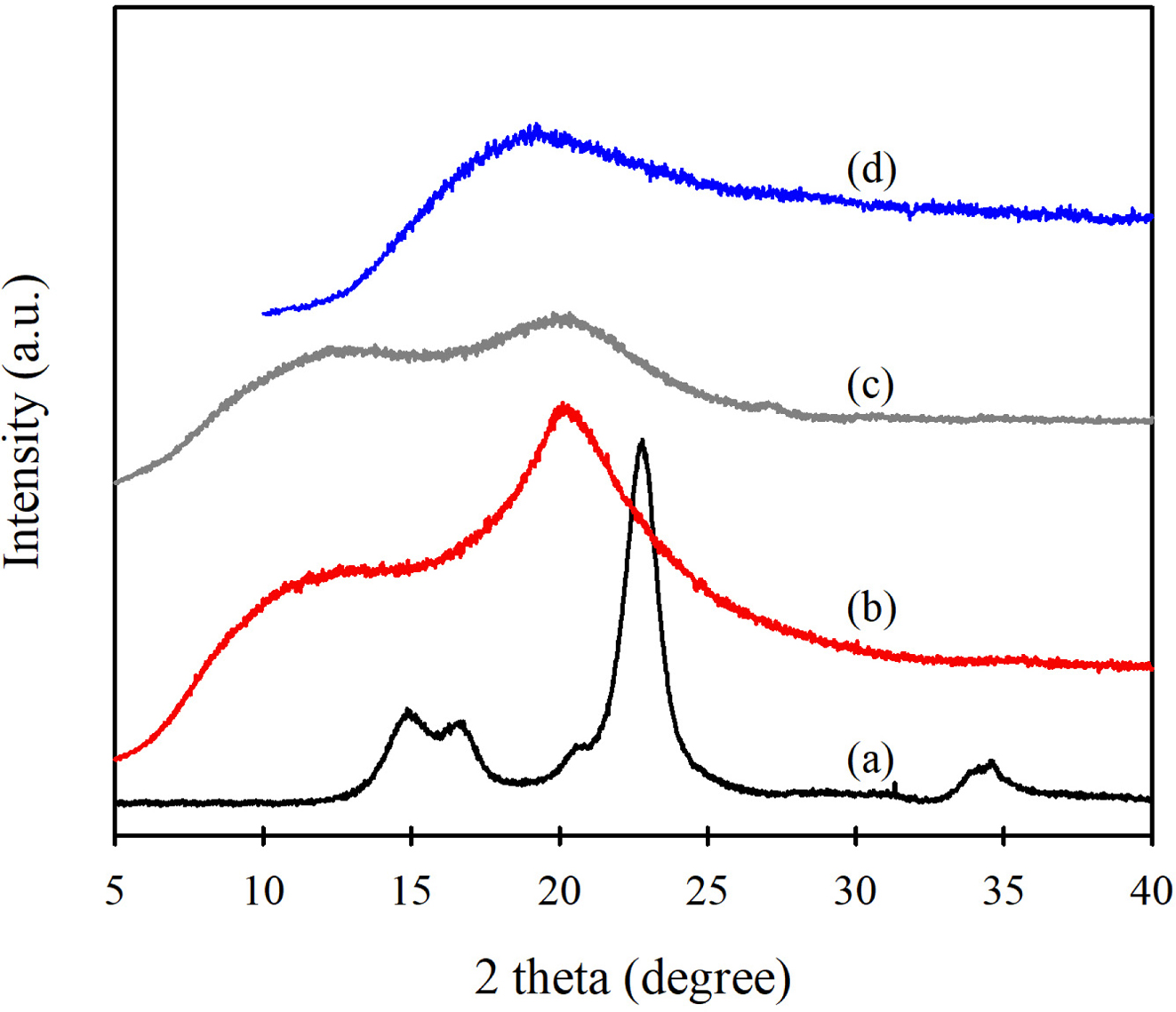
CE-H-HEC 수화젤이 결정구조를 유지하고 있는지 알아보기 위하여 여러 가지 시료들을 XRD로 분석하였다. Figure 11은 셀룰로오스
I, 출발 물질로 사용한 HEC, H0.39-HEC, 및 CE0.75-H0.39-HEC
수화젤의 WAXD 회절 곡선을 나타낸 것이다. 자연에서 얻어지는 셀룰로오스는 셀룰로오스 I의 결정구조를 나타내며, 이를 진한 NaOH와 같은 알칼리로
처리하거나 용매에 녹인 후 재생시키면 결정구조가 셀룰로오스 II로 변한다. 셀룰로오스 유도체의 경우 치환도(DS)가 작은 경우에는 치환되지 않은
셀룰로오스가 결정을 형성하며, 이 경우에는 유도체 합성 과정에서의 변화 때문에 대개 셀룰로오스 II의 결정구조를 나타낸다. 그러나 치환도가 커지면
결정구조를 이루지 못하며, 특히 HEC와 같이 치환체의 크기가 큰 경우에는 더욱 결정구조를 형성하기 곤란하다.
본 연구에서 사용한
HEC는 DS가 1.0이면서 MS가 2.0이었기 때문에 AGU 당 2개의 히드록시기가 미반응 상태로 남아 있으며, 많은 히드록시기들이 잔존하므로
셀룰로오스가 결정구조를 형성할 수 있다. Figure 11을 보면 HEC는 2q=20o 및 13o
부근에서 브로드하지만 셀룰로오스 II에 해당하는 회절 피크가28,29 나타나고 있어 결정구조를 유지하고 있음을 알 수 있다.
그러나 H0.39-HEC는 히드록시에틸기보다 훨씬 큰 치환체인 히드록시-부톡시프로필기가 도입되고 반응되는 히드록시기도 랜덤하기
때문에 불규칙성이 더 커져 결정을 형성하기 어려워진다. 그러나 H0.39-HEC의 HBP 몰 치환도가 0.39이기 때문에 단순
치환도는 이보다 작으며, 이들 치환이 AGU에 잔존하는 히드록시기 뿐만 아니라 H-HEC의 히드록시기 모두에서 일어날 수 있기 때문에 아직
AGU에 미반응 히드록시기가 상당히 남아 있어 셀룰로오스 II 결정구조를 유지하지만 그 양은 감소하여 HEC보다 회절 피크가 훨씬 더 브로드해
졌다. 이에 비하여 H0.39-HEC를 ECH로 가교시킨 CE0.75-H0.39-HEC는 2q=19o 부근에서 브로드한 무정형 halo만29 나타내고 있을 뿐 결정격자에 의한 회절 피크들이 전혀
없어 모두 무정형 구조인 것을 알 수 있다. ECH에 의해 H-HEC에 가교결합이 도입되고 이들이 랜덤하게 존재하기 때문에 CE0.75-H0.39-HEC는
결정구조를 형성하기 어렵게 되었기 때문이다. 이러한 무정형 구조는 결정 형성 시에 비해 수화젤 시료들이 수분을 더 많이 흡수할 수 있게 해줌으로써
수화젤의 팽윤비 증가에 기여한다.
|
Figure 1 FTIR spectra of (a) HEC; (b) H0.33-HEC; (c) H0.58-HEC; (d) BGE. |
|
Figure 2 1H NMR specta of (a) HEC; (b) H0.58-HEC. |
|
Figure 3 Increase in molar substitution (MS) of 2-hydroxy-3-butoxypropyl group in H-HEC with increasing BGE concentration. |
|
Figure 4 Changes in light transmittance of H-HEC aqueous solution at 590 nm with increasing solution temperature. MS of 2-hydroxy-3-butoxypropyl group: (a) 0.11; (b) 0.20; (c) 0.33; (d) 0.39; (e) 0.49; (f) 0.58; (g) 0.71. |
|
Figure 5 LCST change of H-HEC aqueous solution (a) with increasing BGE concentration; (b) with increasing MS of 2-hydroxy-3-butoxypropyl group. |
|
Figure 6 Reversible change in light transmittance of H0.39-HEC aqueous solution at 590 nm when the solution temperature is repeatedly increased and decreased. |
|
Figure 7 Hysteresis of light transmittance (at 590 nm) of an aqueous solution of H0.39-HEC between (a) increasing; (b) decreasing cycle of temperature. |
|
Figure 8 Changes in swelling ratio (Seq) of CE-H0.39-HEC hydrogel swollen in distilled water (a) below LCST (at 25 oC); (b) above LSCT (at 50 oC) with ECH concentration. |
|
Figure 9 Changes in swelling ratio (Seq) and deswelling ratio of CE0.75-H0.39-HEC hydrogel swollen in distilled water with solution temperature. |

|
Figure 10 FE-SEM images (×500) of freeze-dried CE0.75-H0.39-HEC hydrogel swollen (a) below LCST (at 25 oC); (b) above LSCT (at 50 oC). Scale bar=10 μm. |
|
Figure 11 WAXD profiles of (a) cellulose I; (b) HEC; (c) H0.39-HEC; (d) CE0.75-H0.39-HEC hydrogel. |
셀룰로오스 유도체인
히드록시에틸 셀룰로오스(HEC)에 부틸글리시딜에테르(BGE)를 반응시켜 열감응성 고분자인 2-히드록시-3-부톡시프로필 히드록시에틸 셀룰로오스(H-HEC)를
합성하여 특성들을 분석하고, H-HEC를 에피클로로히드린(ECH)으로 가교시킨 수화젤을 제조하고 그 특성들을 분석하여 다음과 같은 결론들을 얻었다.
HEC에 BGE를
반응시켜 친수성 셀룰로오스 유도체인 HEC로부터 열감응성 고분자인 H-HEC를 합성할 수 있으며, 반응시키는 BGE 농도를 변화시켜 여러 가지
HBP 몰 치환도(MS)를 갖는 H-HEC 및 넓은 온도 범위의 LCST를 나타내게 할 수 있다. BGE 농도가 커지면 H-HEC의 HBP 몰
치환도가 직선적으로 증가하며, 몰 치환도가 커지면 LCST는 거의 직선적으로 낮아진다.
ECH를 가교제로
사용하여 CH-H-HEC 수화젤을 제조할 수 있다. 이 수화젤은 가교제인 ECH의 농도에 따라 증류수 팽윤비가 달라지며, ECH 농도가
0.75 몰비 AGU일 때 최대팽윤비를 나타낸다.
H-HEC는 가역적인
LCST 거동을 하지만 승온과 강온에 따른 LCST의 히스테리시스를 나타내며, H-HEC는 약간의 결정구조를 유지하지만 ECH로 가교시킨 수화젤은
결정구조를 전혀 형성하지 못한다.
- 1. D. Klemm, B. Philipp, T. Heinzw, U. Heinze, and W. Wagenknecht, “Functionalization of Cellulose”, in Comprehensive Cellulose Chemistry, Wiley-VCH, N.Y., Vol 2, p 98 (1998).
-

- 2. V. K. Thakur, Editor, Cellulose-based Graft Copolymers: Structure and Chemistry, CRC Press, NY, p 337 (2015).
-

- 3. J. Zhou, Y. Qin, S. Liu, and L. Zhang, Macromol. Biosci., 6, 84 (2006).
-

- 4. W. Sun, D. Sun, Y. Wei, S. Liu, and S. Zhang, J. Colloid Interf. Sci., 311, 228 (2007).
-

- 5. S. P. Li, S. A. Martellucci, R. D. Bruce, A. C. Kinyon, M. B. Hay, and J. D. Higgins III, Drug Develop. Ind. Pharm., 28, 389 (2002).
-

- 6. S. C. Angadi, L. S. Manjeshwar, and T. M. Aminabhavi, Int. J. Biolog. Macromol., 47, 171 (2010).
-

- 7. A. Sannino, C. Demitri, and M. Madaghiele, Mater., 2, 353 (2009).
-

- 8. S. Kim, K. Lee, and C. Cha, J. Biomater. Sci., 27, 1698 (2016).
-

- 9. S. Ekici, J. Mater. Sci., 46, 2843 (2011).
-

- 10. M. Pandey, N. Nohamad, and M. C. I. M. Amin, Mol. Pharm., 11, 3596 (2014).
-

- 11. C. Gao, J. Ren, C. Zhao, W. Kong, Q. Dai, Q. Chen, C. Liu, and R. Sun, Carbohyd. Polym., 151, 189 (2016).
-

- 12. C. Chang, L. Zhang, J. Zhou, L. Zhang, and J. F. Kennedy, Carbohyd. Polym., 82, 122 (2010).
-

- 13. B. J. Kong, A. Kim, and S. N. Park, Carbohyd. Polym., 147, 473 (2016).
-

- 14. J. S. Boateng, K. H. Matthews, H. N. E. Stevens, and G. M. Eccleston, J. Pharm. Sci., 97, 2892 (2008).
-

- 15. S. Gorgieva and V. Kokol, Carbohyd. Polym., 85, 664 (2011).
-

- 16. N. Sun, T. Wang, and X. Yan, Carbohyd. Polym., 172, 49 (2017).
-

- 17. Z. Peng and F. Chen, Inter. J. Polym. Mater., 59, 450 (2010).
-

- 18. C. Chang, B. Duan, J. Cai, and L. Zhang, Eur. Polym. J., 46, 92 (2010).
-

- 19. R. L. G. Lecaros, Z. C. Syu, Y. H. Chiao, S. R. Wickramasinghe, Y. L. Ji, Q. F. An, W. S. Hung, C. C. Hu, K. R. Lee, and J. Y. Lai, Environ. Sci. Technol., 50, 11935 (2016).
-

- 20. Y. Tian, Y. Liu, B. Ju, X. Ren, and M. Dai, RSC Adv., 9, 22686 (2019).
-

- 21. A. Hanafia, C. Faur, A. Deratani, P. Guenoun, H. Garate, D. Quemener, C. P. Bohatier, and D. Bouyer, J. Membr. Sci., 526, 212 (2017).
-

- 22. B. Ju, D. Yan, and S. Zhang, Carbohyd. Polym., 87, 1404 (2012).
-

- 23. B. Ju, C. Zhang, and S. Zhang, Carbohyd. Polym., 108, 307 (2014).
-

- 24. B. Zheng, M. Karski, and S. D. Taylor, Carbohyd. Polym., 209, 145 (2019).
-

- 25. https://www.chemicalbook.com/ProductChemicalPropertiesCB 2728089_EN.htm.
- 26. Y. Tian, B. Ju, S. Zhang, X. Duan, and D. Dong, J. Biomater. Sci., 26, 1100 (2015).
-

- 27. Y. Tian, S. Zhang, and L. Hou, Carbohyd. Polym., 136, 1209 (2016).
-

- 28. S. Nam, A. D. French, B. D. Condon, and M. Concha, Carbohyd. Polym., 135, 1 (2016).
-

- 29. O. J. Rojas, Editor, Cellulose Chemistry and Properties: Fibers, Nanocelluloses and Advanced Materials, Springer, Switzerland, p 115 (2016).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(4): 495-504
Published online Jul 25, 2020
- 10.7317/pk.2020.44.4.495
- Received on Mar 5, 2020
- Revised on Mar 31, 2020
- Accepted on Mar 31, 2020
 Services
Services
Shared
 Correspondence to
Correspondence to
- Young Ho Kim
-
Department of Organic Materials and Fiber Engineering, Soongsil University, Seoul 06978, Korea
- E-mail: ssyhkim@ssu.ac.kr
- ORCID:
0000-0001-8889-3285










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.