- Preparation of Poly(ethylene glycol) Hydrogel Particles Containing Gold Nanoparticles by In Situ Polymerization
Department of Chemical Engineering, Hongik University, Wausanro 94, Mapo-gu, Seoul 04066, Korea
- 한 용기 내 중합반응에 의한 금 나노입자를 함유한 PEG 수화젤 입자의 합성
홍익대학교 화학공학과
As the first step to use an
organic/inorganic composite combining gold nanoparticles (AuNPs) and polymer
particles as a contrast agent for computed tomography (CT), PEG hydrogel
particles containing AuNPs, Au-PEG hydrogel particles, were prepared and the
synthetic conditions were established to improve the CT intensity of the Au-PEG
hydrogel particles. Au-PEG hydrogel particles that had the highest CT intensity
were obtained and the encapsulated AuNPs were not released from the hydrogel
particles when Au-PEG hydrogel particles were synthesized by in situ polymerization with which the
AuNPs were loaded in the PEG hydrogel particles during the polymerization. The
CT intensity of the Au-PEG hydrogel particles increased, as the concentration
of the loaded AuNPs and the 1st polymerization time of the polymerization
process increased. In addition, when the non-ionic surfactant was used as a
dispersion stabilizer, Au-PEG hydrogel particles showed good dispersibility and
the highest CT density.
금 입자와 고분자 입자를 결합한 유무기 복합재료를 컴퓨터단층촬영(CT)의 조영제로 사용하기 위한 첫 단계로, PEG 수화젤 입자 내부에
금 나노입자를 고농도로 탑재하여 최종적으로 합성된 Au-PEG 수화젤 입자의 CT세기를 향상시킬 수 있는 합성방법을 개발하였다. 다양한 방법을
이용하여 Au-PEG 수화젤 입자를 제조한 결과, PEG 수화젤 입자를 중합하는 동안 금 나노입자를 수화젤 내부에 탑재하는 한 용기내 중합(in situ 법)을 사용할 경우, 가장 높은 CT세기를 보이고 탑재된 금 입자가 수화젤로부터
방출되지 않는 안정적인 Au-PEG 수화젤 입자를 합성할 수 있었다.
In situ법을 사용하여 입자를 제조할 경우, 투입한 금 전구체의 농도가
증가할수록 그리고 중합과정에서 1차 중합시간이 증가할수록, 합성된 Au-PEG 수화젤 입자의 CT세기가 증가하였으며, 비이온성 계면활성제를 분산안정제로 사용할 경우, 가장 높은 CT세기를 가지는 입자를 제조할 수 있었다.
As the first step in an attempt to use an
organic/inorganic composite combining gold nanoparticles (AuNPs) and polymer particles as a
contrast agent for computed tomography (CT),
PEG hydrogel particles containing AuNPs were prepared and the synthetic
conditions were established to improve the CT intensity of the Au-PEG hydrogel
particles.
Keywords: polymer hydrogels, gold nanoparticles, organic/inorganic composites, in situ polymerization, computed tomography (CT) contrast agents
본 연구는 한국연구재단(NRF)의 이공분야 기
초연구사업(NRF-2019R1F1A1057048)과 홍익대학교 학술진
흥연구비에 의하여 지원되었으며, 이에 진심으로 감사드립니다.
복합재료(composite)는
두 종류 이상의 소재를 결합하여 원래의 각 소재보다 우수한 성능을 발휘하도록 제조한 재료를 말한다. 최근 들어 무기재료와 유기재료를 결합한 복합재료를
제조하여 광학, 촉매, 전자, 그리고 생의학 등의 분야에서 적용하는 연구가 활발히 진행되고 있는데,1-4 본 연구에서는 금
나노입자와 고분자 입자를 결합한 새로운 유무기 복합재료를 제조하여 영상의학 분야에서의 적용 가능성을 조사하여 보았다. 최근 의학 분야에서 영상의학의
발전은 인체를 직접 절개하지 않고 비침습적으로 다양한 병인을 진단하고 치료하는 것을 가능하게 하였다. 그 중에서 컴퓨터단층촬영(computed
tomography, CT)은 X선의 흡수도에 따라서 체내의 병변을 구별할 수 있는 영상을 제공할 수 있는 가장 널리 이용되는 임상 영상진단 방법으로, 사용이 간편하고, 촬영시간이 짧으며, 다른 어떤 영상검사보다 공간해상능이 우수하고, 3차원
부피 영상을 얻어 진단적 접근성이 매우 수월하다는 장점을 가지고 있다.5-8 이렇게 CT를 이용하는 영상진단에서는 반드시 조영제를
사용하여야 하는데, 현재 가장 널리 사용되고 있는 조영물질은 요오드이다. 그러나 요오드를 기반으로 하는 CT 촬영용 조영제는 체내 체류시간이 매우
짧아 진단에 어려움이 있으며, 신장 독성이 있어 신장관련 질환을 가진 환자에게는 사용이 제한되는 문제점을 가지고 있다.9-11
따라서 이러한 요오드 조영제의 단점을 극복하고 CT 촬영 시 주위조직과의 뚜렷한 대조도를 형성할 수 있는 새로운 조영제에 대한 연구가 필요하였고,
금(Au) 입자를 CT 조영제로서 활용하는 연구가 시도되고 있다. 금의 X선 흡수효율은 100 keV에서 5.16 cm2/g으로 뼈의 0.186 cm2/g, 연조직의 0.169 cm2/g, 그리고 현재 사용되고
있는 조영제인 요오드의 1.94 cm2/g보다 훨씬 높아서 금 입자를
조영제로 사용할 경우, 뼈와 연조직으로 인한 조영효과의 간섭을 방지하고, 환자에게 피폭되는 방사선량을 감소시키면서 선명한 영상을 얻을 수 있다.12
하지만, 금은 고가의 물질이기 때문에 경제적인 측면에서 그 사용량에 제한이 있을 수 밖에 없다. 따라서 금 입자에 의한 CT의 조영효과를
극대화하기 위해서는 적은 양의 금 입자를 고농도로 집적해서 사용할 수 있는 방법의 개발이 필요하다.
본 연구에서는
CT 조영제로서 금 나노입자를 활용하기 위한 시도의 첫 단계로, 금 나노입자를 PEG 수화젤에 고농도로 탑재시킨 유무기 복합재료를 제조하는 방법을
개발하고자 한다. 고분자 수화젤은 친수성의 네트워크 구조를 갖는 가교고분자로, 수화젤이 갖고 있는 높은 수분함량과 우수한 생체적합성 때문에 의학
및 제약 분야에서 예전부터 널리 활용되어지고 있다.13-15 그리고 PEG는 생체적합성이 우수하다고 널리 알려진 고분자 물질로,
이러한 PEG를 나노 및 마이크로 크기의 수화젤 입자로 합성할 경우, 작은 크기, 큰 비표면적, 높은 확산성 및 이동성, 그리고 우수한 캡슐화
효율 등의 특징으로 인해 PEG 수화젤 입자를 약물 전달시스템에 활용하는 연구가 활발히 수행되고 있다.16-19 따라서 본
연구에서는 고농도의 금 나노입자를 안정적으로 함유하는 고분자 수화젤인 Au-PEG 수화젤 입자를 다양한 방법을 시도하여 제조해 보고, 합성조건이
수화젤 입자에 대한 금 나노입자의 탑재에 미치는 영향을 조사하여 최고의 탑재효율을 보이며 동시에 안정적인 Au-PEG 수화젤 입자를 합성할 수
있는 조건을 확립하고자 하였다.
재료. 실험에 사용된 poly(ethylene glycol)
dimethacrylate (PEGDMA, MW 330), gold(III) chloride trihydrate(HAuCl4· 3H2O), trisodium
citrate dihydrate, 4-(1,1,3,3-tetramethylbutyl) phenyl-polyethylene
glycol(Triton X-100), cetyltrimethyl-ammonium bromide(CTAB), 그리고
poly(ethylene glycol) 4-nonylphenyl 3-sulfopropyl ether potassium salt는 Sigma–Aldrich
Chemical Co.로부터, 1-hydroxy cyclohexyl phenyl ketone(Irgacure 184)은 Ciba
Specialty Chemicals로부터 각각 구입하여 사용하였다.
금 나노입자(AuNPs)의 합성. 금 나노입자를 합성하기 위하여, 농도가 2 mg/mL인 gold(III) chloride trihydrate(HAuCl4· 3H2O) 수용액 194 mL을 가열하면서 교반하고, 100 oC에 도달하면 환원제인 trisodium citrate dihydrate 수용액(100 mg/mL) 6 mL를 주입하였다. 환원제를 투입하면 수용액의 색깔이
노란색에서 자주색으로 변하고 이 때 온도를 90 oC로 10분간 유지한 후, 상온에서 식혀 금 나노입자 분산액을 제조하였다.
PEG 수화젤 입자의 합성. PEG 수화젤 입자는 이전에 보고된 방법인 현탁중합을
이용하여 합성하였다.20 간단히 설명하면, 단량체인 PEGDMA 대비 광개시제인 Irgacure 184 그리고 분산안정제인
CTAB를 각각 7.5 wt%씩 투입한 후, 단량체와 분산매의 질량 대비 부피가
1:20이 되도록 분산매인 증류수를 첨가하였다. 이 혼합물을 초음파기기(VCX750, Sonics & Materials)로 90초 동안
교반하여서 현탁용액을 제조하고 세기가 1000 mW/cm2인 UV를 600초 동안 조사하여 중합반응을 수행하였다. 합성된 입자들은 여러
번의 원심분리 및 세척과정을 거친 후 용액으로부터 분리하였다.
Au-PEG
수화젤 입자의 합성. 본 연구에서는 금 나노입자가 탑재된 Au-PEG 수화젤
입자를 제조하기 위하여 ex situ법과 in situ법을 수행하였다. Ex situ법은 이미 제조된 금
나노입자 분산액에 미리 합성한 PEG 수화제 입자를 담지하여 금 나노입자를 PEG 수화젤 입자에 탑재하고 24시간이 경과한 후 원심분리를 이용하여
Au-PEG 수화젤 입자를 회수하는 방법이고, in situ법은 PEG 수화젤을 합성하는 과정에 금 전구체와 환원제를 투입하여 최종적으로
금 나노입자가 함유된 수화젤 입자를 얻는 방법이다. 자세히 설명하면, PEG 수화젤 입자를 합성하는 것과 동일한 방법으로 단량체인
PEGDMA, 개시제인 Irgacure 184 그리고 분산안정제를 분산매인 증류수에 분산시켜 제조한 현탁용액에 UV를 조사하여 1차 중합을 수행하고
초음파 처리를 하였다. 초음파 처리를 한 1차 중합물에 25 mg/mL의 금 전구체인 gold(III) chloride trihydrate(HAuCl4·3H2O)
0.5 g을 첨가하여 상온에서 교반하고, 24 시간이 경과하면
첨가된 금 전구체와 환원제의 질량비가 2:3이 되도록 환원제인 trisodium citrate dihydrate 수용액을 투입한 후, 다시
UV를 조사하여 2차 중합을 실시하였다. Scheme 1에 in situ법을 이용하여 Au-PEG 수화젤 입자를 합성하는 방법을 나타냈다.
합성된 입자용액은 원심분리 및 세척과정을 여러 번 실시하여 최종적으로 Au-PEG 수화젤 입자를 회수하였다. 합성된 Au-PEG 수화젤 입자의 크기와
모양은 dynamic light scattering(DLS, Nano-S90, Malvern)과 field emission transmission
electron microscopy(FE-TEM, Tecnai G2 F30 Series, FEI)을 사용하여 분석하였다. 수화젤 입자에 탑재된 금 나노입자의
농도는 마이크로 CT(NFR-Polaris-G90, Nano Focus Ray)를 이용하여 각 샘플들의 CT세기를 측정하여 분석하였다. 이
CT는 원추빔형의 평판형 X선 영상센서를 기반으로 하는 볼륨 CT로서 X선 발생장치의 관전압 및 관전류는 각각 40-130 kVp, 그리고 65 μA이었다. 일회 조사에 소요되는 시간은 1초로 총 조사시간은
6분이 소요되었다.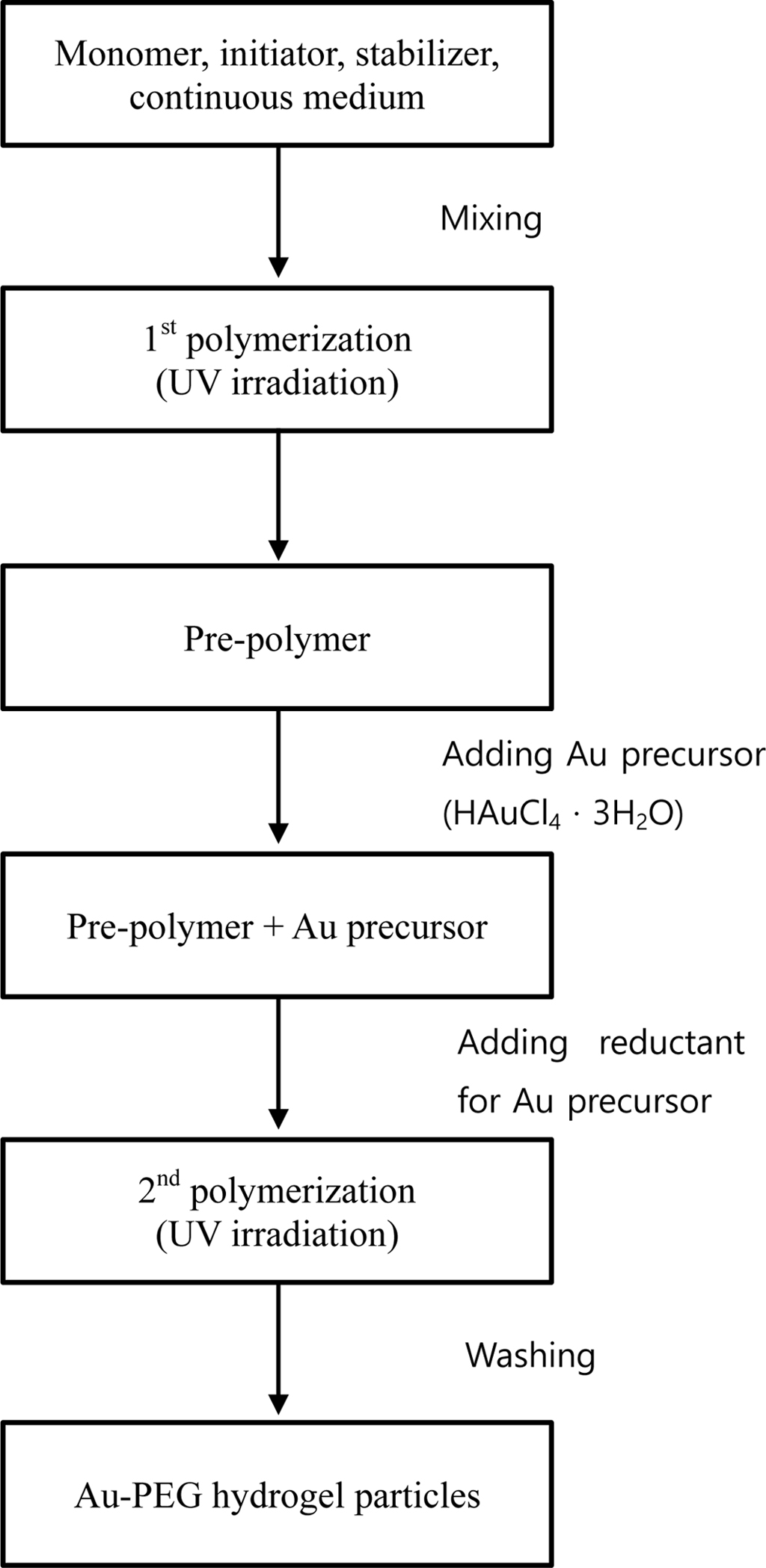
Scheme 1. In situ polymerization to synthesize Au-PEG hydrogel
particles.
본 연구에서는
PEG 수화젤 입자의 내부에 금 나노입자를 탑재하고, 탑재되는 금 나노입자의 농도를 가능한 높여서 최종적으로 Au-PEG 수화젤 입자의 CT세기를
향상시키고자 하였다. 따라서 우선적으로 금 나노입자를 PEG 수화젤 입자에 탑재시키는 방법의 개발이 필요한데, 이러한 Au-PEG 수화젤 입자를
제조하는 방법으로 ex situ법과 in situ법을 수행하여서 비교하였 보았다. Ex situ법은
PEG 수화젤 입자와 금 나노입자를 각각 제조한 후, 고농도의 금 나노입자 분산액에 PEG 수화젤 입자를 장시간 동안 담지하여 금 나노입자를 수화젤 내부에 탑재하는 방법이고,
in situ법은 PEG 수화젤 입자를 중합하는 과정에 금 전구체와 환원제를 투입하여 금 나노입자를 제조하여 금 입자를 수화젤 내부에
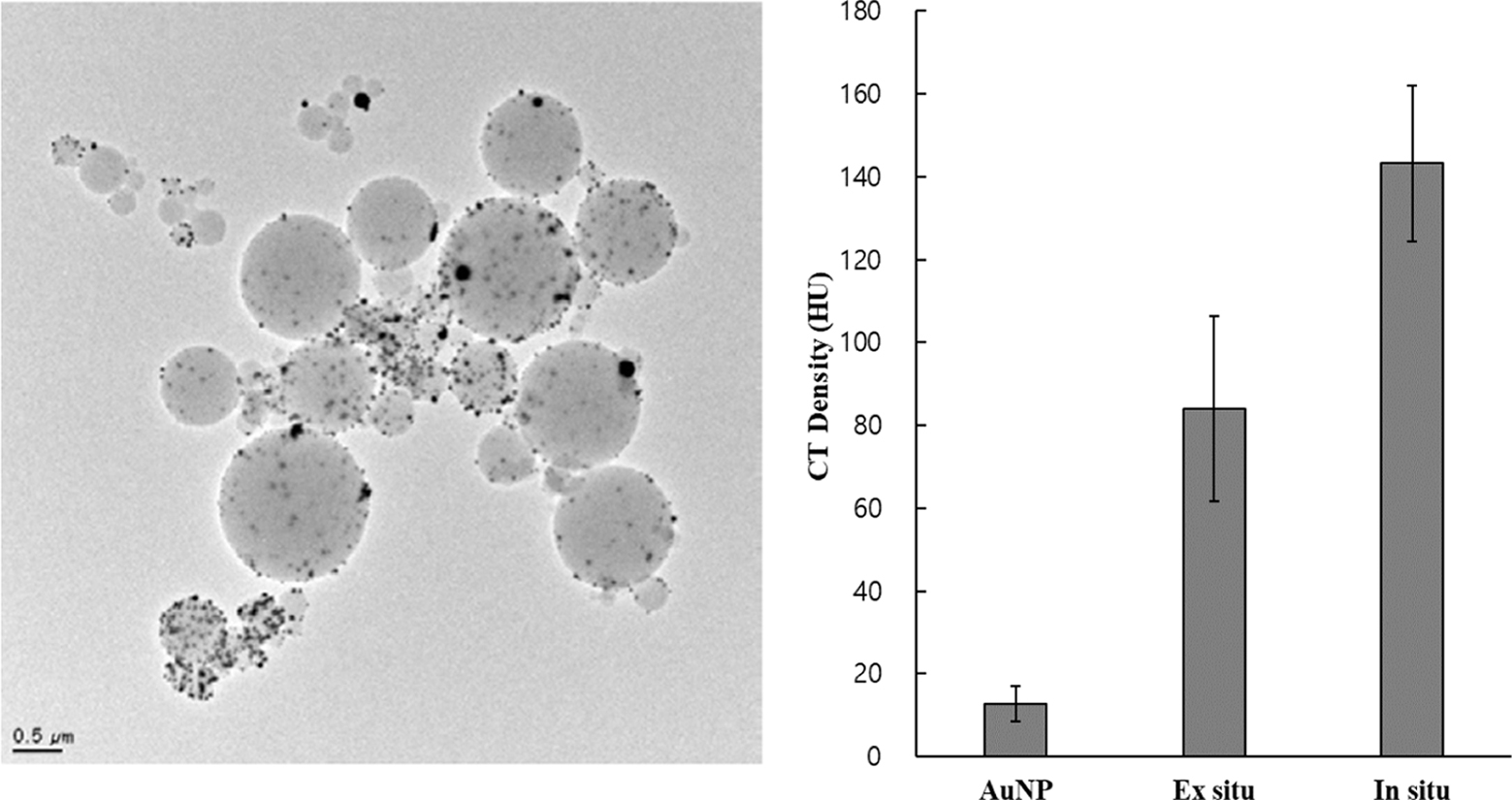
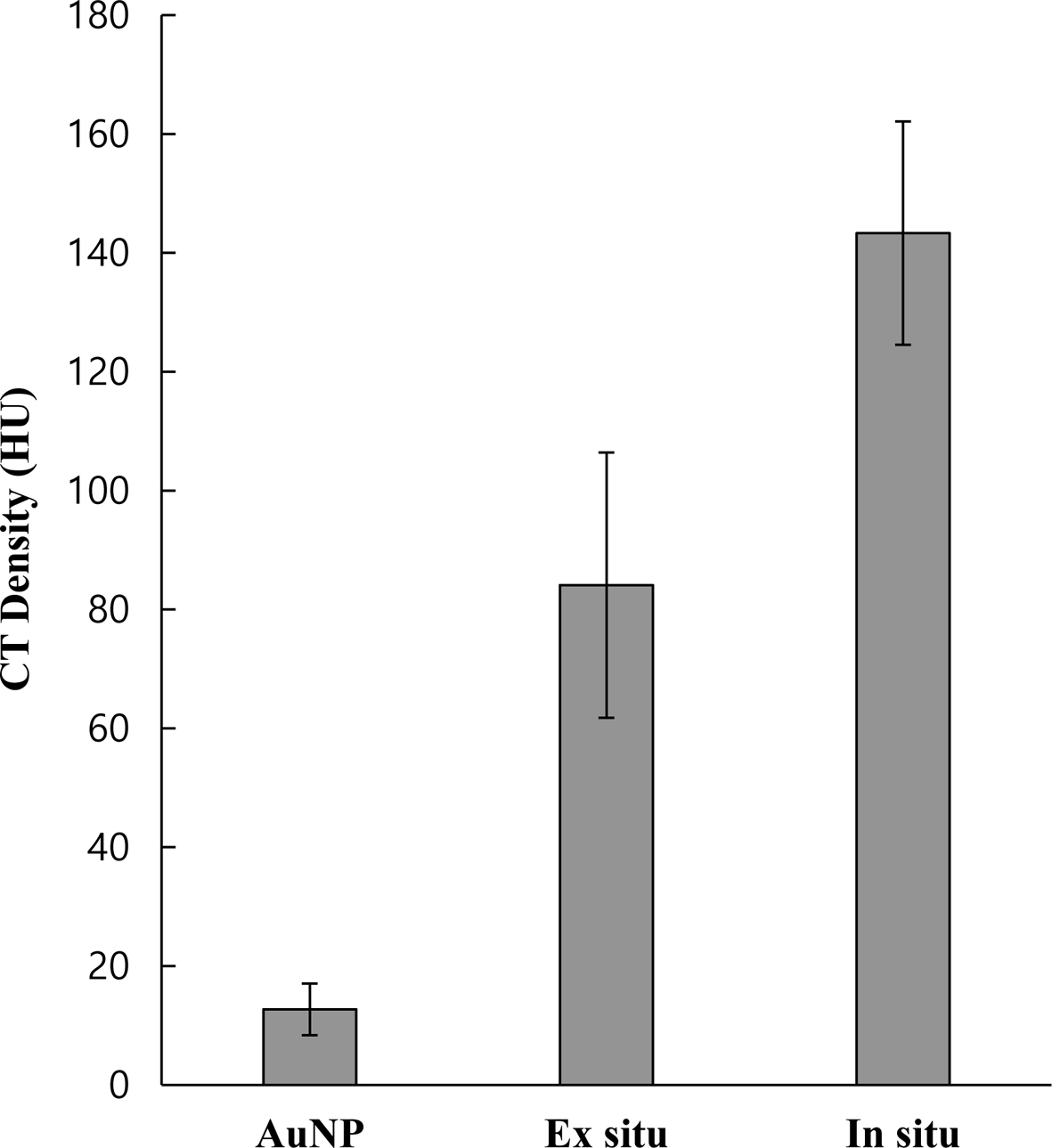
탑재시키는 방법이다. Figure 1에서는 수화젤에 탑재하지 않은 순수 금 나노입자(AuNP), 그리고 ex situ법과 in
situ법으로 각각 합성한 Au-PEG 수화젤 입자의 CT세기를 보여준다. 모두 동일한 양의 금 전구체를 사용하여 제작하였다.
Figure 1에서 보는 바와 같이, 금 입자가 수화젤 입자에 탑재되는 경우, CT세기가 증가하는 것을 볼 수 있었다. 그 이유는 금 나노입자가
수화젤 입자에 탑재되면, 수화젤 없이 분산액에 분산되어 있을 때보다는 금 입자가 존재할 수 있는 공간이 한정되게 되므로, 상대적으로 일정 공간 내에서의 금 입자 농도가 증가하게 되기 때문으로 설명할
수 있다. 그리고 ex situ법과 in situ법을 비교하여 보면 ex situ법으로 만든 Au-PEG
수화젤 입자의 CT세기는
84.1 HU, 그리고 in situ법으로 만든 Au-PEG 수화젤 입자의 CT세기는 143.3 HU로, in situ법으로 만든
Au-PEG 수화젤 입자의 CT세기가 더 높은 것을 알 수 있었다. 따라서 in situ법으로 합성한 Au-PEG 수화젤 입자를
CT 조영제로 사용할 경우, 훨씬 큰 조영효과를 얻을 수 있고 이것은 고가인 금을 사용하는데 있어서 경제성 측면에서도 매우 유리하다고 이야기할
수 있다. 따라서 향후 실험은 in situ법을 이용하여 Au-PEG 수화젤 입자를 합성하는데 있어서, 고농도의 금 나노입자를
PEG 수화젤 입자 내부에 탑재하는 방법에 관한 것을 수행하였다. Figure 2는 in situ법으로 합성한 필름형태의
Au-PEG 수화젤과 TEM으로 관찰한 입자형태의 Au-PEG 수화젤의 사진이다. Au-PEG 수화젤 필름의 사진은 in situ법으로
금 나노입자가 PEG 수화젤에 탑재된 것을 시각적으로 보여주기 위한 목적으로 촬영한 것으로 금 나노입자가 수화젤 내부에 존재하기 때문에 최종적인
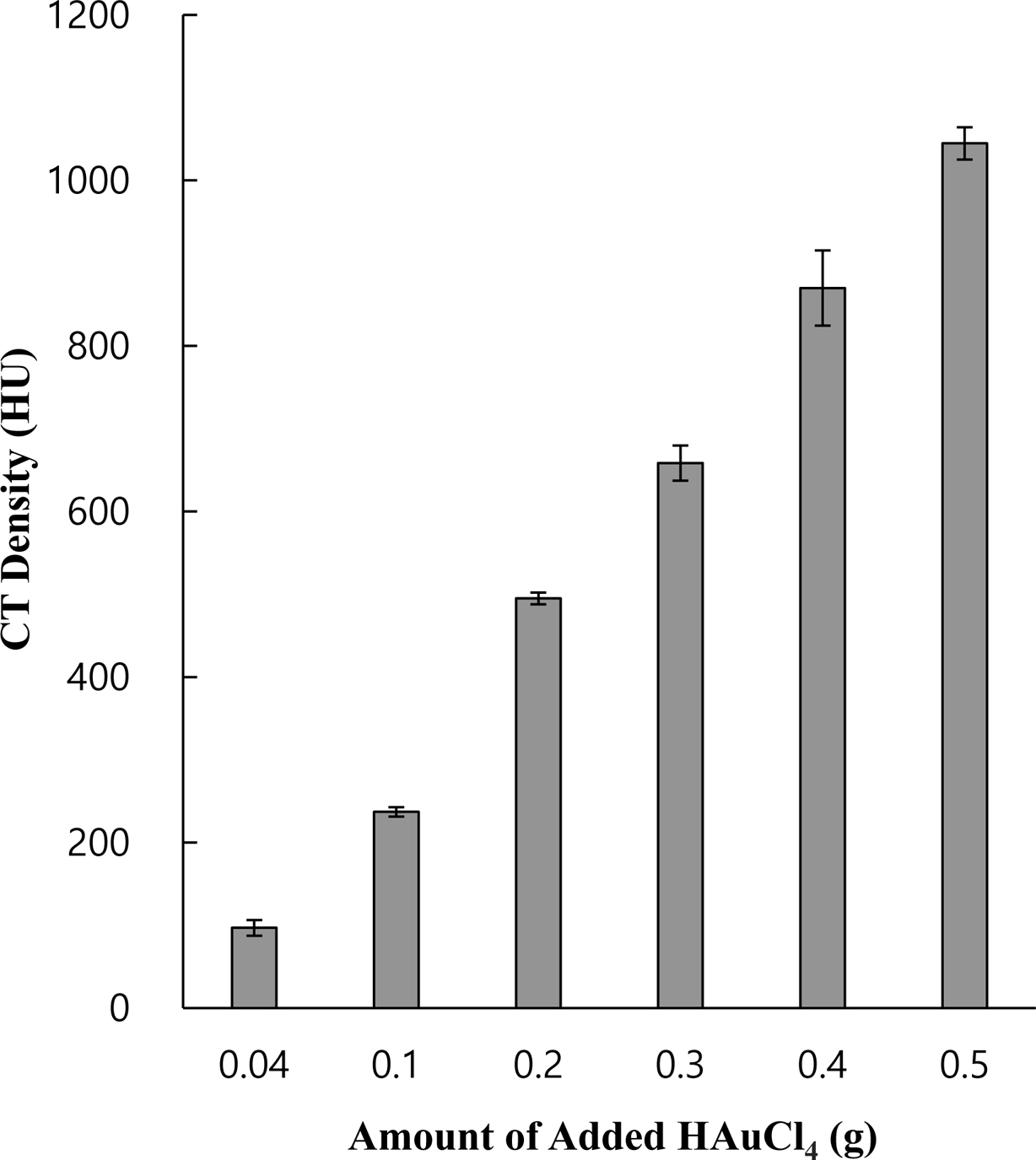
수화젤 필름의 색깔이 보라색을 띠게 되는 것이다. 탑재되는 금 나노입자의 함량이 Au-PEG 수화젤 입자들의 CT세기에 미치는 영향을 관찰하기
위하여 in situ법에서 투입하는 금 전구체인 HAuCl4의 함량을 달리하면서 합성한 Au-PEG 수화제 입자들의
CT세기를 측정하여 Figure 3에 나타냈다. 예상한 바와 같이 투입하는 금 전구체의 함량이 증가함에 따라 최종 Au-PEG 수화젤 입자의
CT세기가 증가함을 볼 수 있었다.
In
situ법으로
Au-PEG 수화젤 입자를 제조할 때, 수화젤 네트워크의 가교밀도가 금 나노입자의 탑재량에 영향을 미칠 수도 있을 것이라 예상하여 중합과정을
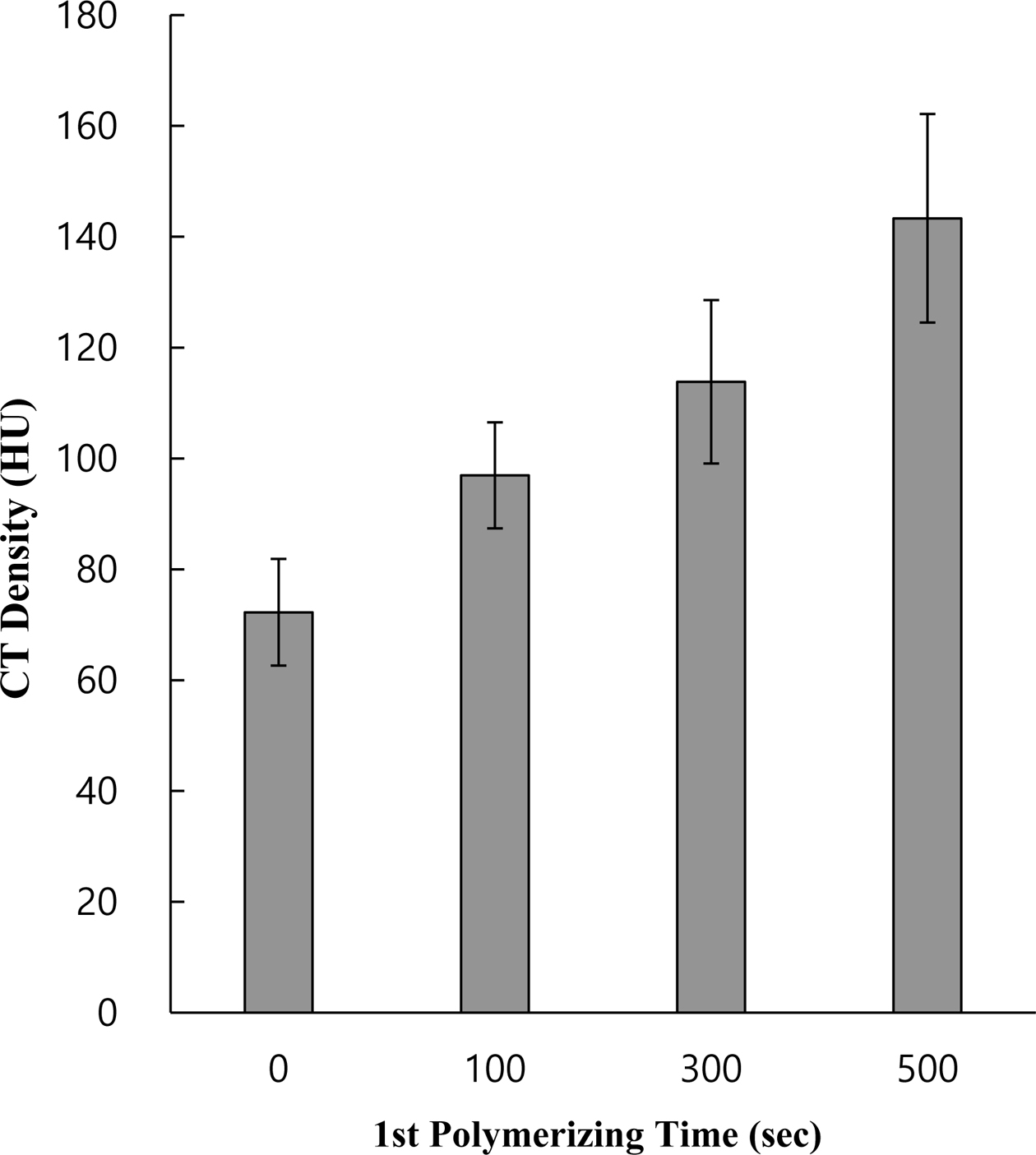
Scheme 1과 같이 두 단계로 나누고, 1차 및 2차 중합시간을 변화시키면서 CT세기에 미치는 영향을 조사하였다. Figure 4는 1차 중합시간의
차이에 따른 Au-PEG 수화젤 입자의 CT세기 변화를 나타낸 것이다. 여기서 1차와 2차 중합시간을 합친 총 중합시간은 600초로 일정하게 하였다.
따라서 1차 중합시간이 늘어나면 2차 중합시간은 상대적으로 감소하게 된다. 예를 들어, 1차 중합시간이 100초인 경우 2차 중합시간은 500초가
된다. Figure 4에서 보는 바와 같이, 1차 중합시간이 증가함에 따라서 Au-PEG 수화젤 입자의 CT세기가 증가함을 볼 수 있다. 즉,
1차 중합시간이 증가함에 따라서 Au-PEG 수화젤 입자 내부에 탑재되는 금 나노입자의 농도가 증가한다는 것을 의미한다. 이 결과는 in
situ법의 1차 중합에서 단량체 일부가 가교를 하여 네트워크 구조를 형성하면 여기에 금 전구체가 존재하다가, 환원제의 투입에 의해 금
나노입자가 되고, 2차 중합에서 완성되는 수화젤의 네트워크에 금 나노입자가 고정되게 되는데, 1차 중합시간이 증가할수록 형성되어지는 가교구조가
조밀하여 환원제에 의해서 형성되는 금 나노입자가 네트워크에 고정될 가능성이 커지는 것으로 설명할 수 있다. 이 결과들을 근거로 본 실험에서는 특별한 언급이 없는 한, 1차 중합시간은 500초 그리고 2차 중합시간은
100초로 각각 수행하였다.
본 연구에서 고분자
수화젤을 입자형태로 합성하기 위하여 현탁중합을 이용하였는데, 일반적으로 현탁중합은 고분자 입자를 중합하는 과정에서 입자들 사이에 응집이 발생하는
것으로 알려져 왔다. 이러한 입자들 사이의 응집을 방지하기 위하여 분산안정제를 첨가해 주는데, 분산안정제는 형성되는 단량체 방울의 표면에 존재하면서
단량체 방울들끼리 응집하는 것을 방지하여서 최종적으로 입자의 분산성을 향상시킨다. 따라서 본 연구에서는 입자들 사이의 응집을 방지하기 위하여 투입하는
분산안정제가 금 나노입자를 제조하기 위하여 투입하는 금 전구체와 상호작용을 하여서 최종적으로 수화젤 입자들 내부에 탑재되는 금 나노입자의 농도에
영향을 미칠 수 있다는 가정 하에 분산안정제가 Au-PEG 수화젤 입자의 CT세기에 미치는 영향을 조사하였다. 분산안정제로는 양이온성 계면활성제인
CTAB, 음이온성 계면활성제인 poly(ethylene glycol) 4-nonylphenyl 3-sulfopropyl ether
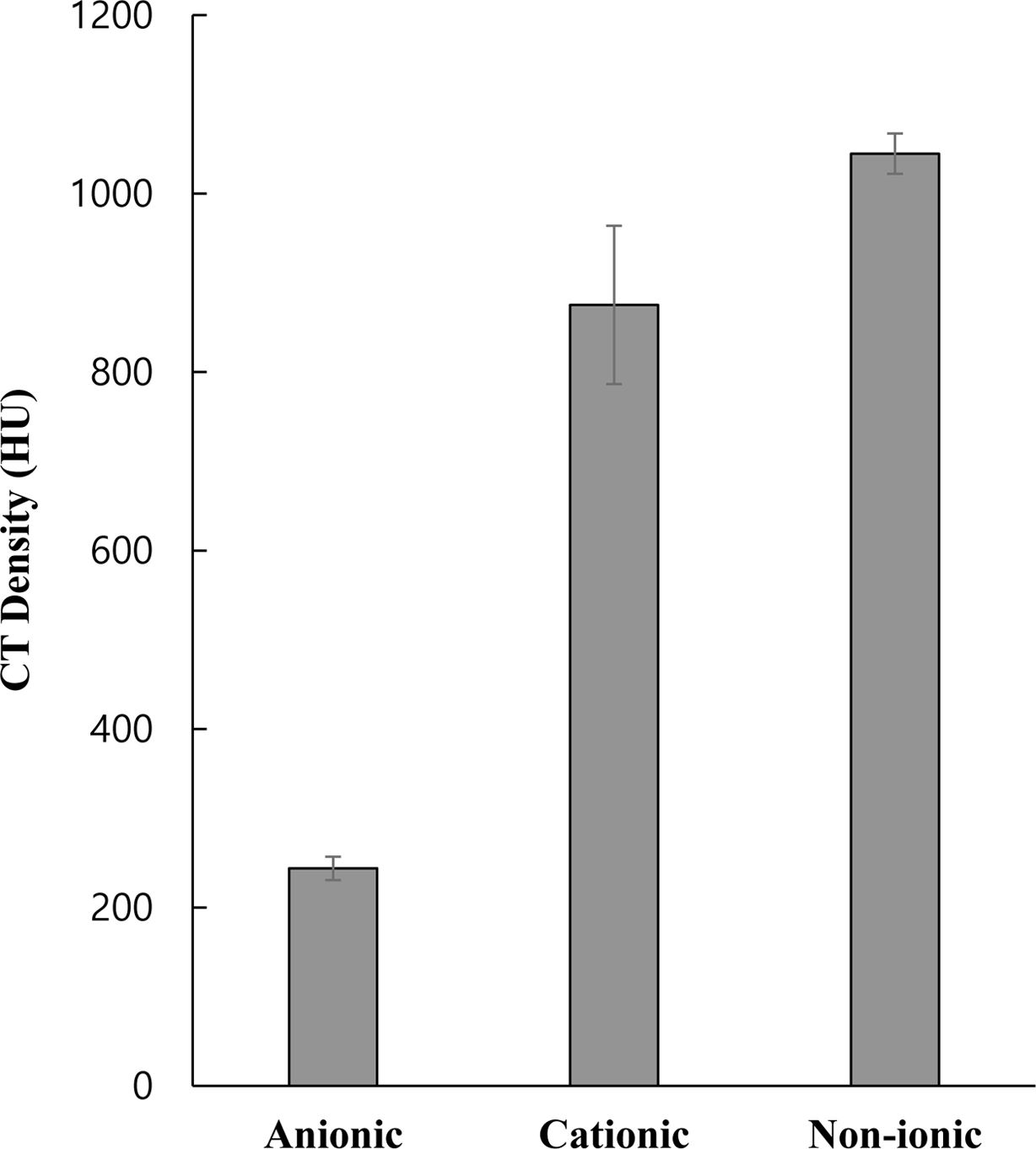
potassium salt, 그리고 비이온성 계면활성제인 Triton X-100를 사용하였다. Figure 5에서 보는 바와 같이, 분산안정제의
종류를 달리하여 제조한 Au-PEG 수화젤 입자 중에서 CT세기가 가장 높은 것은 비이온성인 Triton X-100을 사용하여 제조한 입자로,
평균 1044.7 HU의 CT세기를 나타냈다. 양이온성인 CTAB를 사용하여 제조한 Au-PEG 수화젤 입자는 875.2 HU, 음이온성인 poly(ethylene glycol)
4-nonylphenyl 3-sulfopropyl ether potassium salt를 사용하여 제조한 입자는 243.8 HU의 CT세기를 각각 나타냈다. 이와 같은 결과는 분산안정제로 사용된 계면활성제와 금 전구체인 gold(III)
chloride trihydrate (HAuCl4·3H2O) 사이의 상호작용으로 설명할 수 있다.
Gold (III) chloride trihydrate는 환원제인
trisodium citrate로부터 전자를 제공받기 전에는 양이온 형태로 존재하게 되는데, 음이온 계면활성제인 poly(ethylene glycol)
4-nonylphenyl 3-sulfopropyl
ether potassium salt를 분산안정제로 사용한 경우, 분산안정제가 금 전구체의 양이온과 결합하여 금 입자 형성을 저해할 뿐만 아니라 분산안정제와 결합된 금이온은
중합 후 입자의 세척과정에서 제거가 되어서 음이온 계면활성제를 분산안정제로 사용하여 제조한 입자의 CT세기가 다른 입자들에 비하여 매우 낮은 결과를
가져온 것으로 생각할 수 있다. 그러나 비이온성 계면활성제인 Triton X-100의 경우에는 정전기적 상호작용이 존재하지 않기 때문에
Triton X-100을 분산안정제로 사용할 때, 고농도의 금 나노입자가 수화젤 내부에 탑재되어서 높은 CT세기를 보여주었다. 한편, 양이온 계면활성제인
CTAB를 분산안정제로 사용한 경우에는, 음이온 계면활성제와는 달리 금 이온과 분산안정제 사이에는 정전기적 반발력이 발생하지만, 추후 환원제의 첨가로 인한 금 전구체의
환원에서 분산안정제가 환원제의 전자를 일부 소모하여서 모든 전구체가 금 입자로 환원되는 것을 저해하기 때문에 비이온성 계면활성제인 Triton
X-100를 사용하는 것보다는 제조되어지는 수화젤에 탑재되는 금 나노입자의 농도가 작아서 CT세기가 낮게 관찰되는 것으로 설명할 수 있다.
Au-PEG 수화젤
입자를 여러 분야에서 실제 사용하기 위해서는 무엇보다도 Au-PEG 수화젤 입자로부터 탑재된 금 나노입자들이 외부로 방출되지 않아야 한다. 즉,
Au-PEG 수화젤 입자의 안정성이 보장되어야 한다. 앞서 ex situ법으로 합성한 Au-PEG 수화젤 입자의 경우는 in
situ법으로 제조한 Au-PEG 수화젤 입자보다 CT세기도 작았을 뿐만 아니라 입자 내부에 탑재된 금 나노입자들이 수용액 상에서 시간이 경과하거나 외력이 가해지면 쉽게 방출된다는
문제점이 발견되었다. 따라서 본 연구에서 수행한 in situ법으로 제조한 Au-PEG 수화젤 입자의 안정성을 평가할 필요가 있었다.
안정성 평가를 위하여 초음파로 외부에서 물리적인 외력을 가한 후 Au-PEG 수화젤 입자의 CT세기를 관찰하여 실험결과를 Table 1에 정리하였다.
초음파를 가하기 전 Au-PEG 수화젤 입자의 CT세기는 1044.7 HU, 750 W 세기의 초음파를 가한 후 측정한 CT세기는
1077.9 HU로 큰 차이가 나지 않은 것을 볼 수 있었다. 이 결과는 물리적 외력에도 수화젤 입자에 탑재된 금 나노입자가 방출되지 않았음을
보여주며, 이것은 in situ법으로 합성한 Au-PEG 수화젤 입자가 안정하다는 것을 의미한다.
|
Figure 1 CT density of AuNPs and Au-PEG hydrogel particles prepared using ex situ and in situ polymerization. |

|
Figure 2 Images of Au-PEG hydrogels prepared by in situ polymerization: (a) optical image of Au-PEG hydrogel films; (b) TEM image
of Au-PEG hydrogel particles. |
|
Figure 3 CT density of Au-PEG hydrogel particles prepared using
in situ polymerization as a function of amount of added Au precursor (HAuCl4). |
|
Figure 4 CT density of Au-PEG hydrogel particles prepared using
in situ polymerization as a function of 1st polymerization time. |
|
Figure 5 CT density of Au-PEG hydrogel particles prepared using
in situ polymerization as a function of type of dispersion stabilizer
(anionic: poly(ethylene glycol) 4-nonylphenyl 3-sulfopropyl ether
potassium salt, cationic: CTAB, and non-ionic: Triton X-100). |
X선 흡수효율이 우수한
금 나노입자를 영상의학기기인 CT의 조영제로 사용하기 위해서는 금 나노입자를 작은 공간에 고농도로 집적시켜 국부적인 CT세기를 증가시킬 필요가
있다. 따라서 본 연구에서는 생체적합성이 우수한 PEG 수화젤 입자 내부에 고농도로 금 나노입자를 탑재한 유무기 복합재료를 합성하여 CT 조영제로서의
활용 가능성을 평가하여 보았다. 우선 금 나노입자를 PEG 수화젤에 고농도로 탑재하는 다양한 방법을 비교한 결과, 한 용기내 중합반응인 in
situ법을 사용하였을 때, 가장 높은 CT세기를 가지고, 탑재된 금 나노입자가 수화젤로부터 이탈하지 않는 안정적인 Au-PEG 수화젤
입자를 합성할 수 있었다. 그리고 in situ법을 사용하여 입자를 제조할 경우, 중합과정에서 1차 중합시간이 증가할수록 그리고 투입한
금 전구체의 함량이 증가할수록, 최종 Au-PEG 수화젤 입자의 CT세기가 증가하였으며, 비이온성 계면활성제를 분산안정제로 사용할 경우, 입자들
사이의 응집이 적으면서 가장 높은 CT세기를 가지는 Au-PEG 수화젤 입자들을 제조할 수 있었다.
- 1. S. Mahouche-Chergui, M. Guerrouache, B. Carbonnier, and M. M. Chehimi, Colloids Surf. A-Physicochem. Eng. Asp., 439 43 (2013).
-

- 2. S. Xu, J. Zhang, and E. Kumacheva, Compos. Interfaces, 10, 405 (2003).
-

- 3. A. A. Farah, J. P. Bravo-Vasquez, R. A. Alvarez-Puebla, J. Cho, and H. Fenniri, Small, 5, 1283 (2009).
-

- 4. C. Wang, N. T. Flynn, and R. Langer, Adv. Mater., 16, 1074 (2004).
-

- 5. S. R. Kemmerer, K. J. Mortele, and P. R. Ros, Radiol. Clin. North Am., 36, 247 (1998).
-

- 6. P. Leander, P. Hoglund, A. Borseth, Y. Kloster, and A. Berg, Eur. Radiol., 11, 698 (2001).
-

- 7. R. L. Baron, Am. J. Roentgenol., 163, 323 (1994).
-

- 8. X. Dai, H.-P. Schlemmer, B. Schmidt, K. Hoh, K. Xu, T. M. Ganten, and M. K. Ganten, Eur. J. Radiol., 82, 327 (2013).
-

- 9. H. Shin, Y. Cho, K. Lee, C. Lee, B. W. Choi, and B. Kim, J. Liposome Res., 24, 124 (2014).
-

- 10. J. Zheng, J. Liu, M. Dunne, D. A. Jaffray, and C. Allen, Pharm. Res., 24, 1193 (2007).
-

- 11. H. Katayama, A. Spinazzi, X. Fouillet, M. A. Kirchin, P. Taroni, and A. Davies, Invest. Radiol., 36, 87 (2001).
-

- 12. J. F. Hainfeld, D. N. Slatkin, T. M. Focella, and H. M. Smilowitz, Br. J. Radiol., 79, 248 (2006).
-

- 13. N. A. Peppas, P. Bures, W. Leobandung, and H. Ichikawa, Eur. J. Pharm. Biopharm., 50, 27 (2000).
-

- 14. S. Lee, I. Kwon, and K. Park, Adv. Drug Deliv. Rev., 65, 17 (2013).
-

- 15. R. Langer and N. A. Peppas, AICHE J., 49, 2990 (2003).
-

- 16. N. H. A. Samah and C. M. Heard, Int. J. Pharm., 453, 630 (2013).
-

- 17. S. Maya, B. Sarmento, A. Nair, N. S. Rejinold, S. V. Nair, and R. Jayakumar, Curr. Pharm. Design, 19, 7203 (2013).
-

- 18. Y. Tahara, S. Kosuge, S. Sawada, Y. Sasaki, and K. Akiyoshi, React. Funct. Polym., 73, 958 (2013).
-

- 19. S. J. Bryant and K. S. Anseth, J. Biomed. Mater. Res., 59, 63 (2002).
-

- 20. Y. Kim, M. Chung, and B. Kim, Korea-Aust. Rheol. J., 26, 401 (2014).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2022 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(6): 784-789
Published online Nov 25, 2020
- 10.7317/pk.2020.44.6.784
- Received on May 22, 2020
- Revised on Jun 25, 2020
- Accepted on Jul 2, 2020
 Services
Services
Shared
 Correspondence to
Correspondence to
- Bumsang Kim
-
Department of Chemical Engineering, Hongik University, Wausanro 94, Mapo-gu, Seoul 04066, Korea
- E-mail: bskim@hongik.ac.kr
- ORCID:
0000-0001-7519-168X











 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.