- [Communication]
- Development of Novel Collagen Stimulator Based on Polycaprolactone-poly(ethylene glycol)-polycaprolactone Block Copolymer
Hyeon Jin Jeon*, **,†
 , Woo Sung Lee*, Hak Jin Song*, and Hyung Joo Kim**
, Woo Sung Lee*, Hak Jin Song*, and Hyung Joo Kim***R&D Ceneter, ROSELAB Inc, 209 Bongeunsa-ro, Gangnam-gu, Seoul 06109, Korea
**Department of Biological Engineering, Konkuk University, 120 Neungdong-ro, Gwangjin-gu, Seoul 05029, Korea- 폴리카프로락톤-폴리에틸렌글리콜-폴리 카프로락톤 삼중 블록 공중합체 소재 콜라겐 생성 촉진제 개발
*㈜로즈랩, R&D센터
**건국대학교 생물공학과Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
We synthesized the triblock copolymers consisting of poly(ethylene glycol) (PEG) (Mn 4000 g/mole) and polycaprolactone (PCL) by ring-opening polymerization of ε-caprolactone with poly(ethylene glycol) as an initiator the stannous octoate. The 20 wt% aqueous solution of PCL-PEG-PCL triblock copolymer was exhibited a size of approximately 314 nm by DLS. To confirm the in vivo neocollagenesis, we observed the collagen fiber density in the dermis of Sprague-Dawly (SD) rat after injection of 20 wt% aqueous solution of the PCL-PEG-PCL triblock copolymer. we observed the collagen fiber density was 12% higher in the 8-week group compared to the PBS-injection control group. Furthermore, we confirmed that the presence of injected PCL-PEG-PCL particle at 1 week. In this study, we evaluated in vivo biodegradability and neocollagenesis ability of synthesized triblock copolymer and confirmed the possibility as the collagen stimulator.
평균분자량 4000 g/mole 폴리에틸렌글리콜(PEG)와 폴리카프로락톤(PCL)으로 구성된 PCL-PEG-PCL 삼중 블록 공중합체를 주석산화합물의 존재 하에서 개환중합을 통해 합성하였다. 20 wt% 수용액 상태의 PCL-PEG-PCL 삼중 블록 공중합체는 동적광산란으로 분석한 결과, 입자는 약 314 nm임을 확인하였다. 콜라겐 재생성을 확인하기 위하여 20 wt% 공중합체 용액을 Sprague-Dawly(SD) 랫드의 피내에 주입한 결과, 투여 8주차에 콜라겐 섬유 밀도가 인산완충 생리식염수 투여군보다 12% 더 높았으며 투여 1주 후에는 잔존 물질이 확인되었으나 투여 2주 이후에는 잔존 물질이 관찰되지 않았다. 본 연구에서는 삼중블록 공중합체를 합성하여 피내에 투여하여 생분해와 콜라겐 재생성을 평가하였고, 콜라겐 생성 촉진제로의 가능성을 확인하였다.
The collagen-stimulating effect of polycaprolactone (PCL)-based microparticles is achieved by directly stimulating fibroblasts to promote collagen production. PCL-polyethylene glycol (PEG) block copolymer addresses issues of particle size, biodegradation period, foreign body reactions effects associated with PCL. This study focuses on evaluating the foreign body reaction, residual particles, biodegradability, and collagen production capability of a collagen stimulator fabricated from PCL-PEG-PCL block copolymers.
Keywords: copolymer, dermal filler, pegylation, polycaprolactone, poly(ethylene glycol).
이 논문은 2024년도 산업통상자원부의 재원으로 한국산업기술진흥원의 지원을 받아 수행되었습니다(P0023220, 폴리카프로락톤 소재를 이용한 하이드로겔 조직수복재료 개발).
저자들은 이해상충이 없음을 선언합니다.
다음과 관련된 실험 과정에 대한 정보(PCL-PEG-PCL 삼중 블록 공중합체의 동물실험 결과). 이 자료는 다음 사이트에서 얻을 수 있습니다 (https://journal.polymer-korea.or.kr).
PK_2025_049_02_159_Supporting_Information.pdf (3,800 kb)
Supplementary Information
2009년 새로운 콜라겐 생성 촉진제(Ellansé®, Sinclair Pharma, London, UK)가 CE 인증을 획득하여 전 세계 에스테틱 시장에 소개되었다. 이 콜라겐 생성 촉진제는 친수성 카르복시메틸 셀룰로오스(carboxymetyl cellulose, CMC) 겔 캐리어와 폴리카프로락톤(polycaprolactone, PCL) 마이크로스피어로 구성되어 있다.1 CMC 겔의 1차 수복효과 후에 6-8주간 점차 CMC가 분해되며 PCL 마이크로입자의 생성자극 효과는 주입 후 4주 이후에 섬유아세포
를 직접 자극하여 콜라겐 생성 촉진을 유도하여 안면부 주름과 볼륨을 수복한다고 알려져 있다.2 그러나 PCL 입자 크기가 20-50 mm로 인한 부작용 우려 때문에 콜라겐 생성 자극 효과를 높일 수 있는 피내 주사는 사용할 수 없는 단점을 가지고 있다.3 Pegylated PCL 소재로 한 콜라겐 생성 촉진제가 소개되었으며, 동물실험과4 눈가주름의 임상실험을5 수행하였으나 입자의 크기와 PCL 분자량에 따른 collagen fiber density와 생분해 기간에 대한 보고가 되지 않았다.
다양한 의학 분야에서 사용되고 있는 생체적합성고분자인 폴리에틸렌글리콜(poly(ethylene glycol), PEG)는 물과 유기용매에 대한 높은 용해도를 가지며 비독성이며 단백질 흡착 억제 효과가 크고 친수성이기 때문에 인체 내에서 용해되어 신체 외부로 배출된다.6 이미 PEG를 개시제로 하여 PEG-PCL 블록 공중합체와 같은 주사제형의 약물로서 다양한 연구가 이루어졌다.7,8 그러나 PEG-PCL 블록 공중합체 입자 크기와 분자량에 따른 in vivo 생분해 기간과 콜라겐 생성 촉진제로의 연구가 더 필요하다.
본 연구에서는 평균분자량 4000 g/mol인 폴리에틸렌글리콜을 개시제로 하여 카프로락톤의 개환 중합을 통해 합성된 PCL-PEG-PCL 삼중 블록 공중합체가 콜라겐 생성 촉진제의 역할을 확인하고자 수용액 상태로 제조하여 Sprague-Dawly (SD) 랫드에 주입하여 이물반응과 생분해, 콜라겐 생성 여부를 확인하였다.
시약 및 재료. 개시제로서 PEG(Sigma-Aldrich, USA)는 평균분자량 4000 g/mol를 사용하였고 반응 단량체로서 카프로라톤(ε-caprolactone, ε-CL, Sigma-Aldrich, USA)은 칼슘하이드라이드하에서 감압하여 정제하였고, 냉장 보관하였다. 단량체 카프로라톤의 중합촉매로서 주석산화합물(Stannous octotate, Sigma-Aldrich, USA)를 사용하였고, 공중합체의 반응용매로 메틸렌클로라이드(methylene chloride, MC, SAMCHUN chemical)를 사용하였다. 반응 후 고분자의 침전을 위한 헥산(hexane, SAMCHUN chemical)을 사용하였다.
블록 공중합체 수용액을 제조하기 위한 용수는 대한 멸균증류수(water for injection, Daehan-Pharma)을 사용하였다. 동물실험의 대조군으로는 인산완충생리식염수(phosphate buffered saline, PBS, Gibco, UK)을 사용하였다.
PCL-PEG-PCL의 합성. PCL-PEG-PCL 블록 공중합체를 합성하기 위하여, 개시제인 PEG 1 mmol와 ε-CL 228 mmol를 1 L 반응기에 투입한 후 반응용매 MC를 넣은 다음 중합 촉매로서 0.1 M Sn(Oct)2을 0.005 mol 주입하여 24시간 동안 130 ℃에서 교반시켜 주었다. 반응 후 미반응 단량체나 개시제를 제거하기 위하여 1000 mL의 헥산에 반응물을 서서히 떨어트리면서 침전시켜 주었다. 침전물은 MC에 녹여 거름종이로 거른 후 회전증발기를 통하여 용매를 제거하고자 감압 하에서 2일 동안 건조시켰다.7
PCL-PEG-PCL의 필러 제조. PCL-PEG-PCL 블록 공중합체 필러를 제조하기 위하여, 제조탱크 1000 mL에서 20 wt%의 농도를 갖는 블록 공중합체는 멸균증류수를 가하여 80 ℃에서 용해한 후, 수용액내 공중합체 입자의 균일한 분산을 위해 4 ℃에서 24시간 동안 냉장 보관하였다.8 보관한 고분자 수용액은 멸균 바이알에 3 mL 용액을 주입하고, 멸균 고무마개로 밀전하고 알루미늄 캡으로 밀봉하여 포장을 완료하였다. 용액의 제조 및 충전 공정은 청정도 ISO 5 등급 하에서 무균 공정으로 수행하였고 30 ℃ 이하 실온에서 보관하였다.
특성분석. PCL-PEG-PCL 블록 공중합체의 각각 블록 몰비에 대한 분자량은 내부 기준 시료인 0.05 wt% 테트라메틸실란(TMS)을 포함한 CDCl3(Merck, Germany)을 용매로 하여 1H NMR(Bruker AVANCE II 500 MHz, USA)를 통하여 분석하였다.
수용액의 특성을 분석하기 위해 동적광산란방식(dynamic laser scanning, DLS)의 입도분석기 Litesizer 500(Anton Paar, Austria)를 이용하여 25 ℃에서 입자 크기 및 다분산성(polydispersity)를 분석하였다. 또한, 입자의 형태를 분석하기 위해 Cryo-FE SEM(Crossbeam 550, Carl Zeiss, Germany)을 이용하여 이미지를 촬영하였다. 블록 공중합체 수용액의 pH는 pH미터(HI-2210, HANA instrument, USA)를 이용하여 측정하였다.
동물실험. 본 연구는 건국대학교 동물실험 윤리위원회의 승인을 얻은 후, 위원회의 감독을 받아 수행하였다(KU22089).PCL-PEG-PCL 블록 공중합체의 이물반응(foreign body reaction)과 잔존 물질의 유무를 판단하기 위하여 제조한 20 wt% 용액을 1cc 주사기(30G)를 이용하여 고분자 0.2 mL 용액을 6주령 SD 랫드 피내 투여하였으며, 대조군으로는 PBS을 사용하였다. 투여 1주, 2주, 4주, 8주 후 투여 부위를 생검하여 파라핀 블록으로 제조한 후 3 mm 두께로 절편하여 hematoxylin-eosin(H&E)
염색과 Masson-Trichrome (MT) 염색을 진행하였다. 광학현미경(NSM-3B, SAMWON, Korea)을 이용하여 H&E 염색사진을 촬영하여 이물반응에 따른 염증세포 수와 거대세포, 육아종의 생성유무와 잔존 입자의 유무를 확인하였다.4 또한, 블록 공중합체의 collagen의 생성을 판단하기 위하여 MT염색사진을 촬영 후, Image J(The National Institutes of Health, USA) 프로그램을 이용하여 촬영된 원본 이미지의 color(RGB) channel을 deconvolution한 후 단색 이미지로 분리시켰다. 이후 이미지를 이용하여 투여 부위의 콜라겐 섬유 밀도(collagen fiber density)를 분석하였다.
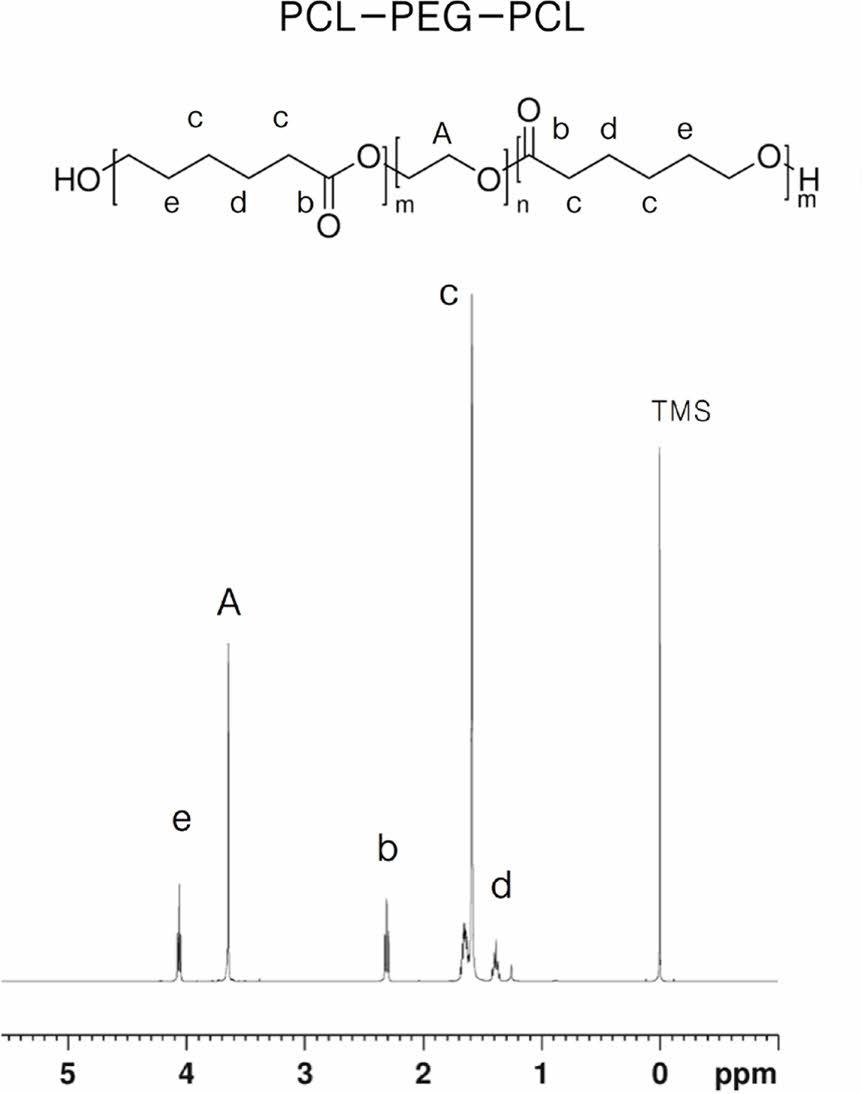
PCL-PEG-PCL 블록 공중합체의 합성. 개시제로 PEG의 말단 OH에 활성화된 ε-CL의 개환중합을 통해 공중합체를 합성하였다. Sn(Oct)2의 존재 하에서 ε-CL과 PEG를 사용하여 중합하였다. 중합된 PCL-PEG-PCL 공중합체의 특정 작용기에 대한 분자 구조와 분자량은 1H-NMR으로 분석하였다(Figure 1) PEG의 반복되는 CH2의 proton은 δ=3.64 ppm(A)에서 신호를 확인할 수 있었다. PCL의 각각의 신호 (b~e)는 δ=2.30, 1.62, 1.39, 그리고 4.07 ppm에서 관찰되었다. PCL-PEG-PCL 블록공중합체를 선행 연구된 1H NMR으로 분석한 각 신호와 비교한 결과가 유사함을 확인할 수 있었다.9 블록 공중합체의 분자량은 각 PEG 블록과 PCL 블록 분자량을 합하여 계산하였다. PCL-PEG-PCL의 이론적 분자량은 분자량 29110 g/mol이며, 1H NMR으로 분석 결과 분자량은 31155 g/mol로 계산되었다(Table 1). 이론적 분자량은 잔존 미반응 단량체 없이 완전 반응이 이루어진 것을 가정하여 계산되었으며, 1H NMR으로 계산한 분자량과 차이는 선행연구에서도 확인되었다.9
PCL-PEG-PCL 블록 공중합체의 수용액. PCL-PEG-PCL 20 wt%의 수용액상 입자 크기와 다분산지수는 분석하였다. 입자의 유체역학적 직경(hydrodynamic diameter)는 314 nm로 측정되었으며, 다분산성은 28.1%로 분석되었다(Figure S1(a)). 수용액을 Cryo-SEM으로 촬영하여 구형 나노입자 형태의 군집을 확인하였다(Figure S1(b)). SEM 촬영으로 분석한 입자의 크기는 약 100 nm 이하로 확인된다. 수용액 상에서 PCL-PEG-PEC 삼중 블록 공중합체는 입자의 내부(core)는 소수성 PCL로 외부(shell)는 친수성인 PEG가 Loop형태로10 알려져 있으며, 유체역학적 직경은 입자 외부(shell)의 PEG Loop 형태를 포함하여 측정하고 내부(core) 직경 크기를 측정하는 SEM을 이용한 측정 결과보다는 유체역학적 직경이 더 커지는 경향에 대하여 보고하였다.11
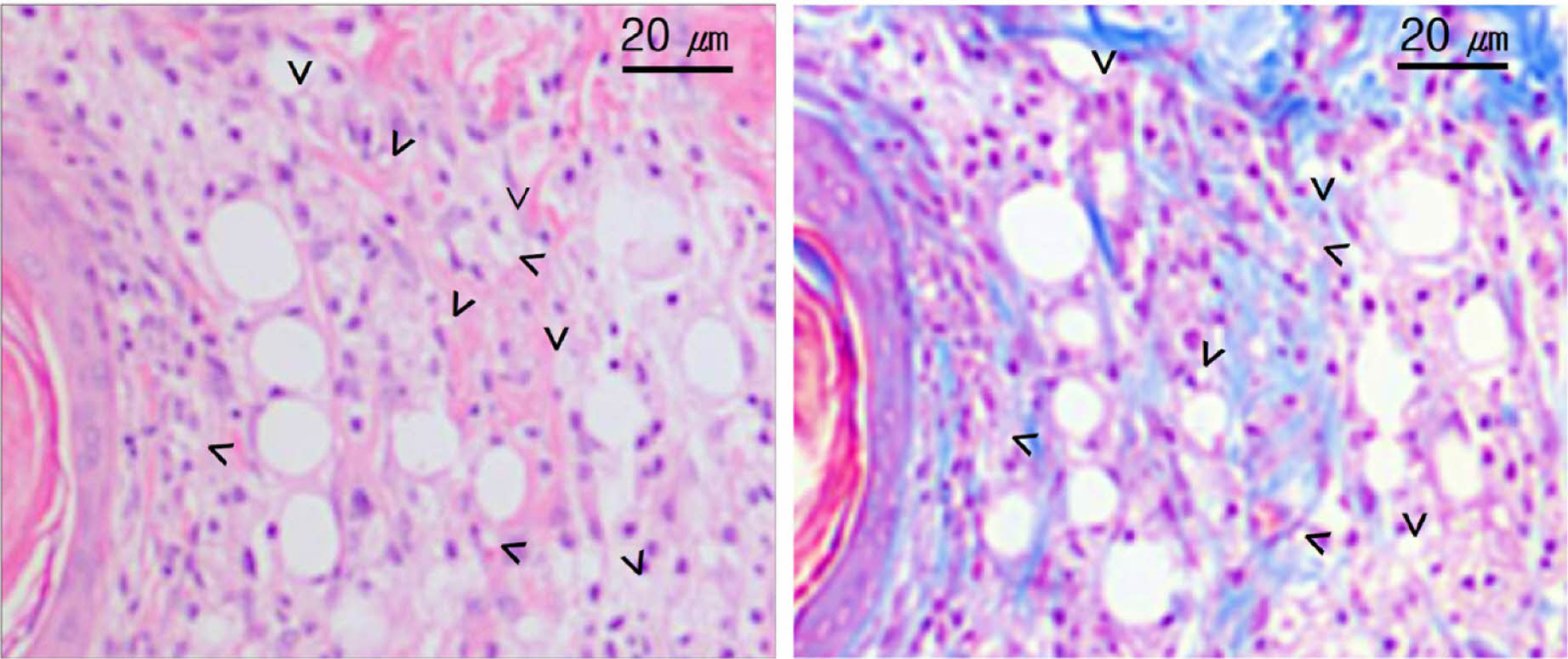
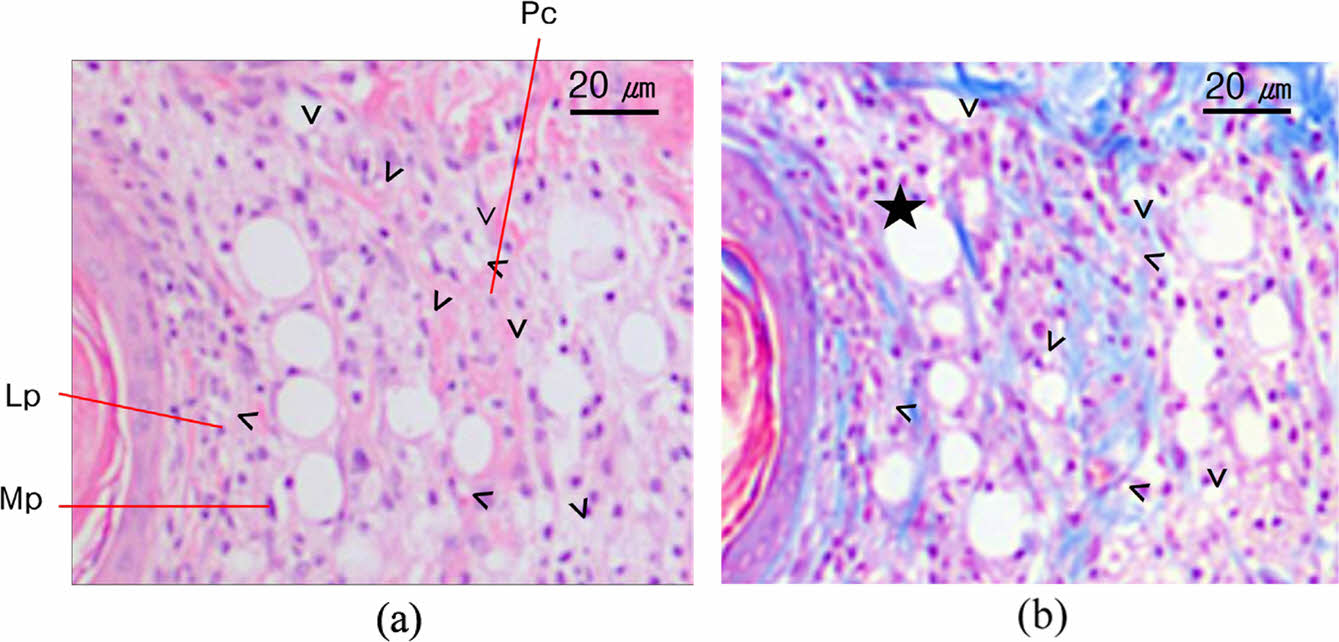
동물실험. SD 랫드 등 부위 피내에 20 wt% PCL-PEG-PCL 수용액은 투여한 부위에서 1주 후 염증 세포가 다수 발견되었으며, 잔존하는 PCL-PEG-PCL 입자 군집이 확인되었다(Figure 2(a),(b)). PCL-PEG-PCL 입자 군집이 진피(dermis)에 위치하며 일부는 진피 하(hypodermis)까지 존재하였다(Figure S2). 입자 군집 주변으로 림프구 등이 다수 관찰되었으나 섬유화나 육아종은 관찰되지 않았다. 2주차에서 1주차보다 염증세포의 수가 감소한 상태로 관찰되었으며, 거대세포 및 육아종이 관찰되지 않았다(Figure S3). PCL-PEG-PCL 수용액 투여 후 모든 시험기간에서 육아종과 거대세포는 관찰되지 않았다. PBS 투여군은 투여 후 1주차에만 소수의 림프구만 확인되었으며, 2주차 이후 염증세포는 관찰되지 않았다.
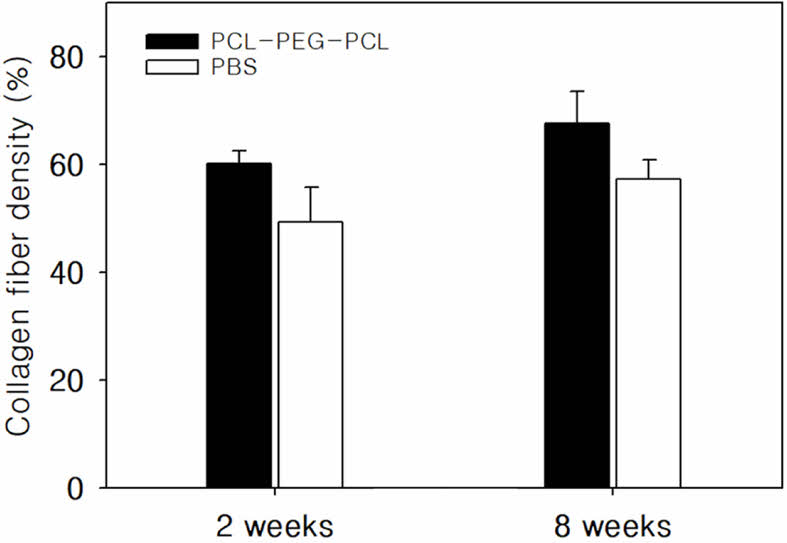
블록 공중합체 수용액의 투여부위 MT 염색 이미지를 이용하여 콜라겐 섬유 밀도를 분석하였다. 블록공중합체 수용액 투여군의 콜라겐 섬유 밀도는 2주차 60.09%, 8주차 67.53%로 분석되었다. PBS 투여군은 2주차 48.19%, 8주차 55.13%로 분석되었다. 8주차에는 PBS 투여군과 대비하여 약 12.4% 증가하였다(Figure 3).
PCL-PEG-PCL 블록 공중합체 20 wt% 수용액 투여 후 시간이 경과함에 따라, 콜라겐 섬유가 두꺼워지는 것을 확인하였다(Figure S4). 대조군인 PBS 투여 부위도 일부 콜라겐이 생성되어 증가한 결과를 보였으나, 이는 실험동물의 성장과 주사침에 의한 초기 콜라겐 생성 자극 유발로 인한 보고된 사례가 있다.4 PCL-PEG-PCL 블록 공중합체 수용액의 콜라겐 생성 촉진제(collagen stimulator)로서의 작용원리는 기존 PCL 입자와는 상이한 것으로 파악된다. PCL 마이크로 입자는 장기간 분해되지 않는 특징을 가지고 있다. 주입된 PCL 마이크로 입자는 급성기에는 다양한 염증세포가 유입되는 특징을 보이며, 만성기에 입자 주변으로 거대세포가 둘러싸고, 섬유아세포에서 생성된 콜라겐에 의해 캡슐화가 진행된다. 시간이 경과함에 따라 더 많은 콜라겐 섬유(collagen fiber)가 마이크로 입자 주변에서 증가한다고 알려져 있다(Figure S4).12,13 그러나 PCL-PEG-PCL 블록 공중합체 입자를 포함하는 수용액의 in vivo 이물평가 실험에서는 PCL 마이크로 입자의 콜라겐 재생 시 관찰되는 거대세포와 캡슐화가 관찰되지 않았다. 또한, 잔존 입자가 2주 이내 빠르게 생분해되는 특징을 가지므로 기존의 콜라겐 생성 촉진제와는 콜라겐 생성 촉진 작용원리가 상이한 것으로 판단된다. 또한, 본 연구에서 사용한 PCL-PEG-PCL 블록 공중합체 입자의 생분해에 대한 특징은 기존 PCL 마이크로입자와 생분해 기간과는 차이가 있는 것으로 결과가 분석되었다. PCL-PEG-PCL 블록 공중합체 분자량이 31115 g/mol이며 PCL 블록의 분자량은 27154 g/mol로 투여 2주 후에는 잔존하고 있는 블록 공중합체의 입자를 식별하기 어려웠다. PCL 마이크로입자의 체내 생분해 연구13에 따르면, 25000 g/mol PCL 마이크로입자의 분해기간은 약 1.51년으로 예측되어 PCL-PEG-PCL 블록공중합체 입자의 분해 기간과는 큰 차이가 있다. PCL 마이크로입자는 25-50 mm로 입자 크기가 크고 표면이 소수성 입자인 반면에, PCL-PEG-PCL 공중합체는 314 nm으로 상대적으로 입자 크기가 작고 표면이 친수성 입자로서 분해 거동이 상이한 것으로 판단된다.
PEG-PCL 블록 공중합체(PEG 10000 g/mol, PCL 22000 g/mol) 나노 입자의 분해 연구에서는 나노 입자가 체액과 유사한 인산완충용액(pH 7.4)에서 15일 동안 노출 시 공중합체 입자 크기가 135 nm에서 75 nm로 축소되었다. PEG-PCL 공중합체 미셀 쉘(shell)에서 PEG 세그먼트가 입자로부터 분리되고 PCL 코어에서 점차 분해가 된다고 보고하였다.14 PCL-PEG-PCL 블록 공중합체의 입자는 외부(shell)는 친수성이며, 내부(core)는 소수성으로 이루어져 구조가 유사하다. 그러므로 PCL-PEG-PCL 블록 공중합체 입자는 SD 랫드 투여 후 체내에서의 분해되어 2주 후 잔존 여부를 확인하기 어려운 더 작은 나노입자로 분해된 것으로 추정된다.
|
Figure 1 1H NMR spectra of PCL-PEG-PCL block copolymer. |
|
Figure 2 Photograph of 1 week after PCL-PEG-PCL block copolymer filler injection in dermis: (★) Adipocyte; (∨) PCL-PEG-PCL copolymer filler; Lp(Lymphocytes); Pc(Polymorphonuclear cells); Mp(Macrophages): (a) H&E staining (×200); (b) MT staining (×200). |
|
Figure 3 Collagen density of PCL-PEG-PCL triblock copolymer solution (20 wt%) and PBS on the dermis of SD rat. |
|
Table 1 Molecular Weight of PCL-PEG-PCL Block Copolymer |
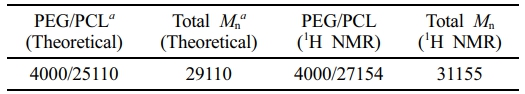
a Theoretical value, calculated according to the feed ratio |
본 연구에서는 31155 g/mol인 PCL-PEG-PCL 블록 공중합체를 합성하여 20 wt%에서 수용액상에서 314 nm인 입자를 제조하였다. 20 wt% 삼중 블록 공중합체 수용액은 SD rat 피내 주사되어 진피에서 육아종이나 거대세포를 관찰되지 않으며 콜라겐 생성을 촉진함을 확인하였다. 이러한 결과로 고분자 수용액은 액상 제형으로 피내 투여가 가능하며, 입자 크기로 인한 부작용을 개선할 수 있어 PCL-PEG-PCL 공중합체를 합성하여 새로운 콜라겐 생성 촉진제로서 응용 가능성이 있음을 확인하였다. 현재, 합성된 블록 공중합체의 콜라겐 생성 촉진 메커니즘을 규명하기 위하여 인간피부섬유아세포를 이용하여 in vitro 실험이 진행 중이다.
- 1. Christen, M. O.; Vercesi, F. Polycaprolactone: How a Well-known and Futuristic Polymer has become an Innovative Collagen-stimulator in Esthetics. Clin. Cosmet. Investig. Dermatol., 2020, 31-48.
-

- 2. Melo, F.; Nicolau, P.; Piovano L.; Lin, S. L.; Tiago, B. F.; King, M. Recommendations for Volume Augmentation and Rejuvenation of the Face and Hands with the New Generation Polycaprolactone-based Collagen Stimulator (Ellanse®). Clin Cosmet. Investig. Dermatol., 2017, 431-440.
-

- 3. Lee, S. J.; Lee, W. S.; Chung, C, H. Safety and Efficacy of Polycaprolactone Copolymer Nanosphere Hydrogel Injected into the Scalp Dermal Tissue of Rats. Arch. Aesthetic Plast. Surg., 2019,25, 147-153.
-

- 4. Hong, J. Y.; Kim, J. H.; Kwon, T. R.; Hong, J. K.; Li, K.; Kim, B. J. In vivo Evaluation of Novel Particle-free Polycaprolactone Fillers for Safety, Degradation, and Neocollagenesis in a Rat Model. Dermatol. Ther., 2022, 34, e14770.
-

- 5. Choi, S. Y.; Koh, Y. G.; Yoo, K. H.; Han, H. S.; Seok, J.; Kim B. J. A Randomized, Participant and Evaluator-Blinded, Matched-Pair, Prospective Study Comparing the Safety and Efficacy Between Polycaprolactone and Polynucleotide Fillers in the Correction of Crow’s Feet. J. Cosmet. Dermatol., 2024, 24, e16576.
-

- 6. Hyun, H.; Cho, Y. H.; Jeong, S. C.; Lee, B.; Kim, M. S.; Khang, G. S.; Lee, H. B. Synthesis and Characterization of Biodegradable Methoxy Poly(ethylene glycol)-Block Copolymers. Polym. Korea,2006, 30, 28-34.
- 7. Seo, K. S.; Park, C. S.; Kim, M. S.; Cho, S. H; Lee, H. B.; Khang, G. S. Thermosensitive Sol-gel Phase Transition Behavior of Methoxy Poly(ethylene glycol)-b-Poly(ε-caprolactone) Diblock Copolymers. Polym. Korea,2004,28, 344-351.
-

- 8. Grossen, P.; Witzigmann, D.; Sieber, S.; Huwyler, J. PEG-PCL-based Nanomedicines: A Biodegradable Drug Delivery System and its Application. J. Controlled Release,2017,260, 46-60.
-

- 9. Nguyen, T. H.; Nguyen, V. C. Formation of Nanoparticles in Aqueous Solution from Poly(ε-caprolactone)–poly(ethylene glycol)–poly(ε-caprolactone). Adv. Nat. Sci. Nanosci. Nanotechnol. 2010, 1, 025012.
-

- 10. Łukasiewicz, S; Mikołajczyk, A; Błasiak, E; Fic, E; D.W, Dziedzicka, M. Polycaprolactone Nanoparticles as Promising Candidates for Nanocarriers in Novel Nanomedicines. Pharmaceutics,2021, 13, 191.
-

- 11. Rabanel, J.M; Hildgen, P; Banquy, X. Assessment of PEG on Polymeric Particles Surface, a Key Step in Drug Carrier Translation. J. Control. Release, 2014, 185, 71-87.
-

- 12. Guo, J; Fang, W; Wang, F. Injectable Fillers: Current Status, Physicochemical Properties, Function Mechanism, and Perspectives. RSC. Adv. 2023, 13, 23841-23858.
-

- 13. Kim, J. S. Isovolemic Degradation of Polycaprolactone Particles and Calculation of their Original Size from Human Biopsy. Plast. Reconstr. Surg. Glob. Open, 2020, 8, e2866.
-

- 14. Jiang, Z.; Zhu, Z; Liu, C.; Hu, Y.; Wu, W.; Jiang, X. Non-enzymatic and Enzymatic Degradation of Poly(ethylene glycol)-b-poly(ɛ-caprolactone) Diblock Copolymer Micelles in Aqueous Solution. Polym., 2008, 49, 5513-5519.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2024 Impact Factor : 0.6
- Indexed in SCIE
 This Article
This Article
-
2025; 49(2): 159-162
Published online Mar 25, 2025
- 10.7317/pk.2025.49.2.159
- Received on Nov 20, 2024
- Revised on Jan 15, 2025
- Accepted on Jan 21, 2025
 Services
Services
Shared
 Correspondence to
Correspondence to
- Hyeon Jin Jeon
-
*R&D Ceneter, ROSELAB Inc, 209 Bongeunsa-ro, Gangnam-gu, Seoul 06109, Korea
**Department of Biological Engineering, Konkuk University, 120 Neungdong-ro, Gwangjin-gu, Seoul 05029, Korea - E-mail: jhjwell@roselab.co.kr
- ORCID:
0009-0003-8722-1200








 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.