- Preparation and Characterization of Inclusion Complexes Using Diamine, Poly(amic acid), and Polyimide Structures with Cyclodextrin
Jaeyeong Choi*,†
 , Minki Choi*, **, Seong Hun Choi*, Wonseong Song*, Yun Ho Kim*,†
, Minki Choi*, **, Seong Hun Choi*, Wonseong Song*, Yun Ho Kim*,†  , and Jong Chan Won*,†
, and Jong Chan Won*,† 
*Advanced Functional Polymers Research Center, Korea Research Institute of Chemical Technology (KRICT), Daejeon 34114, Korea
**Department of Chemical Engineering, Hanyang University, Seoul 04763, Korea- 사이클로덱스트린과 다이아민, 폴리아믹산 및 폴리이미드 구조를 활용한 포접복합체 제조 및 특성 분석
*한국화학연구원 고기능고분자연구센터, **한양대학교 화학공학과
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
Due to the development of communication technology, a low dielectric film for application to the industry is required. In order to study the formation and properties of inclusion complexes using representative polyimide exhibiting such low dielectric properties and cyclodextrin (CD) as a ring component, through mixing diamine used as a monomer for polyimide, polyamic acid as a polymerization precursor, and polyimide was attempted. In order to research the formation and properties of inclusion complex using CD as ring components, an inclusion complex was formed by mixing diamine used as a monomer for polyimide, polyamic acid as a polymerization precursor, and polyimide. Through FTIR spectrum analysis of the solution obtained by mixing each component and CD and dissolving it in dimethyl sulfoxide (DMSO), it was possible to confirm the wide band of 3100 to 3600 cm-1 due to the presence of many hydroxyl groups (-OH) in CD, and the stretchable vibration band of CD specific C-O-C and C-O around 1150 cm-1. In addition, using 1H NMR spectrum analysis, the inclusion complex formation could be confirmed by the chemical shift of CD in all solutions.
통신기술의 개발로 인해 산업에 적용하기 위한 저유전성 필름이 요구되고 있다. 이러한 저유전성을 나타내는 대표적인 폴리이미드와 고리성분인 cyclodextrin(CD)을 활용한 포접복합체 형성과 특성을 연구하기 위하여, 모노머로 사용되는 다이아민과 중합 전구체인 폴리아믹산, 그리고 폴리이미드와 CD와의 혼합을 통하여, 포접복합체의 형성을 시도하였다. 각 성분과 CD를 혼합하고 dimethyl sulfoxide(DMSO)에 용해시켜 얻어진 용액의 FTIR 스펙트럼 분석을 통해 CD의 많은 하이드록시기(-OH)의 존재로 인한 3100-3600 cm-1의 넓은 밴드와 1150 cm-1 부근의 CD 특유의 C-O-C 및 C-O의 신축 진동 밴드를 확인할 수 있었다. 또한, 1H NMR 스펙트럼 분석을 이용하여, 모든 용액 상에서 CD의 chemical shift를 확인하여 포접복합체의 형성을 확인할 수 있었다.
In this study, the formation and properties of inclusion complexes using representative polyimide exhibiting such low dielectric properties and cyclodextrin (CD) as a ring component, through mixing diamine used as a monomer for polyimide, polyamic acid as a polymerization precursor, and polyimide was attempted. Using 1H nuclear magnetic resonance (1H NMR) and Fourier transform infrared (FTIR) spectrum analysis, the inclusion complex formation was checked.
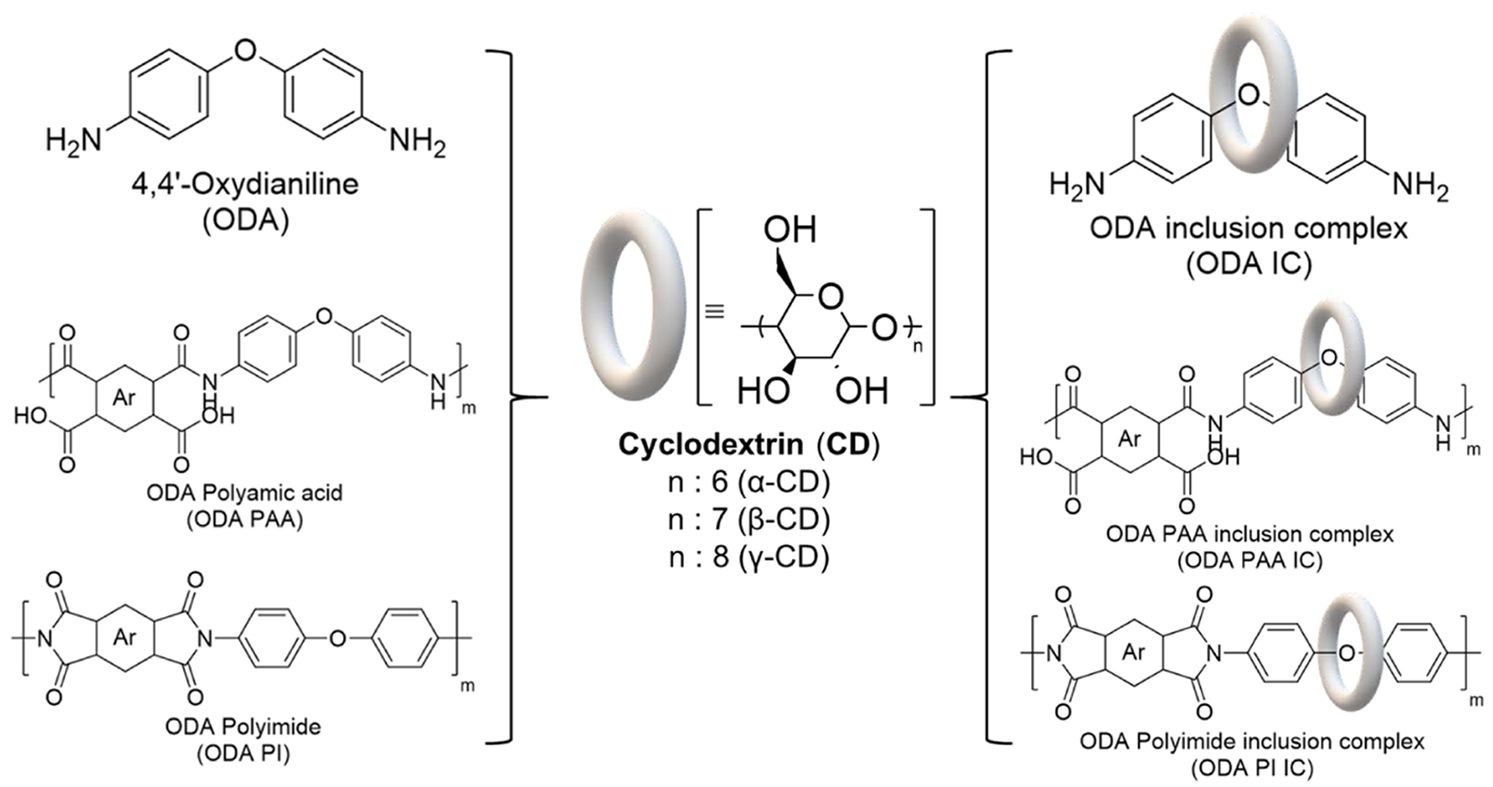
Keywords: polyimide, cyclodextrin, inclusion complex, host-guest interaction, supramolecular chemistry.
본 연구는 과학기술정보통신부 나노·소재기술개발사업(과제번호: NRF-2021M3H4A3A01045740), 산업통상자원부 소재부품기술개발사업(과제번호: KEIT-20024822), 그리고 한국화학연구원 기본사업(과제번호: KS2521-20)의 지원을 받아 수행되었으며, 이에 깊은 감사를 드립니다.
이해상충이 없음을 선언합니다.
고체상의 FTIR 데이터 및 Table 2-4에 대응하는 CD의 구조에 대한 자료는 다음 사이트에서 얻을 수 있습니다(http://journal.polymer-korea.or.kr).
PK_2026_050_02_226_Supporting_Information.pdf (920 kb)
Supplementary Information
현대사회에 이르러 통신기술의 발달로 산업에 적용하기 위한 저유전 특성이 요구되고 있다. 이러한 저유전 특성은 반도체, 5G 통신, 자동차, 항공우주 등 다양한 첨단 산업 분야에서 필수적으로 요구되고 있다.1,2 이들 산업에 적용되는 저유전 소재는 낮은 유전상수(dielectric constant; Dk)와 유전손실(dielectric loss; Df)를 갖는 동시에, 가볍고 우수한 기계적 물성을 가져야 한다.3,4
이러한 저유전을 나타내는 대표적인 소재로서 폴리이미드가 오래전부터 연구되어왔다.5,6 폴리이미드는 고분자 사슬 간의 강한 분자간 상호작용으로 인해 구조가 단단히 고정되어 분극이 어렵고, 이로 인해 일반 고분자보다 낮은 유전율을 나타낸다. 이러한 폴리이미드의 유전율을 더 낮추기 위해 다양한 연구들이 진행되어왔다. 대표적으로, 폴리이미드가 형성하는 전자이동복합체(charge transfer complex, CTC)의 형성이 Dk를 증가시키는 주요 원인 중 하나로 알려져 왔다. CTC는 주로 전자주개(donor)와 전자수용체(acceptor) 간의 강한 분자간 상호작용에 의해 형성되며, 이는 고분자 사슬 간의 정렬을 강화하고, 분극 특성을 증가시켜 결과적으로 유전상수를 높이는 방향으로 작용한다고 알려져 있다.7,8 따라서, 폴리이미드의 유전율을 낮추기 위한 연구는 주로 CTC 형성을 억제하거나, 고분자 내부에 자유 부피(free volume)를 증가시키는 전략을 중심으로 진행되어 왔다. 예를 들어, bulky한 치환기 도입,9,10 불소화 구조 설계,11,12 비선형 구조를 갖는 모노머의 사용,13,14 등의 방법이 대표적인 접근법이다. 이러한 구조적 설계는 분자 간 상호작용을 약화시키고 사슬 간 밀도를 낮춤으로써, Dk와 Df 의 감소 효과를 유도할 수 있다.
한편, 이러한 폴리이미드에 고리형 분자를 도입한 연구들이 약 10년 전부터 시도되어 왔다.15 고리 구조로서 crown-ether는 폴리이미드의 주사슬 구조에 영향을 주지 않으면서도, CTC 형성을 억제하여 유전율 저하를 유도하는 효과가 보고되어 왔다.16 최근에는 crown-ether와 유사한 고리형 구조체인 cyclodextrin (CD)을 폴리이미드에 도입하여 유전특성을 개선하려는 시도도 보고되고 있다.17 반대로, 폴리이미드와 CD를 혼합하여 혼합 필름으로 제조했을 때에는 유전율이 증가했다는 연구사례도 존재한다.18
다만, 이러한 연구들에서 사용한 CD는 상대적으로 α-나 γ-가 아닌 β-CD를 사용하고 있다. 그 이유로는 β-CD가 다른 CD들과 비교하여 상대적으로 친수성이 낮고 소수성을 나타내고, 상대적으로 기능화가 간편하며 값이 저렴하다는 장점이 있기 때문이다. 그러나 α- 및 γ-CD를 활용한 폴리이미드와의 포접복합체 inclusion complex(IC) 형성에 대한 연구는 아직 보고된 바가 드물다.
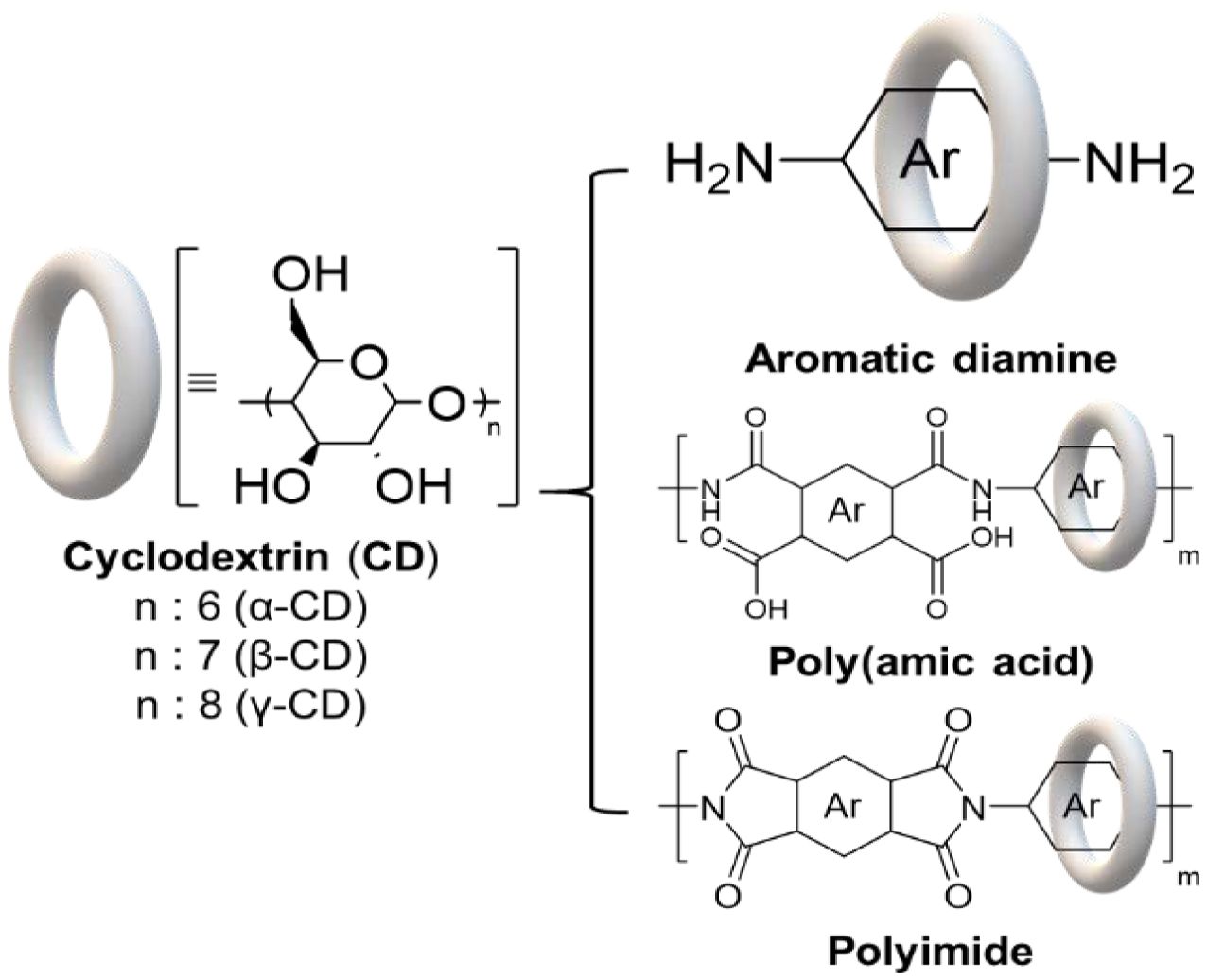
따라서 본 연구에서는 기존에 주로 사용된 β-CD뿐만 아니라, 상대적으로 연구가 부족했던 α-CD 및 γ-CD를 포함한 cyclodextrin 계열 고리 구조를 폴리이미드에 도입하여, 포접복합체 형성 가능성과 그 구조를 체계적으로 분석하고자 하였다. 이를 위해 다이아민, 폴리아믹산, 및 폴리이미드와 다양한 CD와의 혼합을 통해 새로운 초분자 포접복합체의 형성 여부를 확인하고, 그 구조를 용액상 및 고체상에서 비교하려는 것을 도식화하여 Figure 1에 나타내었다. CD가 물에 높은 용해도를 가지는 특성을 고려하여, 본 연구에서는 포접복합체 형성 및 안정성 평가를 위한 용매로서 DMSO를 사용하였다. 이는 DMSO 환경에서 축과 고리 성분이 모두 잘 용해되고, inclusion complex가 안정적으로 형성된다는 기존 문헌 보고에 기반한 것이다.19-21 아울러, DMSO 용액상에서의 혼합물과 그로부터 침전된 고체 상태를 각각 분석함으로써, 각 상태에서의 포접복합체 구조 및 상호작용 차이를 규명하고자 하였다.
|
Figure 1 Schematic illustration of this research paper. |
재료. 다이아민으로는 4,4′-oxydianiline(ODA, ³98.0%)과 고리 성분으로 사용한 a-cyclodextrin(a-CD, >98.0%), β-cyclodextrin (β-CD, >98.0%), γ-cyclodextrin(γ-CD, >99.0%)를 TCI(Japan)에서 구매하여 사용하였다. 산무수물은 4,4′-(Hexafluoroisopropylidene) diphthalic anhydride(6FDA, 99%)를 Changzhou Sunlight Pharmaceutical(China)에서 구매하여 사용하였으며, 각 성분을 혼합하거나 폴리이미드 중합에 사용된 용매로 dimethyl sulfoxide(DMSO, 99.5%)를, imidization을 위해 pyridine(99.5%)을 Daejung(Korea)에서 구매하여 사용하였다. 폴리아믹산의 중합 용매로서 N,N-dimethylacetamide(DMAc, 99%)를 사용하였고, 이미드화를 위해 acetic anhydride(99%)를, 1H NMR 분석을 위한 용매로 DMSO-d6(99.5 atom% D)를 Sigma-Aldrich (USA)에서 구매하여 사용하였다.
모든 시약은 별도의 정제 없이 이용되었다.
기기 및 분석. 구조의 확인은 1H NMR(Bruker advance 500 MHz spectrometer, Billerica, MA, USA)을 이용하여 샘플은 실온에서 DMSO-d6 용매에 용해시켜 측정하였다. FTIR spectrometer(Bruker Alpha-P)를 사용하여 분석하였다. 고분자의 분자량 측정은 RI 검출기가 장착된 젤 투과 크로마토그래피 (GPC) (Agilent 1260 Infinity II) 장치를 사용하고 50 ℃의 조건에서 0.8 mL/min의 속도로 DMAc를 이용하여 측정하였다. 실험에서 사용된 deionized water(DI water)는 water purification system(ELGA, Lane End, UK)을 이용하여 필터링을 통해 사용하였다.
합성 및 Solution 준비. ODA와 ODA Solution 준비: 4,4'-oxydianiline(ODA(1))를 고리 성분과 혼합 및 중합을 위해 용매에서 잘 용해되도록 미세한 분말로 분쇄하여 사용하였다. 분쇄한(1) (10 mg, 0.05 mmol)을 2 mL vial에 DMSO-d6 (1 mL)와 혼합하여 실온에서 약 5분간 초음파를 가해주어 투명한 ODA solution(2)을 조제하였다.
ODA(1): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62 (4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 4.77 (4H, -NH2 in ODA, s).
ODA와 CD를 혼합한 IC 제조: Scheme 1(a)에 명시된 것처럼, 20 mL vial에 (1) (1.0 g, 5.00 mmol)와 α-CD(1.0 g, 1.03 mmol)을 넣고 DMSO(10 mL)를 용매로 사용하여 실온에서 약 5분간 초음파를 가해주었다. 혼합 용액이 모두 투명하게 용해된 후, 실온에서 overnight으로 교반을 진행하였다. 반응 용액을 탈이온수(200 mL)에 넣어 침전시킨 후, 필터 과정을 통해, 고형분을 회수하고, 진공오븐에서 60 ℃, overnight으로 건조하여 ODA α-IC(3)를 얻었다. ODA β-IC (4)와 ODA γ-IC(5)의 경우에도 동일한 과정으로 진행하여 수득하였다.
ODA α-IC(3): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62(4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 4.77(4H, -NH2 in ODA, s).
ODA β-IC(4): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62(4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 4.77(4H, -NH2 in ODA, s).
ODA γ-IC(5): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62(4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 4.77(4H, -NH2 in ODA, s).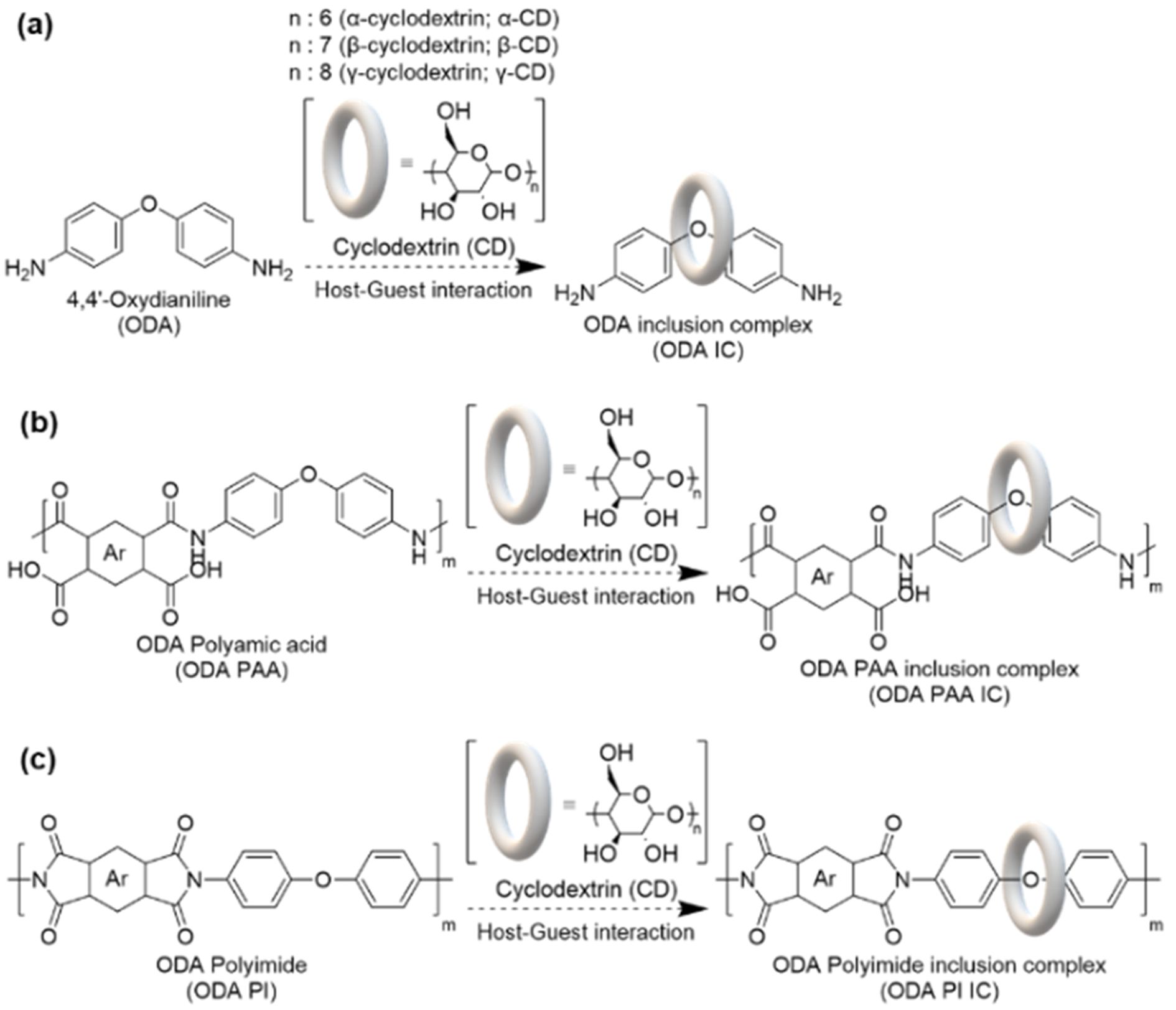
Scheme 1. Preparation of inclusion complex using CD with ODA: (a) PAA; (b) and PI (c)
ODA와 CD를 혼합한 IC Solution 준비: 2 mL vial에 (1) (10 mg, 0.05 mmol)와 a-CD(10 mg, 0.01 mmol)을 넣고 DMSO-d6 (1 mL)와 혼합하여 실온에서 약 5분간 초음파를 가해주어 투명한 IC solution(6-8)을 조제하였다.
ODA a-IC solution(6): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62(4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 5.51-5.50(6H, CD-OH(2-position-OH), d), 5.44-5.43(6H, CD-OH(3-position-OH), d), 4.82-4.81(6H, CD-H(1-position-H), d), 4.76(4H, -NH2 in ODA, s), 4.48-4.45(6H, CD-OH(6-position-OH), t), 3.81-3.77(6H, CD-H(3-position-H), m), 3.71-3.58(18H, CD-CH2(6-position-H), CD-CH(5-position-H), m), 3.42-3.38 (6H, CD-CH(4-position-H), t), 3.31-3.27(6H, CD-CH(2-position-H), m).
ODA β-IC solution(7): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62(4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 5.71-5.70(7H, CD-OH(2-position-OH), d), 5.67-5.66 (7H, CD-OH(3-position-OH), d), 4.85-4.84(7H, CD-H(1-position-H), d), 4.78(4H, -NH2 in ODA, s), 4.44-4.42(7H, CD-OH(6-position-OH), t), 3.70-3.61(21H, CD-CH2(6-position-H), CD-CH(3-position-H), m), 3.59-3.56(7H, CD-CH(5-position-H), m), 3.38-3.35(7H, CD-CH(4-position-H), t), 3.32-3.30(7H, CD-CH(2-position-H), m).
ODA γ-IC solution(8): 1H NMR(500 MHz, r.t., DMSO-d6) δH 6.65-6.62(4H, Ar-H in ODA, m), 6.54-6.51(4H, Ar-H in ODA, m), 5.76-5.75(8H, CD-OH(2-position-OH), d), 5.73-5.72(8H, CD-OH(3-position-OH), d), 4.90(8H, CD-H(1-position-H), d), 4.76(4H, -NH2 in ODA, s), 4.52-4.49(8H, CD-OH(6-position-OH), t), 3.65-3.59(24H, CD-CH2(6-position-H), CD-CH(3-position-H), m), 3.57-3.53(8H, CD-CH (5-position-H), m), 3.38-3.35(8H, CD-CH(4-position-H), t), 3.35-3.31(8H, CD-CH (2-position-H), m).
ODA-6FDA PAA 중합과 Solution 준비: Scheme 2(a)에서,125 mL vial에 ODA(6.00 g, 30.0 mmol)와 6FDA(13.33 g, 30.0 mmol)를 혼합하고 DMSO(100 mL)를 용매로 사용하여 실온에서 overnight으로 중합을 진행하였다. 반응 용액에 acetic anhydride(8.51 mL, 90.0 mmol)와 pyridine(7.25 mL, 90.0 mmol)을 넣어주고, 70 ℃에서 24시간 반응으로 이미드화를 진행하였다. 반응 용액은 탈이온수(800 mL)에 침전을 진행하고 교반을 진행하여 세척을 진행하였다. 필터 과정을 통해, 얻어진 고형분은 진공오븐에서 60 ℃, overnight으로 건조하였다.
얻어진 (9) (10 mg)을 2 mL vial에 DMSO-d6(1 mL)와 혼합하여 실온에서 약 5분간 초음파와 열을 가해주어 투명한 ODA-6FDA PAA solution(10)을 조제하였다.
ODA-6FDA PAA(9): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.42-10.85(1H, -COOH, s), 10.58-10.38(1H, -CONH-, m), 8.20-6.69(14H, Ar-H).
PAA와 CD를 혼합한 IC 조제: Scheme 1(b)에 명시된 것처럼, 20 mL vial에 (9) (1.0 g)와 α-CD(1.0 g, 1.028 mmol)을 넣고 DMSO(10 mL)를 용매로 사용하여 실온에서 약 5분간 초음파를 가해주었다. 혼합 용액이 모두 투명하게 용해된 후, 실온에서 overnight으로 교반을 진행하였다. 반응 용액은 탈이온수(200 mL)에 반응 용액은 탈이온수(200 mL)로 침전과 필터 과정을 통해, 고형분을 회수하고, 진공오븐에서 60 ℃, overnight으로 건조하여 PAA α-IC(11)을 얻었다. 위와 동일한 방법으로, PAA β-IC(12)와 PAA γ-IC(13)를 얻었다.
PAA α-IC(11): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.64 -10.81(2H, -COOH, s), 10.57-10.37(2H, -CONH-, m), 8.20-6.69(14H, Ar-H), 5.46(12H, CD-OH(2,3-position-OH), s), 4.81 (6H, CD-H(1-position-H),d), 4.48(6H, CD-OH(6-position-OH), s), 3.81-3.08(36H, CD-H(2,3,4 and 5 position-H)).
PAA β-IC(12): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.62-10.79(2H, -COOH, s), 10.57-10.37(2H, -CONH-, m), 8.20- 6.69(14H, Ar-H), 5.68(14H, CD-OH(2,3-position-OH), s), 4.85 (7H, CD-H(1-position-H),d), 4.43(7H, CD-OH(6-position-OH), s), 3.67-3.08(42H, CD-H(2,3,4 and 5 position-H)).
PAA γ-IC(13): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.73-10.75(2H, -COOH, s), 10.57-10.37(2H, -CONH-, m), 8.20-6.69 (14H, Ar-H), 5.73(16H, CD-OH(2,3-position-OH), s), 4.90(8H, CD-H(1-position-H),d), 4.50(8H, CD-OH(6-position-OH), s), 3.65-3.08(48H, CD-H(2,3,4 and 5 position-H)).
PAA와 CD를 혼합한 IC Solution 준비: 2 mL vial에 (9) (10 mg, 0.05 mmol)와 α-CD(10 mg, 0.01 mmol)을 넣고 DMSO-d6(1 mL)와 혼합하여 실온에서 약 5분간 초음파와 열을 가해주어 투명한 IC solution(14-16)을 조제하였다.
PAA α-IC solution(14): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.67-11.26(1H, -COOH, s), 10.58-10.37(1H, -CONH-, m), 8.18-6.69(14H, Ar-H), 5.49-5.44(12H, CD-OH(2,3-position-OH), d), 4.81(6H, CD-H(1-position-H),d), 4.46(6H, CD-OH (6-position-OH), s), 3.80-3.28(36H, CD-H(2,3,4 and 5 position-H)).
PAA β-IC solution(15): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.75-10.76(2H, -COOH, s), 10.58-10.38 2H, -CONH-, m), 8.20-6.69(14H, Ar-H), 5.68(14H, CD-OH(2, 3-position-OH), s), 4.85-4.84(7H, CD-H(1-position-H),d), 4.43(7H, CD-OH (6-position-OH), s), 3.69-3.30(42H, CD-H(2,3,4 and 5 position-H)).
PAA γ-IC solution(16): 1H NMR(500 MHz, r.t., DMSO-d6) δH 12.82-10.81(2H, -COOH, s), 10.58-10.37(1H, -CONH-, m), 8.18-6.68(14H, Ar-H), 5.74(16H, CD-OH(2,3-position-OH), s), 4.90-4.89(8H, CD-H(1-position-H),d), 4.50(8H, CD-OH(6-position-OH), s), 3.66-3.31(48H, CD-H(2,3,4 and 5 position-H)).
PI 중합과 Solution의 준비: 70 mL vial에 ODA(6.00 g, 30.0 mmol)와 6FDA(13.32 g, 30.0 mmol)를 혼합하고 DMSO (100 mL)를 용매로 사용하여 실온에서 overnight으로 중합을 진행하였다. 반응 용액에 acetic anhydride(8.51 mL, 90 mmol)와 pyridine(7.25 mL, 90 mmol)을 넣어주고, 70 ℃, 24시간 반응으로 이미드화를 진행하였다. 반응 용액은 탈이온수(1,000 mL)에 침전을 진행하고 세척을 진행하였다. 필터 과정을 통해, 얻어진 고형분은 진공오븐에서 60 ℃, overnight으로 건조하여 ODA-6FDA PI(17)를 얻었다. 얻어진 (17) (10 mg)을 2 mL vial에 DMSO-d6(1 mL)와 혼합하여 실온에서 약 30분간 초음파와 열을 가해주어 투명한 ODA-6FDA PI solution(18)을 조제하였다.
ODA-6FDA PI(17): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.20-8.19(2H, Ar-H in 6FDA, d), 7.98-7.96(2H, Ar-H in 6FDA, d), 7.77(2H, Ar-H in 6FDA, s), 7.52-7.50(4H, Ar-H in ODA, d), 7.26-7.24(4H, Ar-H in ODA, d).
PI와 CD를 혼합한 IC 조제: Scheme 1(c)에 명시된 것처럼, 20 mL vial에 (17) (1.0 g)을 넣고 DMSO(10 mL)를 용매로 사용하여 실온에서 약 30분간 초음파와 열을 가해주었다. 용액이 모두 투명하게 용해된 후, α-CD(1.0 g, 1.028 mmol)를 첨가하고, 실온에서 overnight으로 교반을 진행하였다. 반응 용액은 탈이온수(200 mL)로 침전과 필터 과정을 통해, 고형분을 회수하고, 진공오븐에서 60 ℃, overnight으로 건조하여 PI α-IC(19)을 얻었다. 위와 동일한 방법으로, PI β-IC(20)와 PI γ-IC(21)를 수득하였다.
PI α-IC(19): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.20-8.19 (2H, Ar-H in 6FDA, d), 7.98(2H, Ar-H in 6FDA, d), 7.78 (2H, Ar-H in 6FDA, s), 7.52-7.50(4H, Ar-H in ODA, d), 7.26-7.25 (4H, Ar-H in ODA, d), 5.49-5.45(12H, CD-OH(2, 3-position-OH), s), 4.82(6H, CD-H(1-position-H), d), 4.48(6H, CD-OH(6-position-OH), s), 3.80-3.09(36H, CD-H(2,3,4 and 5 position-H)).
PI β-IC(20): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.20- 8.18(2H, Ar-H in 6FDA, d), 7.97(2H, Ar-H in 6FDA, d), 7.77 (2H, Ar-H in 6FDA, s), 7.51-7.49(4H, Ar-H in ODA, d), 7.26-7.24(4H, Ar-H in ODA, d), 5.68(14H, CD-OH(2,3-position-OH), s), 4.85-4.84(7H, CD-H(1-position-H), d), 4.42(7H, CD-OH(6-position-OH), s), 3.70-3.09(42H, CD-H(2,3,4 and 5 position-H)).
PI γ-IC(21): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.20- 8.18(2H, Ar-H in 6FDA, d), 7.97-7.96(2H, Ar-H in 6FDA, d), 7.77(2H, Ar-H in 6FDA, s), 7.51-7.50(4H, Ar-H in ODA, d), 7.26-7.24(4H, Ar-H in ODA, d), 5.73(16H, CD-OH(2,3-position-OH), s), 4.90(8H, CD-H(1-position-H), d), 4.50(8H, CD-OH (6-position-OH), s), 3.65-3.09(48H, CD-H(2,3,4 and 5 position-H)).
PI와 CD를 혼합한 IC Solution 준비: 2 mL vial에 (17) (10 mg, 0.05 mmol)를 넣고 DMSO-d6(1 mL)와 혼합하여 실온에서 약 30분간 초음파와 열을 가해주어 투명한 용액을 제조하고, α-CD(10 mg, 0.01 mmol)를 첨가하여 다시 약 5분간 초음파를 가해주어 투명한 IC solution(22-24)을 조제하였다.
PI α-IC solution(22): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.19-8.18(2H, Ar-H in 6FDA, d), 7.97-7.96(2H, Ar-H in 6FDA, d), 7.76(2H, Ar-H in 6FDA, s), 7.51-7.49(4H, Ar-H in ODA, d), 7.26-7.23(4H, Ar-H in ODA, d), 5.51-5.43(12H, CD-OH(2,3-position-OH), d), 4.81(6H, CD-H(1-position-H), d), 4.46(6H, CD-OH(6-position-OH), s), 3.80-3.28(36H, CD-H (2,3,4 and 5 position-H)).
PI β-IC solution(23): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.19-8.18(2H, Ar-H in 6FDA, d), 7.97-7.96(2H, Ar-H in 6FDA, d), 7.76(2H, Ar-H in 6FDA, s), 7.51-7.49(4H, Ar-H in ODA, d), 7.26-7.23(4H, Ar-H in ODA, d), 5.70-5.66(14H, CD-OH(2, 3-position-OH), d), 4.84(7H, CD-H(1-position-H), d), 4.43(7H, CD-OH(6-position-OH), s), 3.69-3.30(42H, CD-H (2,3,4 and 5 position-H)).
PI γ-IC solution(24): 1H NMR(500 MHz, r.t., DMSO-d6) δH 8.19-8.18(2H, Ar-H in 6FDA, d), 7.97-7.96(2H, Ar-H in 6FDA, d), 7.77(2H, Ar-H in 6FDA, s), 7.51-7.49(4H, Ar-H in ODA, d), 7.25-7.23(4H, Ar-H in ODA, d), 5.75-5.72(16H, CD-OH(2,3-position-OH), s), 4.90(8H, CD-H(1-position-H), d), 4.51(8H, CD-OH(6-position-OH), s), 3.65-3.35(48H, CD-H (2,3,4 and 5 position-H)).
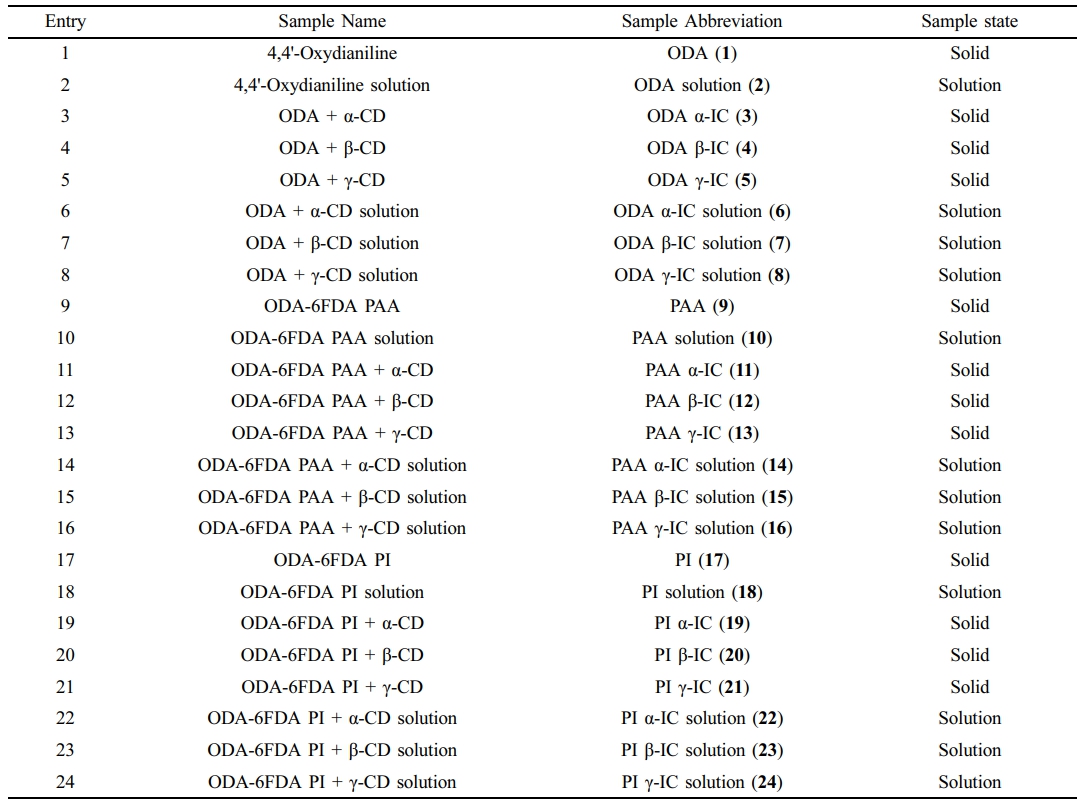
고분자의 중합 과정과 IC의 형성을 통해 얻어진 샘플들의 정보를 Table 1에 정리하였다. 모든 고체 샘플들은 60 ℃에서 overnight으로 건조하였고, solution 샘플은 DMSO에 용해된 상태이다.
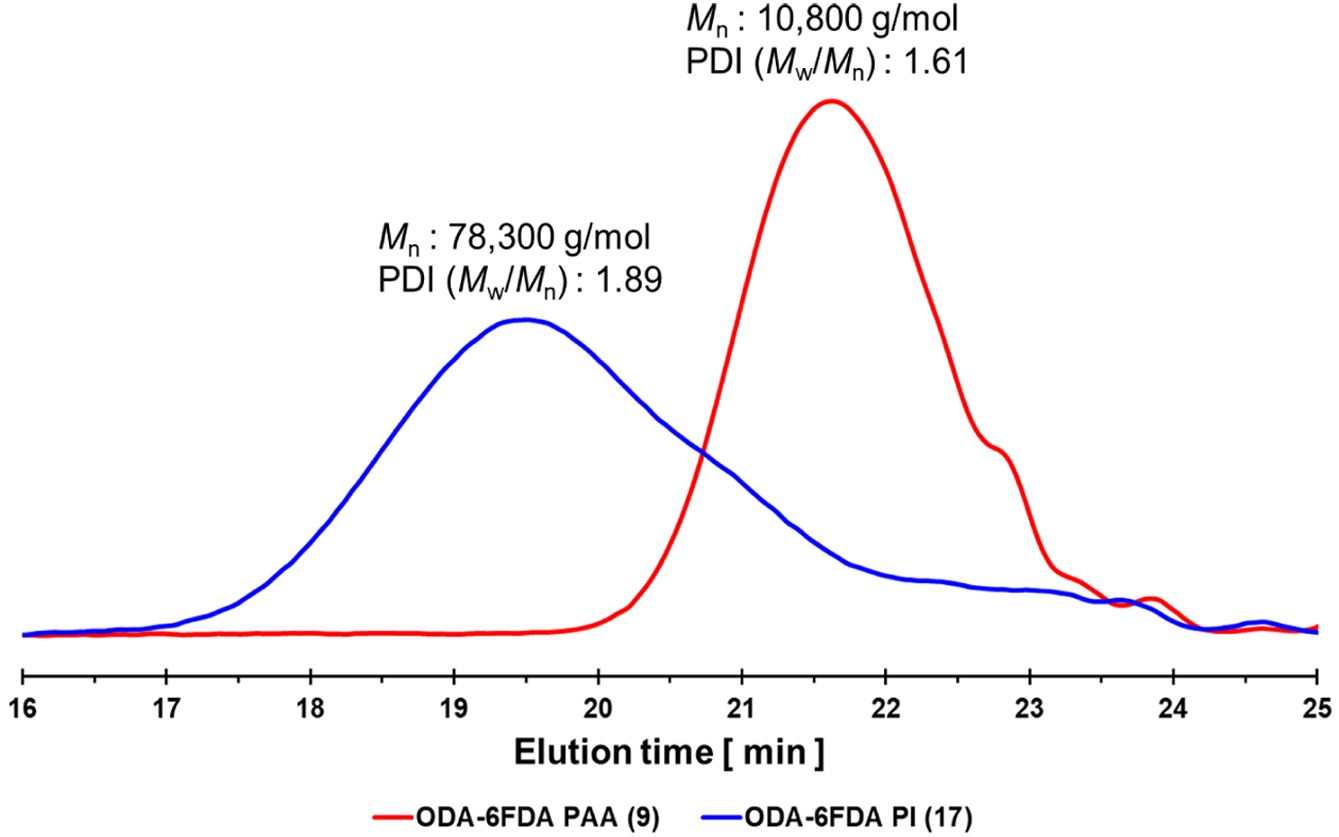
이렇게 다양한 샘플들 중에서 먼저, 폴리아믹산과 화학적 이미드화로 얻어진 폴리이미드의 분자량 분석을 위해 DMAc 용리액을 사용하여 GPC 측정을 진행하여 Figure 2에 나타내었다. 폴리아믹산의 분자량(Mn)은 10800 g/mol이고 다분산지수 polydispersity index((PDI), Mw/Mn)는 1.61로 확인되었다. 폴리이미드의 경우, Mn은 78300 g/mol로 측정되었으며, 1.89의 PDI로 더 넓은 분자량 분포를 나타냈다. 폴리아믹산과 폴리이미드의 GPC 측정 결과에서 큰 분자량 차이를 확인할 수 있었다. 이러한 이유로는 먼저, 폴리아믹산은 DMAc를 용매로 이용하여 중합하였고, 폴리이미드는 DMSO를 용매로 중합하여 화학적 이미드화를 바로 진행하였다. 다른 용매의 조건이기도 하지만, 상대적으로 유연한 고분자 사슬을 나타내는 폴리아믹산과 상대적으로 덜 유연한 고분자 사슬인 폴리이미드의 차이로 인해, 상대적으로 GPC 용매로 사용한 DMAc에도 폴리아믹산은 비교적 쉽게 용해되었으나, 폴리이미드는 초음파와 열을 주어도 잘 용해되지 않았다. 이러한 차이는 앞서 설명한 것처럼, 폴리아믹산은 아미드(–CONH–)와 카르복실산(–COOH)의 부분을 갖고 있기 때문에, 수소결합이 가능하고, 자유롭게 회전이 가능한 사슬의 운동성을 나타낸다. 반면, 폴리이미드는 이미드결합의 구조로 인해, 분자간의 회전이 어려워지고, 분자 간의 정렬성이 더 높아지게 된다. 결과적으로 분자량이 큰 폴리이미드의 경우, CD가 상대적으로 포접복합체를 형성하기 어려울 것처럼 보이지만, 소수성 물질과 Host-Guest 상호작용을 형성하는 CD의 입장에선, 포접복합체를 형성하기 쉬울 수 있다. 반면에, 폴리아믹산은 분자량이 상대적으로 작고, 분자간의 회전 등, 포접복합체를 형성하기 더 쉬울 것으로 예상할 수 있지만, 오히려 수소결합을 형성하기 때문에, CD와의 포접복합체를 형성하는데 방해물로 작용할 수 있다. 결과적으로 고분자 사슬의 분자량과 소수성의 관점에서는 폴리아믹산과 폴리이미드가 서로 대조적인 위치에 있으므로, 분자량 측정보다는 다른 구조적인 분석을 진행하는 것이 포접복합체 형성 여부를 판별하는데 더 도움이 될 것으로 판단했다.
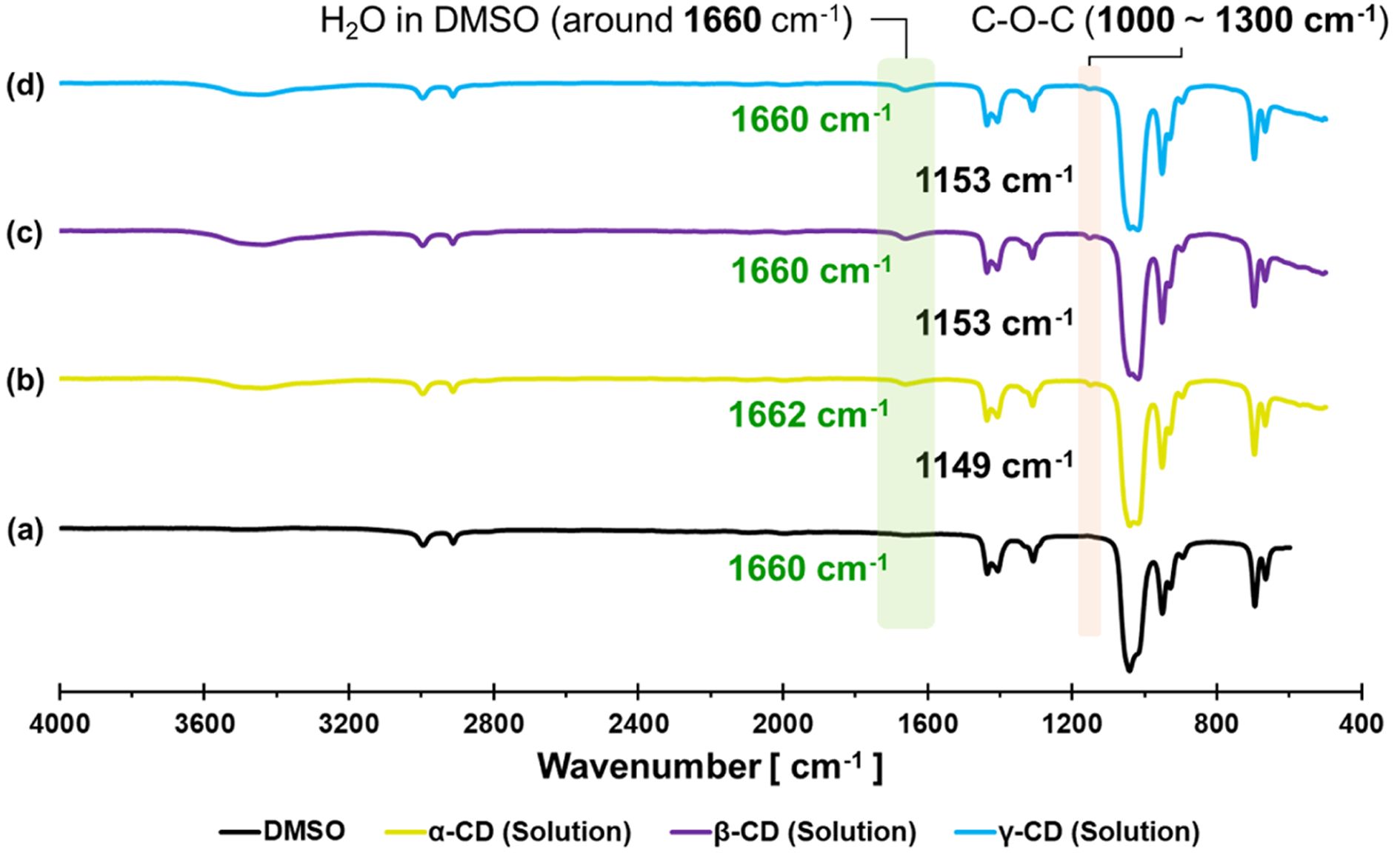
다음으로 각 샘플들을 이용해서 FTIR 스펙트럼을 분석하였다. 먼저 Figure 3에서, 용매로 사용한 DMSO와 다이아민을 넣지 않은 CD를 DMSO에 용해시킨 CD solution을 함께 분석하였다. 이 분석을 통해 DMSO에는 존재하는 않는 1150 cm-1 부근의 피크를 확인할 수 있었다. 이는 CD가 보유하고 있는 많은 ether(C-O-C)의 비대칭 stretch와 alcohol(C-O-H)의 부분으로 생각할 수 있다. 보통 alcohol의 부분은 1020 cm-1에 나타나므로, 이 피크의 대부분은 ether 결합으로 인한 부분으로 생각할 수 있다. 또한, 1660 cm-1의 부분은 DMSO에 포함된 수분의 피크로 알려져 있다. CD는 고체 상태에서도 공기 중의 수분을 흡수하는 것으로 알려져 있다.22 이 부분은 DMSO의 경우에는 매우 작은 피크를 나타내지만, CD를 용해한 경우, CD가 가지고 있는 수분의 함량으로 이 부분의 피크가 증가하는 것을 확인할 수 있었다.
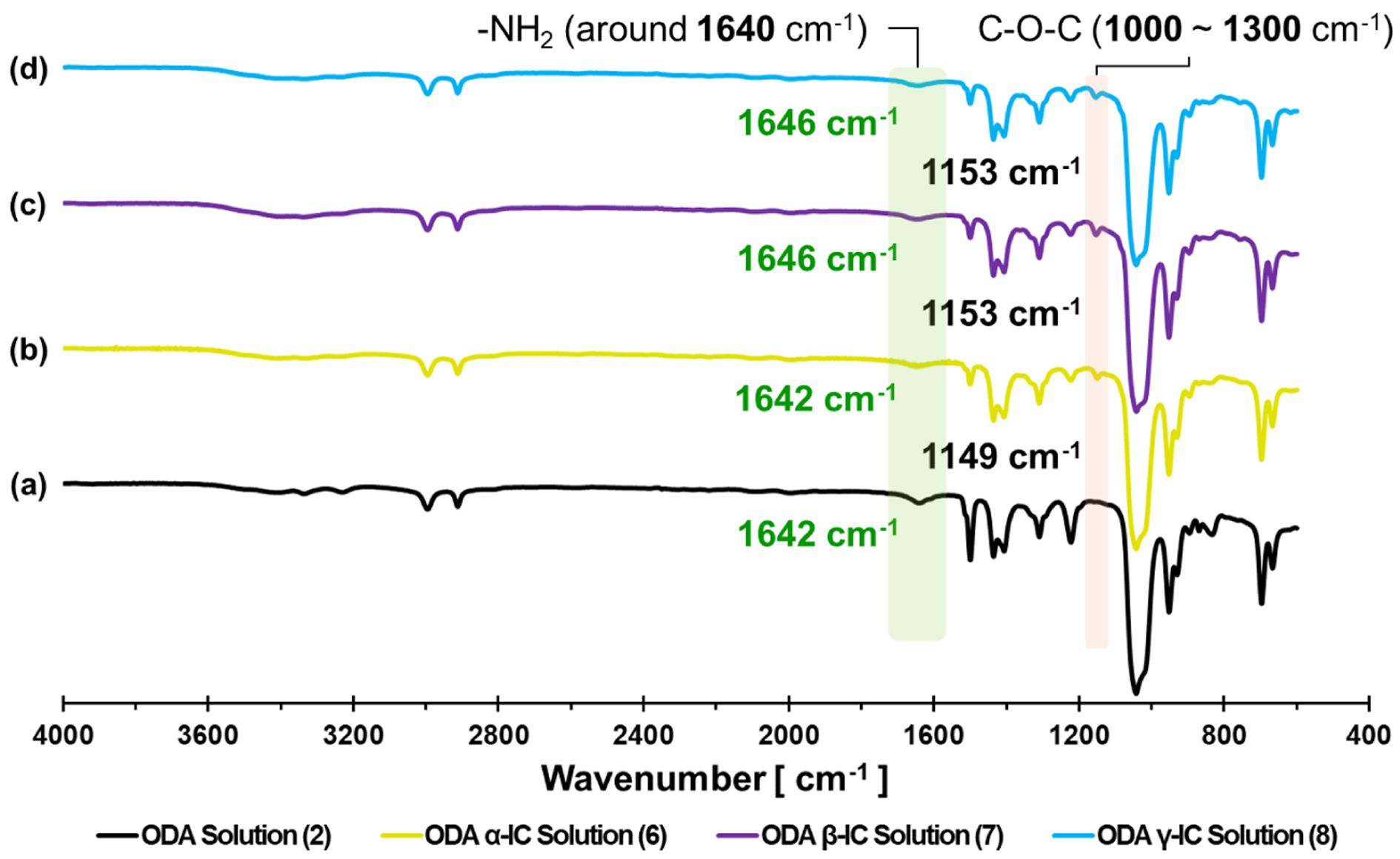
이어서, 다이아민인 ODA와 CD를 혼합한 샘플들을 DMSO에 용해시켜 분석하였다. Figure 4에서 모든 샘플들은 1640 cm-1 부근의 피크를 확인할 수 있었다. 이 부분은 ODA에 존재하는 방향족 primary amine(-NH2)의 밴드를 나타내고 있다. 또한, ODA에는 존재하지는 않지만, CD에는 존재하는 1150 cm-1 부근의 피크를 확인할 수 있었다.
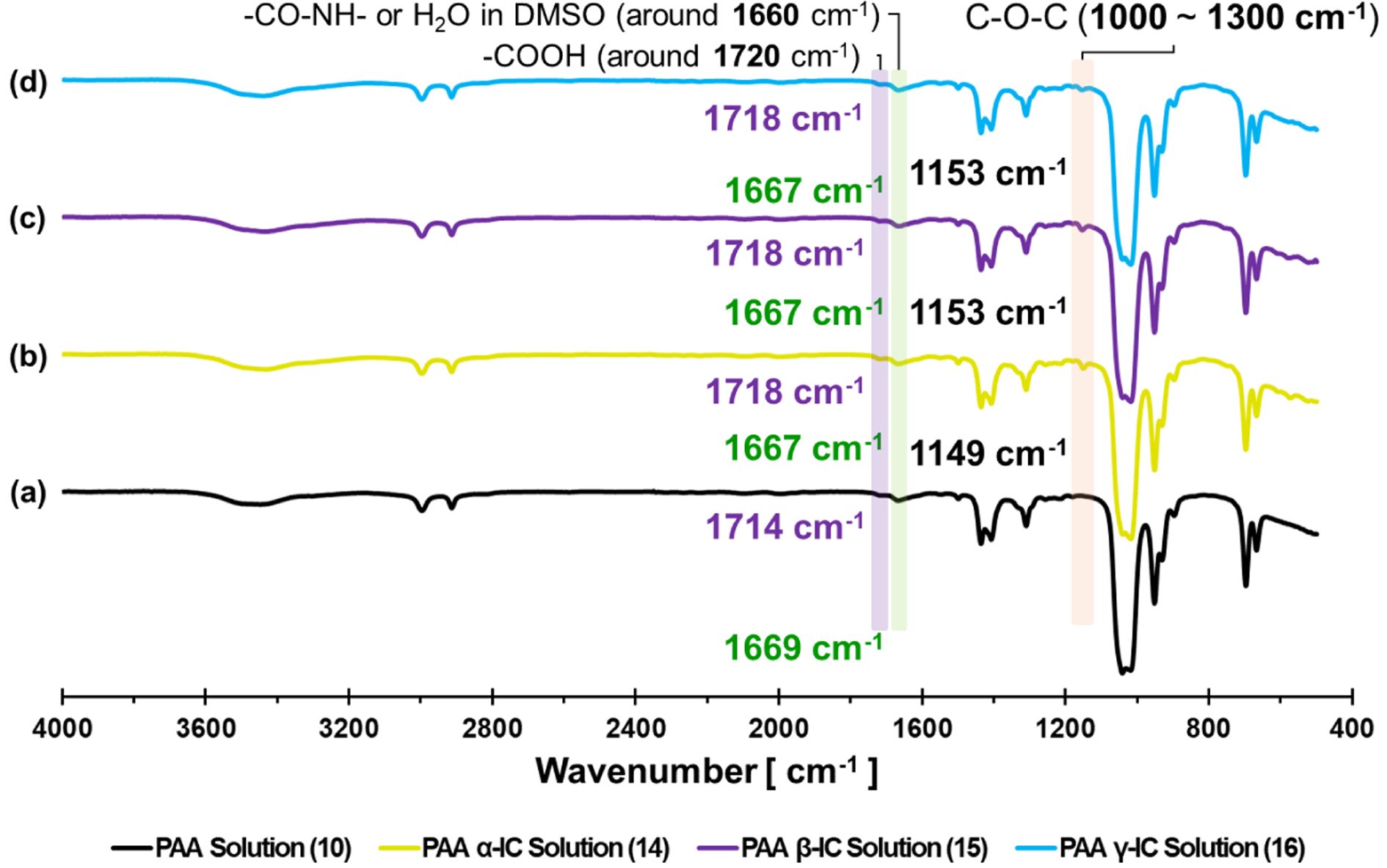
다음으로는, 폴리아믹산과 CD를 혼합한 샘플들을 ODA와 마찬가지로 DMSO에 용해시켜 분석하였다. Figure 5에서 모든 샘플들은 1720과 1660 cm-1 주변의 피크를 확인할 수 있었다. 1720 cm-1는 폴리아믹산이 가지고 있는 카르복실산(-COOH)의 카르보닐기(C=O)에 의한 신축 밴드로 생각할 수 있고, 1660 cm-1은 폴리아믹산의 아미드결합(-CO-NH-) 부분 또는 DMSO에 포함되어 있는 수분으로 생각할 수 있다. 또한, ODA의 경우와 마찬가지로, CD에는 존재하는 1150 cm-1 부근의 피크를 확인할 수 있었다.
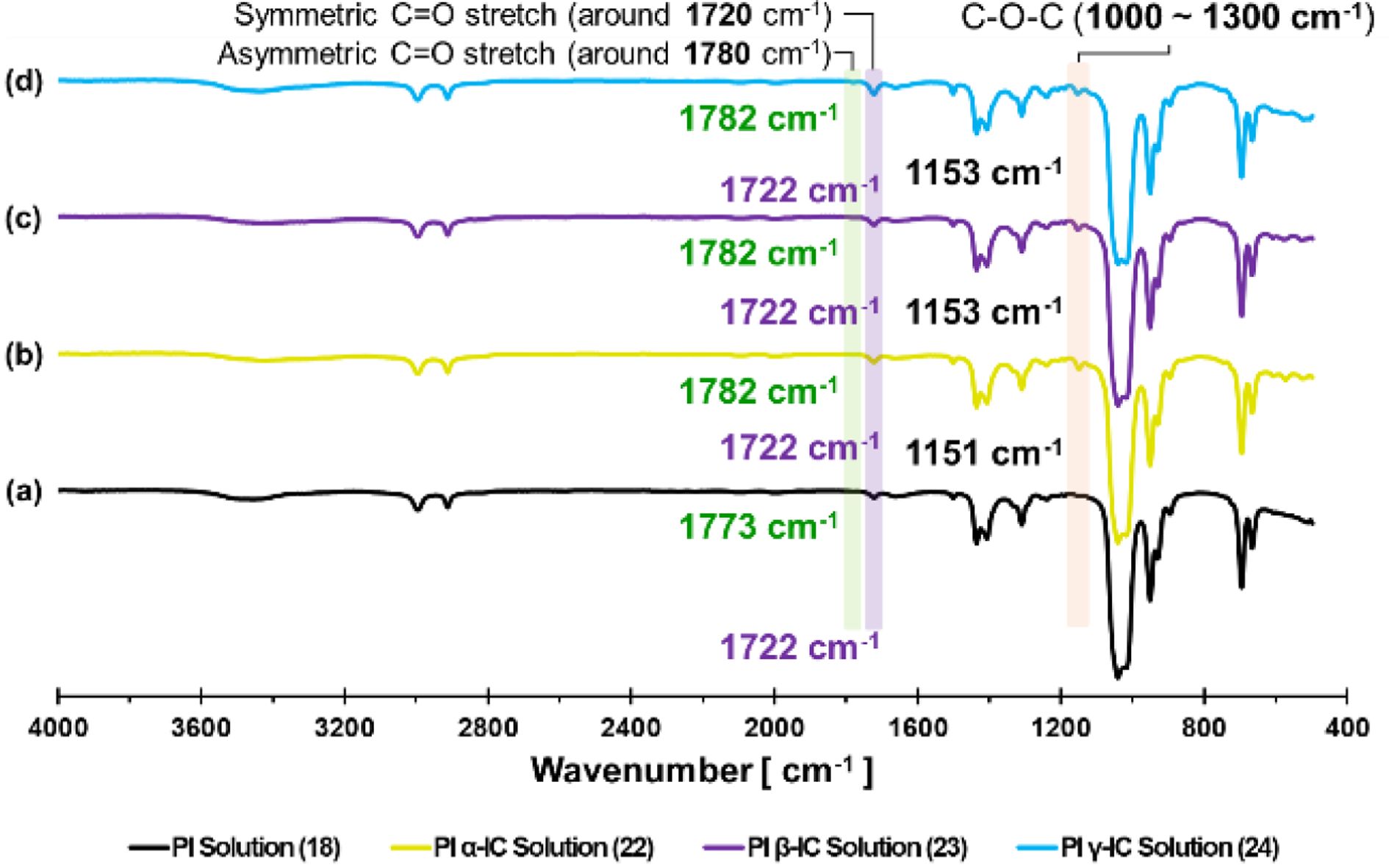
동일하게 폴리이미드와 CD를 혼합한 샘플들도 같은 조건으로 분석하였다. Figure 6에서 모든 샘플들에서 1780과 1720 cm-1 주변의 피크를 확인할 수 있었다. 1780 cm-1의 피크는 폴리아믹산이 가지고 있는 카르복실산의 피크와 같이 이미드결합에 포함된 카르보닐기(C=O)에 의한 비대칭 신축 진동으로, 1720 cm-1는 카르보닐기(C=O)의 대칭 신축 진동으로 생각할 수 있다. 용액상에서는 1780 cm-1의 피크가 작게 확인되었으나 추가정보의 Figure S4에서는 고체상에서의 피크를 자세하게 확인할 수 있다. 또한 각 성분들의 FTIR 밴드 이동에 대해 정리한 표를 추가정보에서 확인할 수 있다(Table S1-S3).
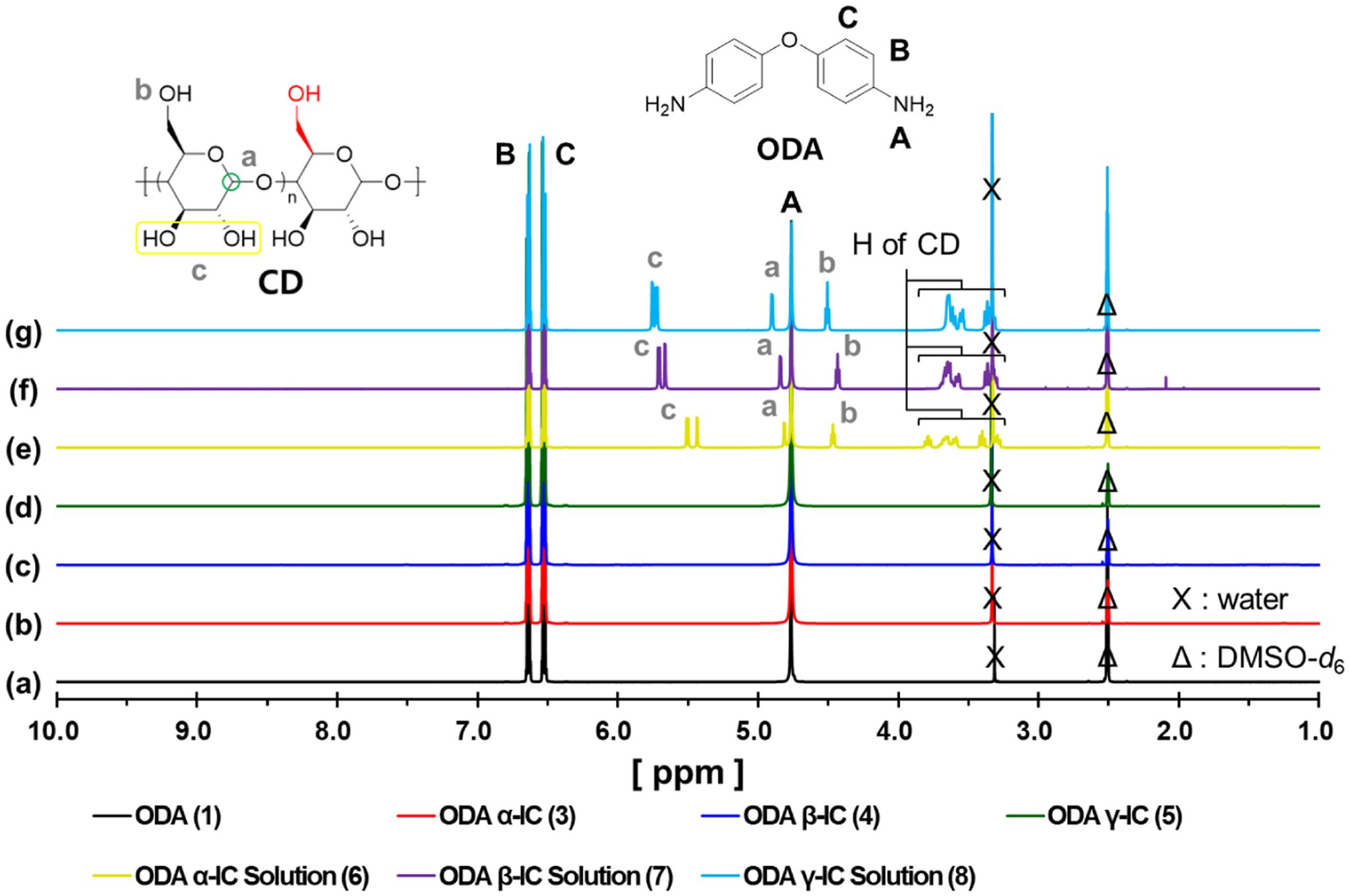
이어서, 1H NMR을 이용하여 각 고체상과 용액상의 샘플들을 분석하였다. 먼저, Figure 7에서, 다이아민인 ODA와 IC의 고체상에서는 CD의 피크를 확인할 수 없었다. 반대로, 용액상에서는 CD의 피크를 확인할 수 있었고, CD가 가진 H의 chemical shift를 확인할 수 있었다. 이를 통해, DMSO와 함께 혼합된 용액에서는 IC를 형성하지만, 여기서 물을 첨가하여 침전을 유도하게 되면, 친수성이 높은 CD는 IC 구조에서 이탈하여 물로 녹아들어가지만, ODA는 물에 녹지 않기 때문에, 그대로 회수되었다고 생각할 수 있다.
Figure 7에서 chemical shift가 있는 용액상의 샘플을 기존의 CD가 가진 H의 1H NMR과 비교하여 chemical shift의 차이를 Table 2에 표현하였다. α-와 β-CD에서는 chemical shift를 확연히 확인할 수 있었지만, γ-CD의 경우, 2가지 다른 CD에 비해 작은 값을 나타내었다. 이러한 이유는 γ-CD는 α-와 β-CD와 비교하여 내부의 공간이 더 큰 크기를 가지고 있기 때문에, 상대적으로 ODA가 IC를 형성하거나 이탈하는 것이 다른 CD들과 비교하여 더 자유로울 수 있다.23,24
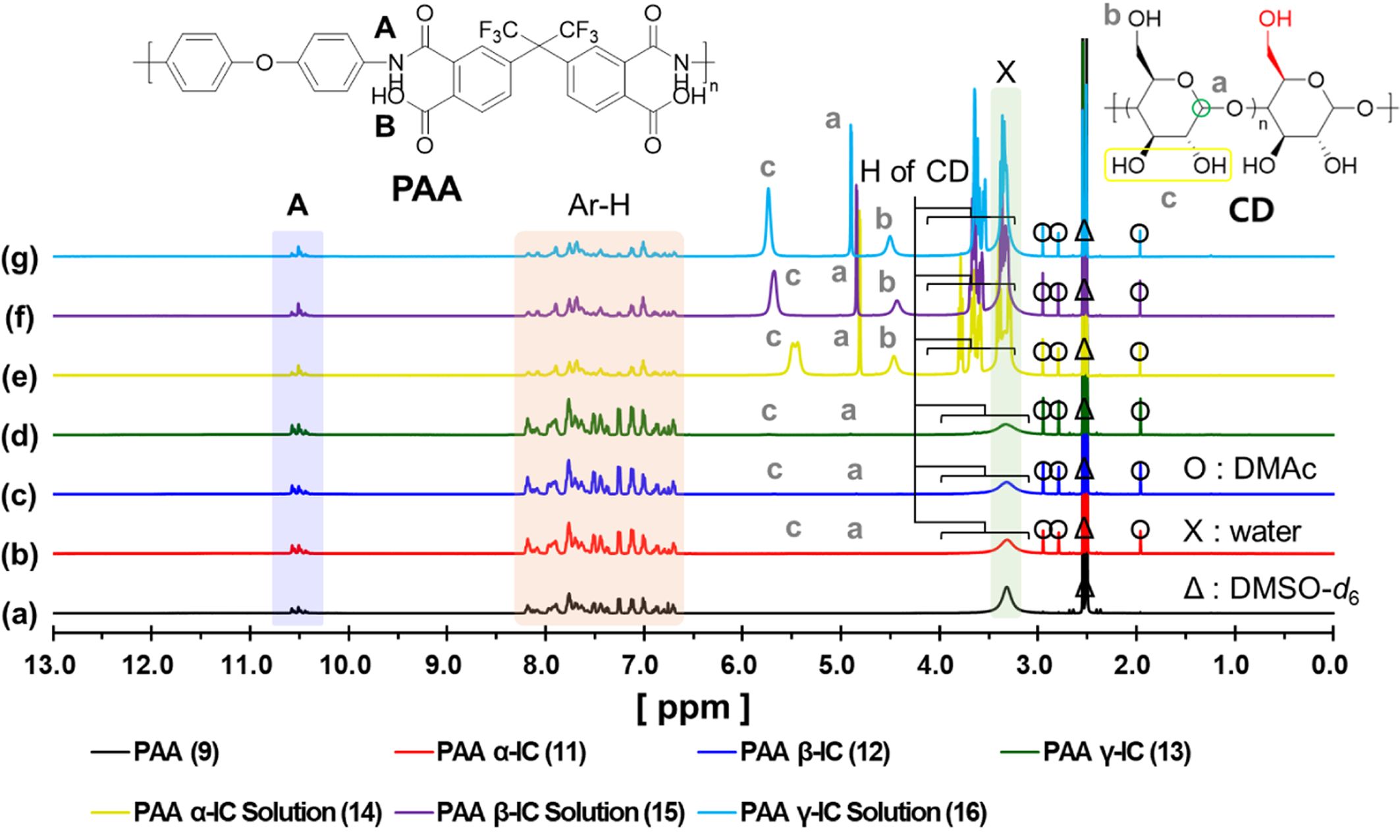
다음으로, Figure 8에서 폴리아믹산과 IC 샘플들의 NMR을 비교하였다. ODA와는 다르게 아주 조금이지만, 고체상에서도 CD의 피크를 확인할 수 있었다. 이는, 분자량이 짧은 다이아민보다 분자량이 긴 고분자 사슬에 포접된 CD가 물의 첨가로 침전되면서 이탈하지 못한 CD의 존재로 생각할 수 있다. 또한, 고체상태에서도 용액상과 동일한 chemical shift를 나타냈기에, 포접복합체로서 생각할 수 있다.
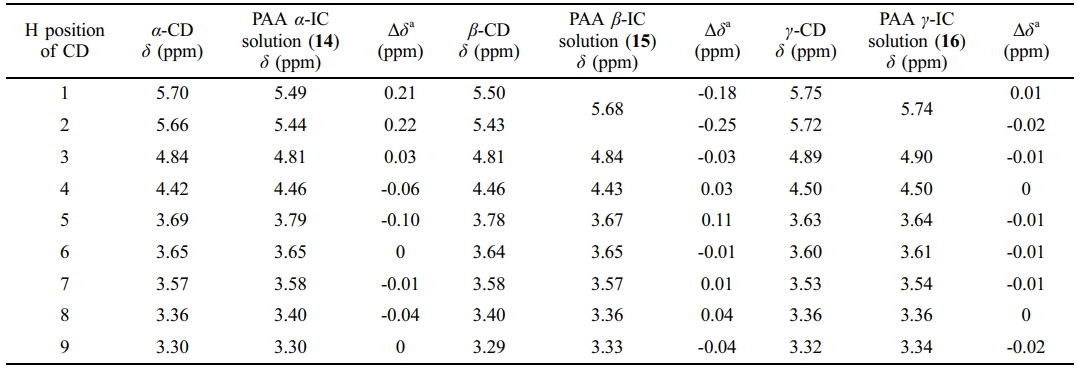
다이아민의 경우와 마찬가지로 Table 3에 chemical shift를 용액상의 샘플을 free CD의 H과 비교하여 차이를 나타내었다. 이러한 chemical shift의 차이는 앞서 ODA의 경우와 유사하게 나타난다. g-CD의 경우, 폴리아믹산에서도 큰 차이를 나타내지 않았는데, 이 또한 ODA에서의 경우와 같은 이유로 설명할 수 있다.
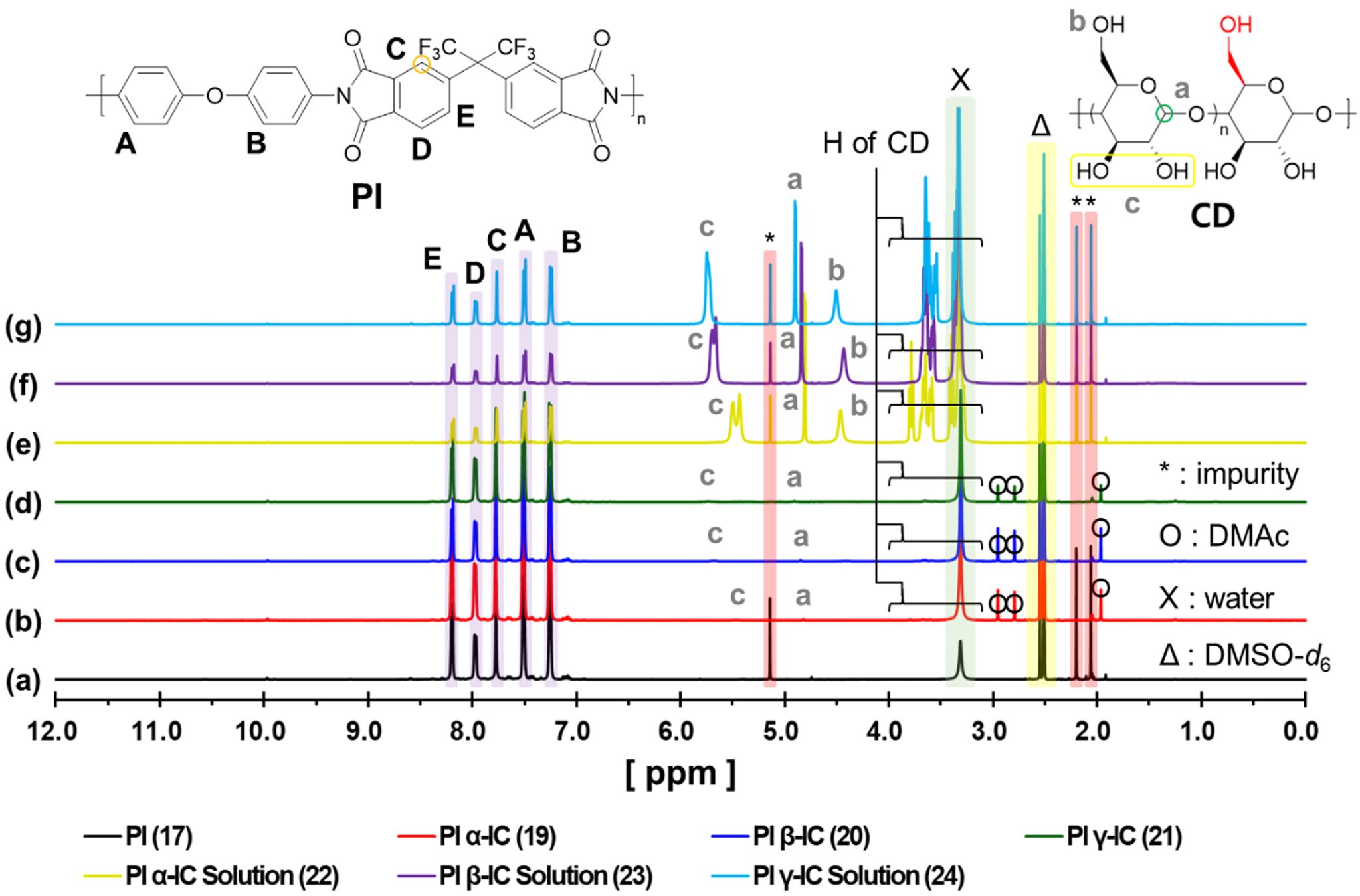
마지막으로 Figure 9에서 폴리이미드와 그를 사용한 IC 샘플들의 1H NMR 분석을 진행하였다. 폴리아믹산과 유사하게 용액상뿐만 아니라 고체상에서도 CD의 피크를 확인할 수 있었다. GPC 분석을 통해 확인된 폴리이미드의 분자량이 폴리아믹산보다 더 크기 때문에 고분자 사슬에 포접된 CD가 물의 첨가로 침전되면서 이탈하지 못한 CD의 존재로 생각할 수 있다. 또한, 상대적으로 PDI가 넓어짐에 따라, 분자량이 낮은 고분자 사슬에 포접되어 있을 가능성도 존재한다고 볼 수 있다.
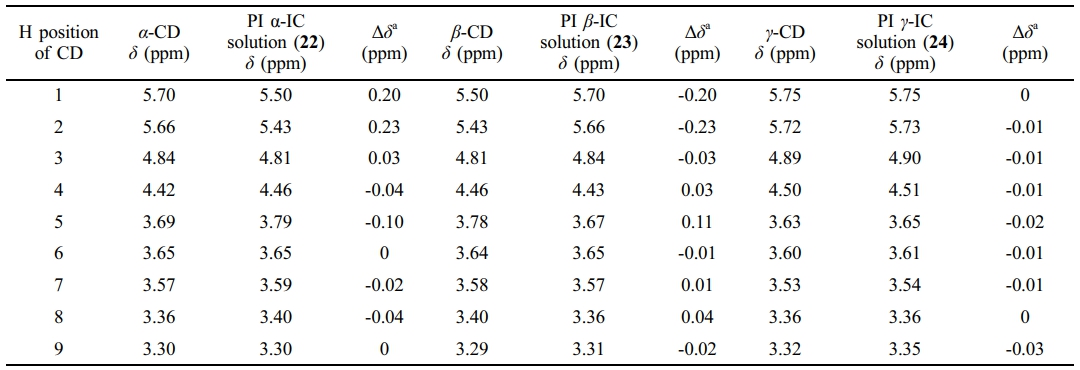
Table 4에는 IC solution과 free CD의 프로톤이 가진 chemical shift를 비교하였다. Chemical shift의 차이는 다이아민이나 폴리아믹산과 거의 유사하게 나타났고, γ-CD의 chemical shift가 가장 작다는 경향도 동일하게 확인할 수 있었다.
1H NMR의 분석 결과를 통해, CD가 다이아민, 폴리아믹산, 폴리이미드와 혼합되어 chemical shift를 나타내는 것으로, 해당 물질들과 Host-Guest 상호작용을 형성하여 포접복합체를 구성했다는 것을 시사한다. Host-Guest 상호작용과 관련하여, 1H NMR의 chemical shift 수치를 추가정보의 Table S4에서 자세하게 확인할 수 있다.
|
Figure 2 GPC curves of PAA (9) and PI (17). |
|
Figure 3 FTIR spectra of DMSO and CD solution. |
|
Figure 4 FTIR spectra of ODA solution (2) and ODA CD-IC solution (6-8). |
|
Figure 5 FTIR spectra of PAA solution (10) and PAA CD-IC solution (14-16). |
|
Figure 6 FTIR spectra of PI solution (18) and PI CD-IC solution (22-24). |
|
Figure 7 1 H NMR spectra of ODA (1), ODA CD-IC (3-5) and ODA CD-IC solution (6-8). |
|
Figure 8 1 H NMR spectra of PAA (9), PAA CD-IC (11-13) and PAA CD-IC solution (14-16). |
|
Figure 9 1 H NMR spectra of PI (17), PI CD-IC (19-21), and PI CD-IC solution (22-24). |
|
Table 2 Chemical Shift of CD Protons in ODA CD-IC Solution of by 1H NMR |
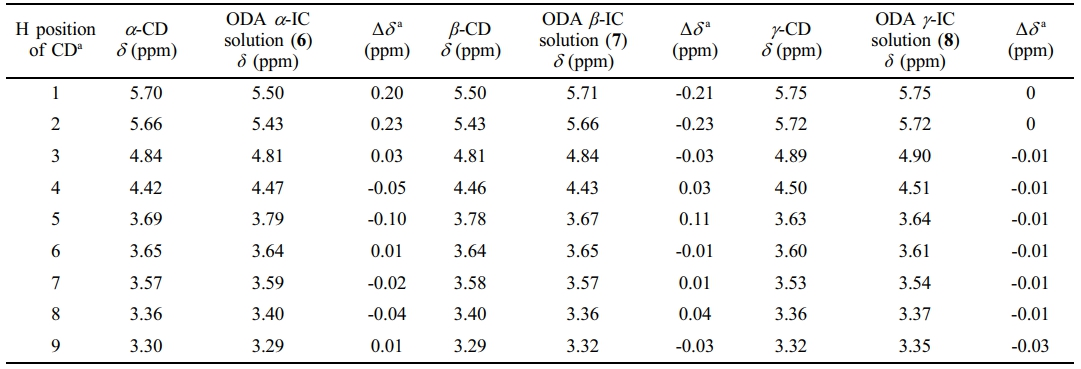
aΔδ = δ(free CD)−δ(complex CD) |
|
Table 3 Chemical Shift of CD Protons in PAA CD-IC Solution of by 1H NMR |
aΔδ = δ(free CD) − δ(complex CD) |
|
Table 4 Chemical Shift of CD Protons in PI CD-IC Solution of by 1H NMR |
aΔδ=δ(free CD) − δ(complex CD) |
본 연구에서는 다이아민 ODA와 6FDA를 이용하여 중합한 폴리아믹산, 그리고 chemical imidization을 통해서 얻어진 폴리이미드에 CD를 혼합하고 DMSO에 용해시키는 것으로 용액상의 포접복합체를 얻을 수 있었다. 또한, DMSO의 용액상에 물을 첨가하는 것으로, 고체상으로 회수를 할 수 있었다. 이렇게 용액상과 고체상을 분석하여 포접복합체 구조를 확인하였다. FTIR 스펙트럼 분석 결과를 통해, 모든 용액상에서의 포접복합체는 CD의 존재로 3100-3600 cm-1에서 -OH기의 확인과 1150 cm-1 부근에서는 C-O-C 또는 C-O의 밴드를 확인할 수 있었다. 또한, 1H NMR 스펙트럼에서는 CD가 포접복합체를 형성하는데 관여하는 H의 피크가 shift한 것을 확인할 수 있었다. 이러한 결과들을 통해서, 포접복합체는 용액상에서 안정하게 형성된다는 것을 알 수 있었다. 또한, 고체상으로 회수하는 과정에서 대부분의 CD는 포접복합체에서 분리되고 물에 용해되어, 고체상에서는 CD의 피크가 검출되지 않거나 매우 작게 검출되는 경향을 보였다. 다이아민의 경우에는 포접복합체를 형성하더라도 분자의 사슬이 매우 짧기 때문에, CD가 쉽게 이탈하고 용해되어 제거되는 것으로 생각할 수 있다. 반면, 폴리아믹산이나 폴리이미드의 경우에는 분자량이 높아짐에 따라, 일부의 CD가 포접복합체에서 이탈하지 못하고 회수되는 것으로 생각할 수 있다. 이러한 결과들을 통해서, 폴리이미드의 포접복합체의 형성을 위해서 다이아민과 CD를 용매에서 혼합한 상태에서 중합 과정을 통해, 내부에 포접된 CD는 이탈하기 어렵고, 포접되지 않은 CD들은 물로 세척하는 과정에서 제거할 수 있다. 이를 통해 폴리아믹산 또는 폴리이미드의 포접복합체 형성에 대한 가능성을 고려해볼 수 있으며, 고리성분을 활용한 다양한 폴리아믹산과 폴리이미드의 연구에 기여되기를 희망한다.
- 1. Hu, Z.; Liu, X.; Ren, T.; Saeed, H. A. M.; Wang, Q.; Cui, X.; Huai, K.; Huang, S.; Xia, Y.; Fu, K.; Zhang, J.; Chen, Y. Research Progress of Low Dielectric Constant Polymer Materials. J. Polym. Eng. 2022, 42, 677-687.
-

- 2. Wang, L.; Yang, J.; Cheng, W.; Zou, J.; Zhao, D. Progress on Polymer Composites with Low Dielectric Constant and Low Dielectric Loss for High-frequency Signal Transmission. Front. Mater. 2021, 8, 774843.
-

- 3. Maeda, H.; Liang, Y.; Hosoya, R.; Marui, R.; Yoshida, E.; Chen, Y.; Hatakeyama-Sato, K.; Nabae, Y.; Nakagawa, S.; Morikawa, J.; Tokita, M.; Sawada, R.; Ando, S.; Hayashi, Y.; Yoshida, R.; Furuya, H.; Hayakawa, T. Smectic Liquid Crystalline Poly(ester imide)s with Low Dielectric Dissipation Factors for High-frequency Applications. Polym. J. 2025, 57, 665-677.
-

- 4. Hou, J.; Sun, J.; Fang, Q. Oxygen-free Polymers; New Materials with Low Dielectric Constant and Ultra-low Dielectric Loss At High Frequency. Polym. Chem. 2023, 14, 3203-3212.
-

- 5. Hasegawa, M.; Horie, K. Photophysics, Photochemistry, and Optical Properties of Polyimides. Prog. Polym. Sci. 2001, 26, 259-335.
-

- 6. Zou, B.; Zhao, S.; Bao, F.; Zhou, L.; He, B.; Zhao, Y.; Zhang, J.; Peng, W.; Shen, Y.; Huang, M.; Nan, C.-W. Optimizing the Charge Transfer Complex Structure of Polyimides with Fluorinated Side Biphenyl for Superior High-temperature Capacitive Performance. Adv. Funct. Mater. 2025, 35, 2505254.
-

- 7. Zhang, C.; He, X.; Lu, Q. High-frequency Low-dielectric-loss in Linear-backbone-structured Polyimides with Ester Groups and Ether Bonds. Commun. Mater. 2024, 5, 55.
-

- 8. Chen, Y. C.; Lin, Y. C.; Chang, E. C.; Kuo, C. C.; Ueda, M.; Chen, W. C. Investigation of the Structure-dielectric Relationship of Polyimides with Ultralow Dielectric Constant and Dissipation Factors Using Density Functional Theory. Polymer 2022, 256, 125184.
-

- 9. Li, X.; Zheng, R.; Wang, C.; Chang, H.; Chen, S.; Wang, L.; Cui, X.; Liu, Y.; Li, J.; Yu, G.; Shi, J. Preparation and Properties of Low-dielectric Polyimide Films Containing Tert-butyl. Polymers 2024, 16, 984.
-

- 10. Qi, H.; Wang, X.; Zhu, T.; Li, J.; Xiong, L.; Liu, F. Low Dielectric Poly(imide siloxane) Films Enabled by a Well-defined Disiloxane-linked Alkyl Diamine. ACS Omega 2019, 4, 22143-22151.
-

- 11. Wang, H.; Zhang, Y.; Lv, X.; Li, J.; Wang, K.; Zhang, G.; Sun, R. Synthesis and Properties of a Novel Perfluorinated Polyimide with High Toughness, Low Dielectric Constant and Low Dissipation Factor. Ind. Chem. Mater. 2025, 3, 587-595.
-

- 12. Chen, Y.; Liu, Y.; Min, Y. Innovative Fluorinated Polyimides with Superior Thermal, Mechanical, and Dielectric Properties for Advanced Soft Electronics. Polymers 2025, 17, 339.
-

- 13. Pang, Z.; Sun, H.; Guo, Y.; Du, J.; Li, L.; Li, Q.; Yang, J.; Zhang, J.; Wu, W.; Yang, S. Research Advances of Porous Polyimide-based Composites with Low Dielectric Constant. Polymers 2023, 15, 3341.
-

- 14. Qian, C.; Bei, R.; Zhu, T.; Zheng, W.; Liu, S.; Chi, Z.; Aldred, M. P.; Chen, X.; Zhang, Y.; Xu, J. Facile Strategy for Intrinsic Low-k Dielectric Polymers: Molecular Design Based on Secondary Relaxation Behavior. Macromolecules 2019, 52, 4601-4609.
-

- 15. Li, Y.; Zhao, J. Q.; Yuan, Y. C.; Shi, C. Q.; Liu, S. M.; Yan, S. J.; Zhao, Y.; Zhang, M. Q. Polyimide/crown Ether Composite Films with Necklace-like Supramolecular Structure and Improved Mechanical, Dielectric, and Hydrophobic Properties. Macromolecules 2015, 48, 2173-2183.
-

- 16. Li, H.; Wang, X.; Gong, Y.; Zhao, H.; Liu, Z.; Tao, L.; Peng, Y.; Ma, K.; Hu, Z.; Dastan, D. Polyimide/crown Ether Composite Film with Low Dielectric Constant and Low Dielectric Loss for High Signal Transmission. RSC Adv. 2013, 13, 7585-7596.
-

- 17. Zhang, X.; Dou, Y.; Liu, L.; Song, M.; Xi, Z.; Xu, Y.; Shen, W.; Wang, J. Polyimide Films Based on β-cyclodextrin Polyrotaxane with Low Dielectric and Excellent Comprehensive Performance. Polymers 2024, 16, 901.
-

- 18. Zhang, C.; Yu, Y.; Ding, Y.; Yang, T.; Duan, G.; Hou, H. β-Cyclodextrin Toughened Polyimide Composites Toward All-organic Dielectric Materials. J. Mater. Sci. Mater. Electron. 2018, 29, 1182-1188.
-

- 19. Saura-Sanmartin, A.; Nicolas-Garcia, T.; Pastor, A.; Quiñonero, D.; Alajarin, M.; Martinez-Cuezva, A.; Berna, J. Control of the Assembly of a Cyclic Hetero[4]pseudorotaxane from a Self-complementary[2]rotaxane. Chem. Sci. 2023, 14, 4143-4151.
-

- 20. Su, H.; Chen, W.; Li, L.; Li, B.; Zhang, Z.-Y.; Li, C. Coordination-driven Poly[2]pseudorotaxanes in Highly Polar Organic Solvent. Front. Chem. 2020, 8, 579.
-

- 21. Dong, S.; Yuan, J.; Huang, F. A Pillar[5]arene/imidazolium [2]rotaxane: Solvent- and Thermo-driven Molecular Motions And Supramolecular Gel. Chem. Sci. 2014, 5, 247.
-

- 22. Nakai, Y.; Yamamoto, K.; Terada, K.; Kajiyama, A.; Sasaki, I. Properties of Crystal Water of α-, β-, and γ-cyclodextrin. Chem. Pharm. Bull. 1986, 34, 2178-2182.
-

- 23. Hazra, S.; Kumar, G. S. Physicochemical Properties of Inclusion Complexes of Sanguinarine with Natural Cyclodextrins: Spectroscopy, Calorimetry and NMR Studies. RSC Adv. 2015, 5, 1873-1882.
-

- 24. Thi, T. D.; Nauwelaerts, K.; Froeyen, M.; Baudemprez, L.; Van Speybroeck, M.; Augustijns, P.; Annaert, P.; Martens, J.; Van Humbeeck, J.; Van den Mooter, G. Comparison of the Complexation Between Methylprednisolone and Different Cyclodextrins in Solution by 1H NMR and Molecular Modeling Studies. J. Pharm. Sci. 2010, 99, 3863-3873.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2024 Impact Factor : 0.6
- Indexed in SCIE
 This Article
This Article
-
2026; 50(2): 226-237
Published online Mar 25, 2026
- 10.7317/pk.2026.50.2.226
- Received on Jul 30, 2025
- Revised on Nov 4, 2025
- Accepted on Nov 28, 2025
 Services
Services
Shared
 Correspondence to
Correspondence to
- Jaeyeong Choi*, Yun Ho Kim* , and Jong Chan Won*
-
*Advanced Functional Polymers Research Center, Korea Research Institute of Chemical Technology (KRICT), Daejeon 34114, Korea
- E-mail: mookii93@gmail.com, yunho@krict.re.kr, jcwon@krict.re.kr
- ORCID:
0009-0002-2508-4354








 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.