- Polyester Synthesis via Ring-Opening Copolymerization: Comparison of the Effects of Catalysts and Cocatalysts
Department of Chemistry, Chungnam National University, Daejeon 34134, Korea
- 개환 공중합 반응을 통한 폴리에스터 합성: 촉매와 조촉매 영향 비교
충남대학교 자연과학대학 화학과
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
Polyester, as eco-friendly polymers, have received increasing attention in various industrial fields. However, conventional synthetic methods often face limitations in controlling molecular weight distribution and achieving structural diversity. To overcome these challenges, we studied ring-opening copolymerization (ROCOP) of cyclic anhydrides and epoxides catalyzed by (salcy)AlCl complex or aminotriphenolate-based Cr complexes. The effects of four different co-catalysts and the presence or absence of solvent were investigated in conversion and ester selectivity. The structures of the synthesized polyesters were confirmed by 1H NMR spectroscopy, and the molecular weights and dispersity were determined by gel permeation chromatography (GPC). This work provides fundamental insights for the synthesis of functional polyesters and the optimization of catalyst systems.
친환경 고분자인 폴리에스터는 다양한 산업 분야에서 주목받고 있다. 분자량 분포의 제어와 구조적 다양성 확보에 한계가 있는 기존 합성법의 한계를 극복하기 위해, 본 연구에서는 고리형 무수물과 에폭사이드의 고리 개환 공중합을 도입하였으며 (salcy)AlCl 및 aminotriphenolate 기반 Cr 촉매를 적용하여 폴리에스터 중합의 성능을 비교하였다. 이와 함께 4종의 조촉매와 용매 조건에 따른 전환율과 선택성 변화를 체계적으로 분석하였다. 합성된 폴리에스터 구조는 핵자기 공명분광분석(nuclear magnetic resonance, NMR)으로 확인하였으며, 분자량과 분자량 분포도는 겔 투과 크로마토그래피(gel permeation chromatography, GPC) 분석을 통해 측정하였다. 본 연구를 통해 기능성 폴리에스터 합성과 촉매 시스템의 최적화에 있어 유용한 기초 데이터를 제공할 수 있을 것으로 기대된다.
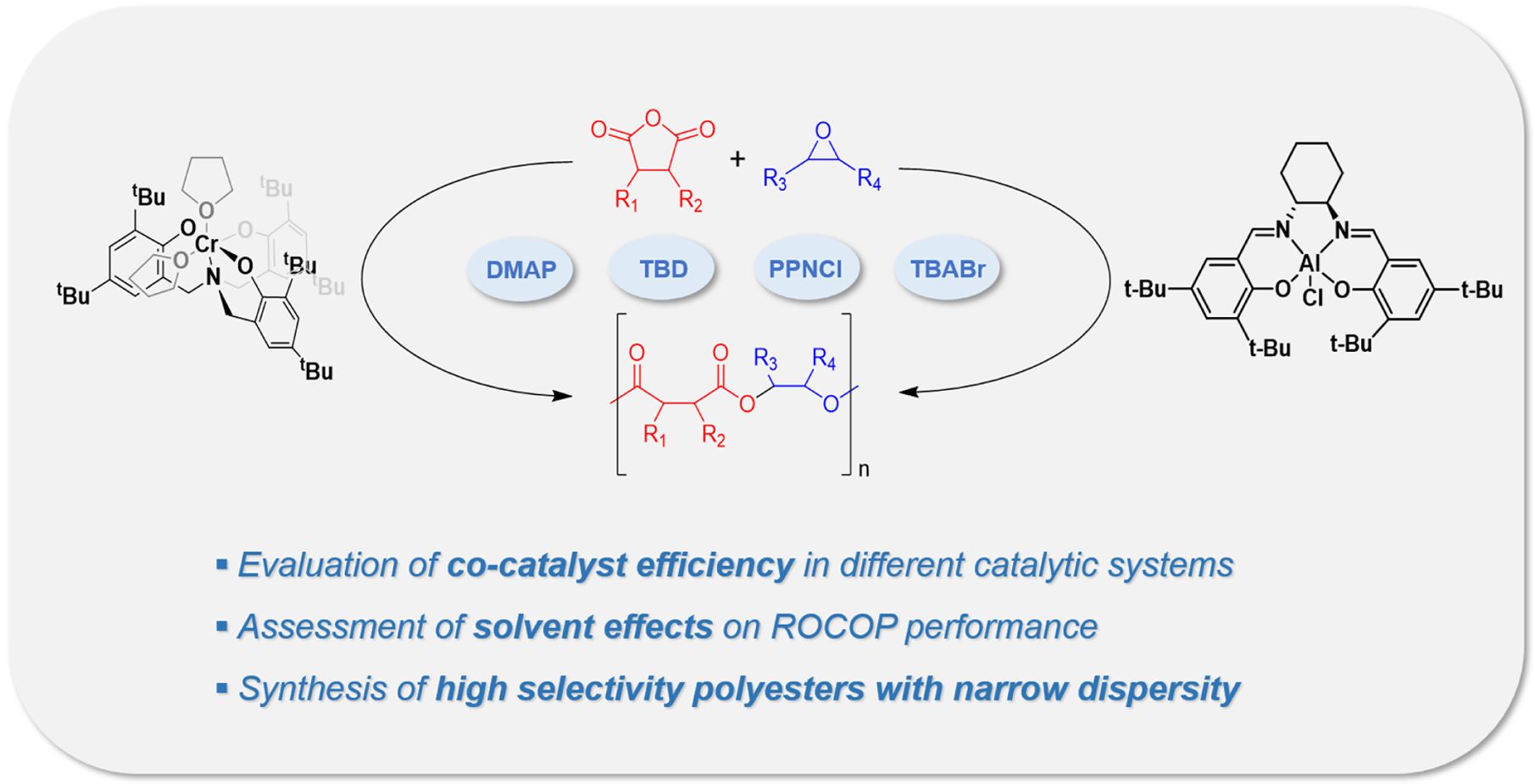
Polyester synthesis via ring-opening copolymerization (ROCOP) was carried out using (salcy)AlCl or aminotriphenolate-Cr complex in combination with various co-catalysts to compare catalytic efficiency and solvent effects. This approach enabled the synthesis of polyesters with narrow dispersity in high selectivity using various monomer combinations.
Keywords: polyester, ring-opening copolymerization, catalyst, co-catalyst.
이 연구는 충남대학교 학술연구비에 의해 지원되었습니다.
저자들은 이해상충이 없음을 선언합니다.
본 연구에서 합성한 폴리에스터의 1H NMR 스펙트럼, GPC 분석 결과, 그리고 가능한 ROCOP 메커니즘이 포함되어 있습니다. 자세한 내용은 다음 사이트에서 확인할 수 있습니다(http://journal.polymer-korea.or.kr).
PK_2026_050_02_238_Supporting_Information.pdf (490 kb)
Supplementary Information
폴리에스터(polyester)는 대표적인 친환경 고분자로 경량성, 우수한 가공성과 기계적 특성으로 섬유, 코팅, 플라스틱, 가소제 등 다양한 산업 분야에서 광범위하게 활용되고 있다.1,2 이러한 폴리에스터는 전통적으로 다이올(diol)과 다이에스터(diester) 또는 다이카복실산(dicarboxylic acid)의 축합 중합(condensation polymerization)을 통해 합성된다(Scheme 1). 하지만 해당 중합 방식은 반응 과정에서 물이나 메탄올(methanol)과 같은 저분자 부산물이 생성되며, 전환율과 분자량을 높이기 위해 부산물을 제거하는 과정이 필수적으로 필요하다는 단점이 있다.3,4 또한, 축합 중합은 고분자 구조의 중합 제어의 한계가 있다는 등 여러 가지 단점을 가지고 있다.5 이러한 문제점을 해결하기 위한 대안으로 락톤(lactone) 단량체의 개환 중합(ring-opening polymerization, ROP)이 도입되었다. ROP는 촉매와 개시제를 이용해 제어된 중합이 가능하며, 좁은 분자량 분포도를 갖는 폴리에스터 합성이 가능하다.6 하지만, ROP에서 주로 사용되는 락톤 단량체는 구조 다양성이 부족하고 그로 인해 합성된 폴리에스터의 물성 및 열적 특성이 제한된다는 한계가 있다.7
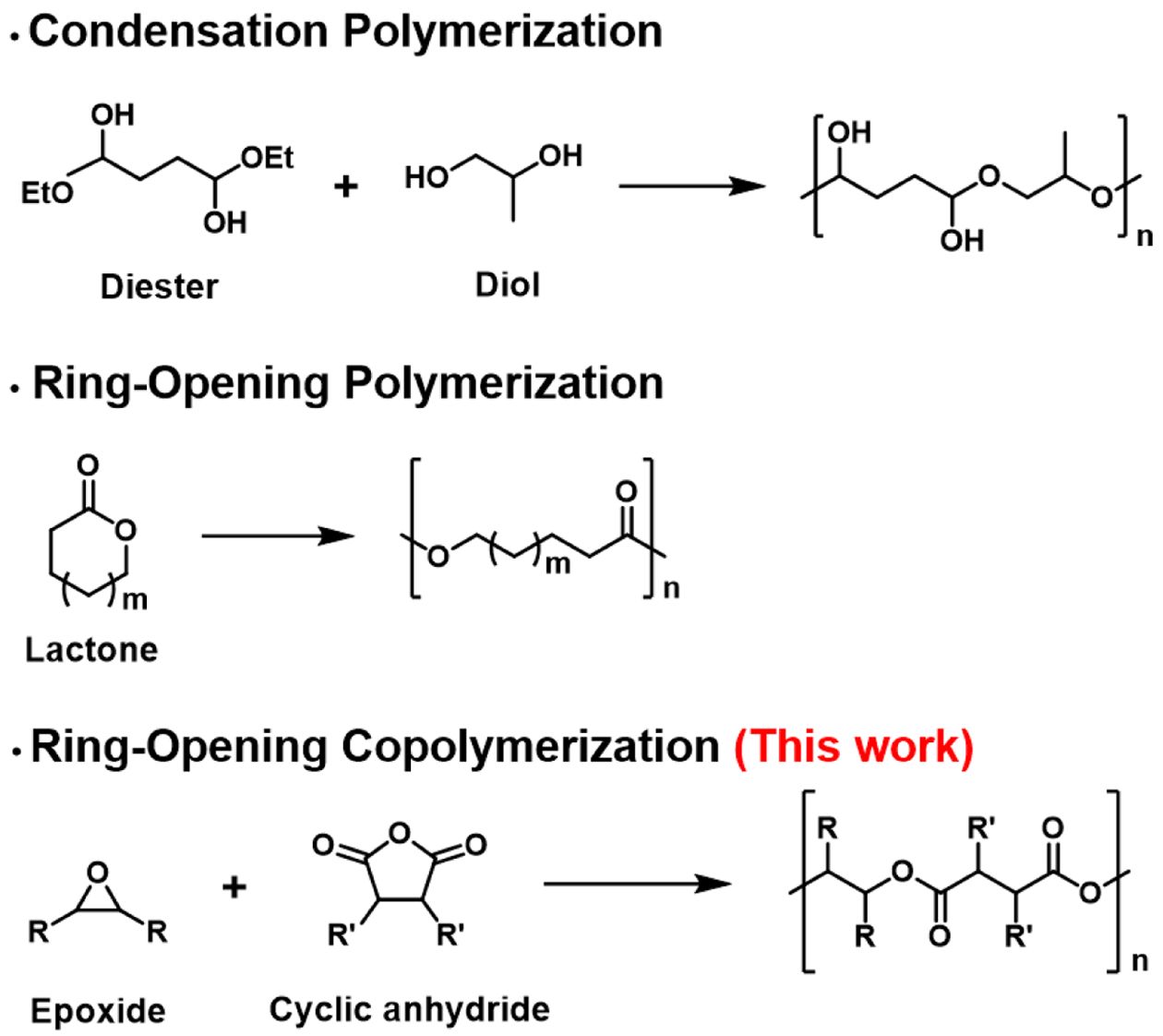
Scheme 1. Representative synthetic routes for polyester.
이러한 구조적 한계를 극복하기 위한 전략으로 본 연구에서는 개환 공중합(ring-opening copolymerization, ROCOP)을 이용한 폴리에스터 합성 전략을 선택하였다. ROCOP는 에폭사이드(epoxide)와 고리형 무수물(cyclic anhydride)의 고리가 교대로 열리며 진행되는 중합 방식이다. 단량체 선택의 자유도가 높고 반응 제어가 용이하여 다양한 구조의 폴리에스터를 설계할 수 있는 장점이 있다. 일반적인 ROCOP 메커니즘은 개시(initiation) 단계에서 에폭사이드 고리가 개환되면서 알콕사이드(alkoxide) 음이온이 생성된다. 이후, 해당 알콕사이드 음이온이 친핵체로 작용하며 고리형 무수물의 전자 결핍성 카보닐기(carbonyl)를 공격하여 에스터(ester) 결합을 형성하는 과정을 반복하며 중합이 진행된다(Figures S9-S11, Supporting Information 참조).7-9 최근 ROCOP 연구는 다양한 단량체 조합을 바탕으로 빠르게 발전하고 있으나, 일부 조합에서는 낮은 촉매 활성 및 선택성을 보인다.10 특히, 에터(ether) 서열 형성으로 인한 낮은 에스터 선택성과 같은 한계가 존재한다. 이러한 문제를 극복하기 위한 ROCOP 연구에서는 다양한 금속계 촉매와 리간드(ligand)가 개발되고 있다.11-13 최근 본 연구실에서도 쉽게 합성 가능한 아미노트라이페놀레이트(aminotriphenolate) 리간드 기반 Cr 촉매를 사용하여 ROCOP 중합 효율 향상에 기여한 바 있다.14,15
본 연구에서는 대표적인 무독성, 저렴한 금속 촉매인(R,R)-N,N'-bis(3,5-di-tert-butylsalicylidene)-1,2-cyclohexane diaminoaluminuma chloride [(salcy)AlCl]와, 이전 연구에서 높은 중합 효율을 보인 aminotriphenolate 기반 크롬 복합체를 사용하여 조촉매 및 다양한 반응 조건에 따른 중합 효율 변화를 비교하고자 한다. 단량체는 phthalic anhydride(PA)와 cyclohexene oxide(CHO) 외에도, vinyl cyclohexene oxide(VCHO), limonene oxide(LO), 1,8-naphthalic anhydride(NA) 등을 사용하였으며, 구조적 다양성을 갖는 폴리에스터 합성을 목표로 하였다. 고분자 전환율(conversion)과 폴리에스터 선택성은 1H NMR(proton nuclear magnetic resonance) 분석을 통해 평가하였고, 합성된 고분자의 분자량 및 분자량 분포도는 겔 투과 크로마토그래피(gel permeation chromatography, GPC)를 통해 분석하였다. 이 연구를 통해 우리는 ROCOP 반응 조건을 최적화하고 촉매 시스템 비교를 통해 고기능성 폴리에스터 합성을 위한 기초 데이터를 제공하고자 한다.
실험재료. 톨루엔(toluene), bis(triphenylphosphoranylidene) ammonium chloride(PPNCl), 1,5,7-triazabicyclo[4.4.0]dec-5-ene(TBD), CrCl3(THF)3, sodium hydride(NaH), (salcy)AlCl, LO, NA는 Sigma-Aldrich(St. Louis, USA)에서 구매하였다. Tetrabutylammonium bromide(TBABr), 4-dimethylaminopyridine (DMAP), 펜테인(pentane), CHO, VCHO, PA는 Tokyo Chemical Industry(Tokyo, Japan)에서 구매하였다. NMR 용매인 deuterated chloroform-d는 Cambridge Isotope Laboratories(Tewksbury, USA)에서 구매하였다. 다이에틸에터(diethyl ether), 헥세인(hexane), 다이클로로메테인(dichloromethane)은 Samchun Chemical Co.(Seoul, Korea)에서 구매 후 정제 없이 사용하였다. 이외에 반응에 사용된 모든 시약은 재결정 또는 정제를 통해 사용하였다. 조촉매는 극소량의 다이클로로메테인에 용해시킨 후 헥세인을 이용해 재결정하였고, 1~2일간 냉동 보관 후 하루 정도 진공 건조하여 사용하였다. 고리형 무수물은 150 mL의 뜨거운 다이에틸에터에 녹인 뒤 실온에서 서서히 냉각시키고 냉동 보관하여 재결정하였다. 톨루엔은 Na/benzophenone 시스템에서 2일간 교반 후 증류하였다. 증류된 용액은 냉동-진공-해동(freeze-pump-thaw) 방법을 3회 반복하여 탈기했다. 그 외의 에폭사이드 단량체는 칼슘하이드라이드(calcium hydride, CaH2) 하에서 2일간 교반 후, 진공 증류 및 동일한 탈기 과정을 3회 수행하였다. 모든 재결정 및 정제된 시약은 글러브 박스(glove box) 내부 냉동고에서 보관하였다.
실험 장비. NMR 분석은 400 MHz FT-NMR(AVANCE Neo 400; Bruker, USA)을 사용하였으며, 화학적 이동은 deuterated 용매의 내부 표준을 기준으로 분석했다. GPC 분석은 충남대학교 Core Facility의 Breeze HPLC system(Waters Corp., USA)을 사용하였다. Shodex KF-803, KF-804, KF-805(8.0×300 mm) 컬럼을 직렬로 연결하고, 보호용 가드컬럼 KF-G(4.6×10 mm)을 장착하였다. 이동상으로는 HPLC grade tetrahydrofuran(THF, HPLC grade, J.T.Baker, USA)를 사용하였으며, 유속은 1.0 mL/min으로 유지하였다. 검출기는 굴절률 검출기(refractive index detector, 40 ℃)를 사용하였고, 시료는 약 3-5 mg/mL 농도로 THF에 용해하여 30 μL 주입하였다. 분자량 및 분산도는 단분산 polystyrene 표준물질을 기준으로 보정하였다.
Aminotriphenolate-Cr 촉매 합성. Cr 촉매 합성 방법은 이전 논문에 보고한 절차를 참고하였다.14 NaH(17.2 mg, 0.72 mmol, 3.3 eq)와 리간드 LtBu,tBu(146 mg, 0.217 mmol, 1 eq)를 20 mL 바이알(vial)에 넣고 THF 10 mL를 첨가하여 1시간 실온 교반하였다. 이후, CrCl3(THF)3 (81.3 mg, 0.217 mmol, 1 eq)를 첨가하고 혼합물을 60 ℃에서 24시간 동안 교반했다. 반응 후 용매를 제거하고 남은 고체를 펜테인으로 추출하고 최종 Cr 복합체를 얻었다.
폴리에스터 합성. 모든 반응 용기는 130 ℃ 오븐(oven)에서 하루 정도 충분히 건조한 후 사용하였다. 중합 반응은 글러브 박스 내부에서 수행되었으며, 정제된 고리형 무수물, 에폭사이드, 촉매를 10 mL 둥근 바닥 플라스크에 넣은 후 조촉매를 첨가했다. 이후 설정된 온도의 오일 배스(oil bath)에서 일정 시간 동안 교반하였다. 반응이 종료된 후 NMR 분석을 위한 시료를 채취하였고, 생성물은 2 mL의 다이클로로메테인에 용해한 뒤 500 mL 메탄올에 천천히 침전시켰다. 침전된 생성물을 여과한 후, 진공 오븐에서 하루 동안 건조시켜 최종 고분자를 얻었다. 해당 고분자의 분자량 및 분자량 분포도는 GPC 분석을 통해 얻었다.
ROCOP 연구에서 가장 보편적으로 사용되는 단량체 조합인 PA와 CHO를 이용하여, 단량체:촉매:조촉매의 몰비율을 250:1:1로 설정하고 중합 반응을 진행하였다(Scheme 2). 초기 실험에서는 110 ℃에서 조촉매로 DMAP을 사용하여 용매가 없는 조건에서 중합을 시도하였다(entry 1, Table 1). 이러한 조건에서, 반응 2시간 후 고분자의 젤화가 진행되었으며, 50%의 전환율과 96%의 에스터 선택성을 나타냈다. 여기서 에스터 선택성이란, 에스터 결합을 형성하는 반응이 에터 결합을 형성하는 부반응에 비해 얼마나 우세하게 일어났는지를 나타내는 지표이다. 합성된 중합체는 7.1 kg/mol의 수평균 분자량(Mn)과 1.09의 좁은 분자량 분포도 지수를 나타냈다. 다음, 용매를 이용해 중합 속도를 조절할 수 있는지 확인하고자 반응 용매로 톨루엔을 사용하였다(entry 2). 톨루엔 0.5 mL를 첨가한 조건에서는 젤화가 상대적으로 느리게 진행되었고, 4시간 내 85%의 높은 전환율과 99% 이상의 에스터 선택성이 관찰되었다. 이 조건에서 얻은 폴리에스터는 13.1 kg/mol의 분자량과 1.06의 좁은 분자량 분포도를 나타냈다(Figure S5). 합성된 고분자의 구조는 1H NMR 분석을 통해 확인하였으며, 각 피크에 대한 구조 배정을 수행하였다(Figure S1).
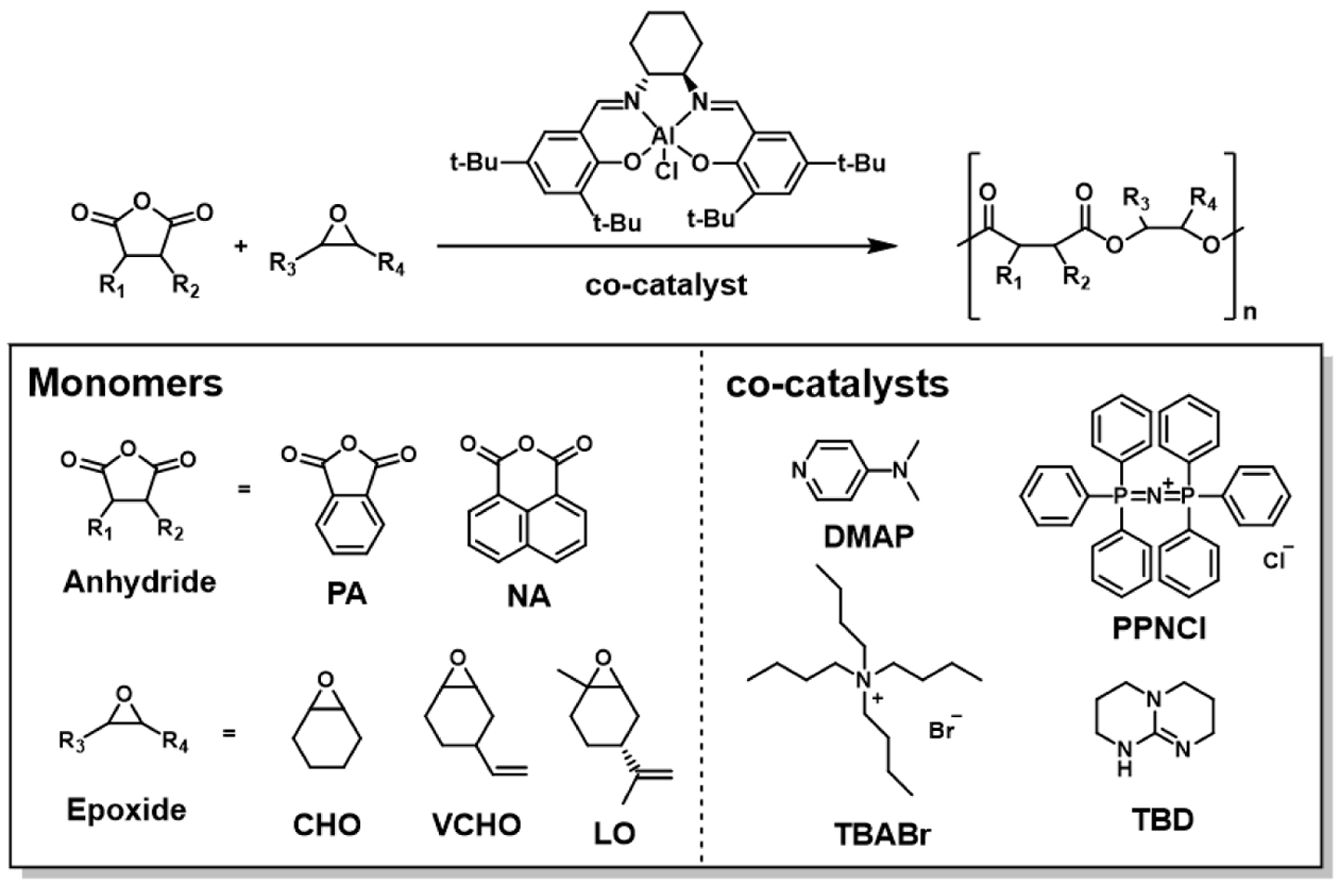
Scheme 2. Synthesis of polyesters via ROCOP of cyclic anhydrides and epoxides using (salcy)AlCl catalyst with various co-catalysts (Table 1)
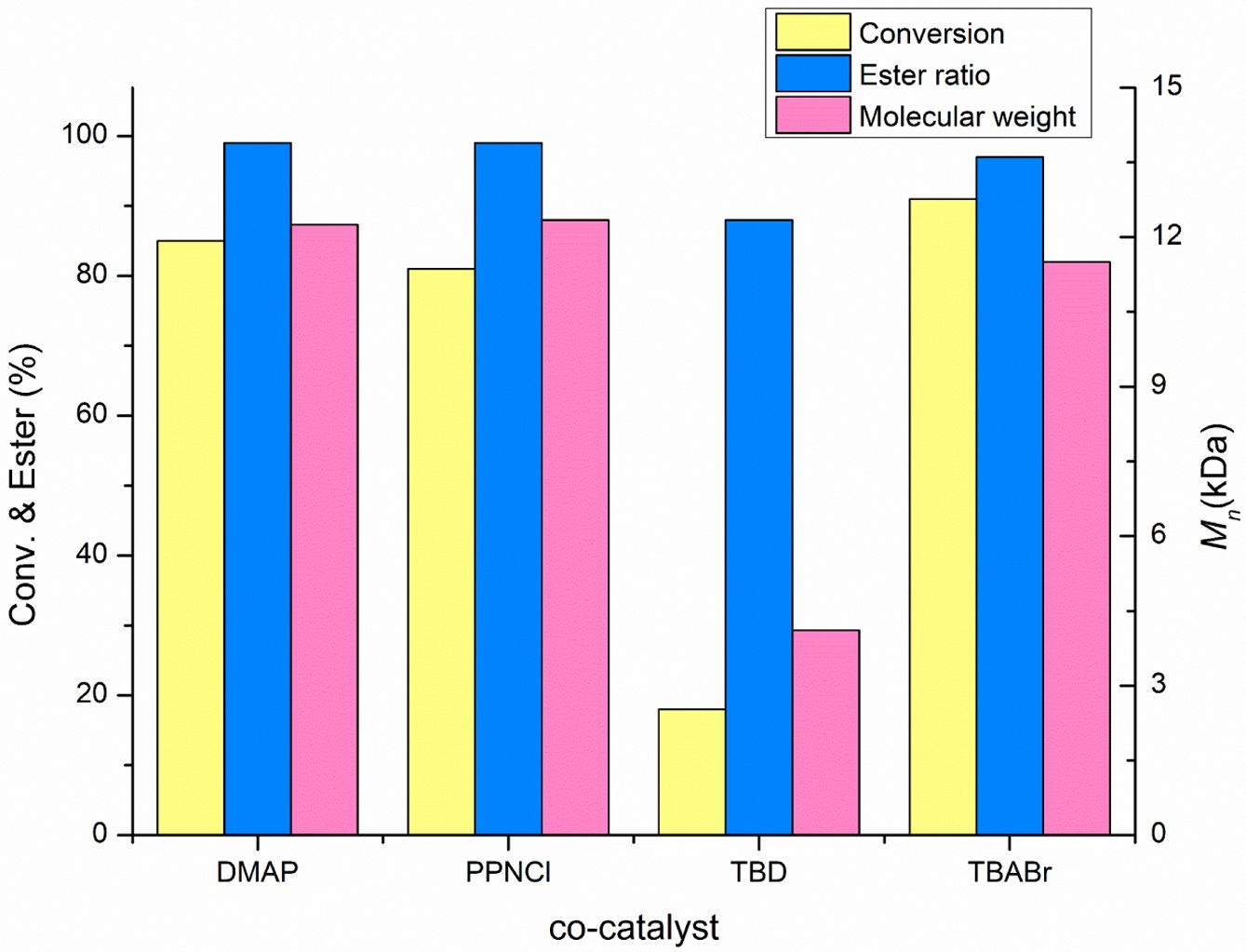
이후 동일한 용매 조건에서 조촉매를 변경하며 중합 반응을 수행하였다. DMAP 대신 PPNCl 조촉매를 사용한 경우, 81%의 전환율과 99% 이상의 선택성이 관찰되었으며, 얻어진 폴리에스터는 13.2 kg/mol의 분자량과 1.08의 분포도를 나타내어 DMAP과 유사한 성능을 보였다(entry 3). 반면, TBD 조촉매를 사용한 경우 전환율은 18%로 급감하였으며, 생성된 고분자의 분자량 역시 4.4 kg/mol로 낮아졌다(entry 4). 이는 (salcy)AlCl 촉매 시스템 하에서 TBD 조촉매가 에폭사이드의 고리를 개환하는 개시 효율이 상대적으로 낮거나 느린 전파 속도 때문으로 해석되며, 이러한 경향은 Kummari et al.의 연구 논문에서 유사하게 보고된 바 있다.16 해당 ROCOP 연구에서는 Al(CH3)3을 포함한 여러 촉매 시스템에서 TBD가 PPNCl, DMAP 등 보다 낮은 활성을 보이며 전환율이 저하된다는 사실을 실험적으로 입증한 바 있다. 한편, TBABr을 조촉매로 사용한 조건에서는 91%의 가장 우수한 고분자 전환율이 나타났으며, 97%의 선택성을 기록하였다(entry 5). 이 조건에서 중합된 고분자는 12.3 kg/mol의 분자량과 1.04의 좁은 분자량 분포도를 보여 DMAP과 PPNCl 조건과 유사한 결과를 보였다. 이후 TBABr을 사용하여 용매가 없는 조건에서 중합을 시도하였다(entry 6). 이때, 전환율은 56%로 다소 감소하였으나 생성 고분자의 분자량은 14.3 kg/mol으로 약간 증가하였다. 각각의 조촉매 효율을 나타낸 결과를 표로 정리하였다(Figure 1). 전환율, 선택성, 분자량 등을 모두 고려했을 때, TBD를 제외한 DMAP, PPNCl, TBABr 조촉매 모두(salcy)AlCl 촉매에서 우수한 효율을 나타냈다.
다음, 고분자 구조의 다양화를 위해 VCHO, LO, NA 등의 새로운 단량체를 이용한 폴리에스터 합성을 시도하였다. 먼저 PA/VCHO 조합의 경우, 기존 PA/CHO 시스템과 동일한 용매, 당량비, 온도 조건에서 실험을 진행하였다(entry 7). 반응 2시간 이내에 젤화가 발생했으며, 93%의 높은 전환율과 98%의 선택성을 보였다. 합성된 고분자는 4.5 kg/mol의 분자량과 1.14의 분포도를 나타냈다(Figure S6). 이는 기존 PA/CHO 조합에 비해 다소 낮은 분자량과 넓은 분포도이다. 한편, 바이오 기반 단량체인 LO와 PA의 조합에서는 LO의 큰 치환기로 인해 중합 속도가 저하되어 24시간 후에 젤화가 발생하였으며, 95%의 전환율 및 99% 이상의 선택성이 나타났다(entry 8). 이때 생성된 고분자는 3.1 kg/mol의 분자량과 1.23의 분포도를 보였다(Figure S7). 한편, PA 단량체로 합성한 고분자의 분자량 분포에서는 공통적으로 이중 분포(bimodal distribution)가 관찰되었다(Figures S5-S7). 이는 반응계 내 존재할 수 있는 프탈산(phthalic acid)이나 미량의 물에 기인한 것으로 해석된다.17 조촉매 개시 이외의 상이한 개시 경로는 이러한 이중 분포를 유발한 것으로 보이며, 유사한 현상은 선행 연구들에서도 반복적으로 보고된 바 있다.18 물성 측면에서 이러한 이중 분포는 원칙적으로 고분자의 기계적 및 열적 특성에 영향을 줄 수 있으나, 본 연구에서 분산도 값은 비교적 좁은 범위를 유지하였기 때문에 최종 고분자의 물성에는 제한적인 영향만 있을 것으로 판단된다. 고리형 무수물 NA와 CHO의 중합에서는 NA의 낮은 용해도로 인해 톨루엔 용매량을 2 mL까지 증가시키고 반응 시간을 24시간으로 조절하였다. 반응 24시간 후에도 젤화는 발생하지 않았으며, 전환율은 64%로 비교적 낮았다(entry 9). 생성된 폴리에스터는 1.7 kg/mol의 낮은 분자량을 가지며, 올리고머 형성에 머무른 것으로 보인다 (Figure S8). Entries 7-9에서 생성된 고분자는 모두 1H NMR 분석을 통해 구조를 확인하였다(Figures S2-S4). 종합적으로 PA/CHO 조합은 비교적 빠른 반응 속도와 높은 전환율 및 선택성을 보이며 안정적인 고분자화를 유도한다. 반면, VCHO, LO, NA 등의 조합에서는 단량체 구조에 기인한 반응성 저하로 인해 제한된 분자량의 중합체가 주로 형성되었고, 분자량 분포도 또한 넓어지는 경향을 나타냈다. 이러한 반응성 저하는 입체 장애가 큰 치환기 또는 경직된 고리 구조로 인해 중합 속도가 느려지는 것으로 해석된다. 이는 추가적인 치환기가 도입되었을 때 고온 및 장시간 반응이 요구되고 결과적으로 더 넓은 분자량 분포를 나타낸다고 보고된 기존 연구 결과와도 일치한다.19
조촉매 효과에 이어, 우리는 촉매에 의한 중합 결과를 비교해보고자 aminotriphenolate-Cr 복합체를 이용한 개환 공중합 실험을 110 ℃ 온도에서 톨루엔 용매 하에 진행하였다 (Scheme 3). 단량체와 촉매 및 조촉매 당량은 (salcy)AlCl 촉매 실험과 동일하게 250:1:1로 고정한 뒤, 이전(salcy)AlCl 촉매 실험에서 우수한 전환율과 선택성을 보인 PPNCl과 DMAP 조촉매부터 적용해보았다. 먼저, Table 2의 entry 1에서 PPNCl 조촉매는 2시간 만에 빠른 젤화가 나타났으며, 96%의 높은 전환율과 우수한 에스터 선택성이 확인되었다. 생성 고분자의 분자량은 6.1 kg/mol, 분자량 분포도는 1.10의 결과를 보였다. 동일한 조촉매 조건에서 용매 효과를 확인하기 위해 톨루엔 용매가 없는 조건에서 반응을 진행하였다(entry 2). 그 결과, 고분자 전환율은 76%로 다소 감소했으며, 에스터 선택성 역시 83%로 낮아졌다. 이는 개환 공중합에서 부반응의 억제를 위해 용매 도입이 선택성 조절에 효과적일 수 있음을 시사한다. 이러한 경향은 Zhang et al.이 보고한 Zn 촉매 시스템에서도 유사하게 관찰되었다.20 해당 연구에서는 CHO와 MA의 공중합에서 벌크(bulk) 조건에서는 poly(ester-co-ether) 구조가 주로 형성되었으나, 톨루엔 등의 용매를 도입할 때 에스터 결합이 우세한 완전 교대 구조의 폴리에스터가 생성되었다. 이와 같은 결과는 용매 조건이 반응 선택성에 중요한 영향을 미친다는 점을 뒷받침한다. 이후 다른 조촉매의 영향을 추가로 비교하고자 반응 시간을 2시간으로 통일하여 실험을 진행하였다. Entry 3에서 보듯이, DMAP 조촉매는 다소 낮은 50 %의 전환율과 에스터 선택성(87%)을 나타내었다. 해당 조건에서 합성된 고분자의 분자량은 5.4 kg/mol, 분자량 분포도는 1.04로 좁은 분포를 보였다. Entry 4에서는 TBABr을 사용한 결과, 56% 전환율이 관찰되었다. 생성 고분자의 분자량은 5.8 kg/mol, 분자량 분포도는 1.10이었다. Entry 5의 TBD 조촉매는 79%의 전환율과 87%의 선택성을 보였으며, 생성 고분자의 분자량과 분자량 분포도는 각각 5.7 kg/mol과 1.09로 TBABr과 유사한 수준이었다. 이 결과로부터, Cr 촉매 시스템에서 PPNCl 조촉매가 가장 선택성 높고 효율적인 개시제임을 확인할 수 있었다.
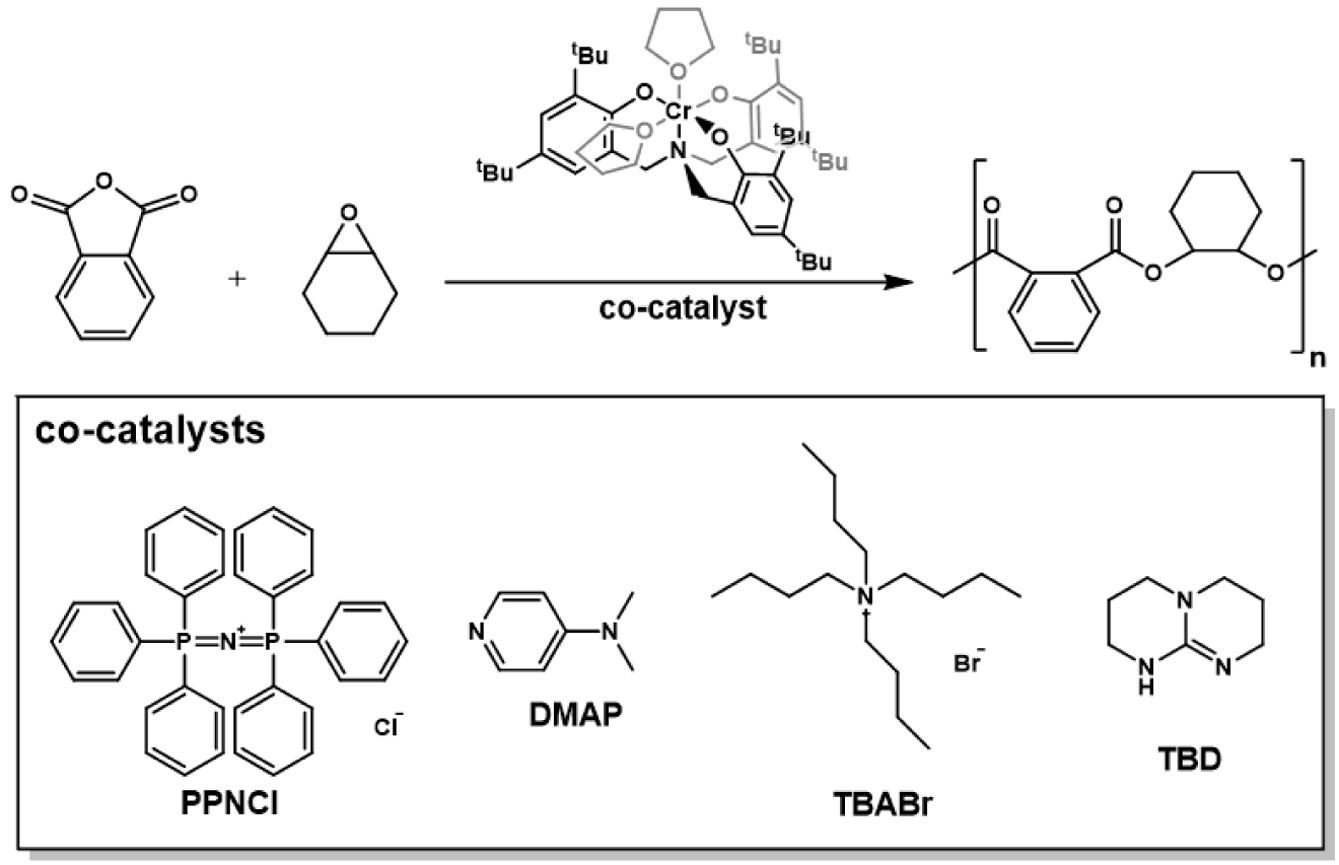
Scheme 3. Synthesis of polyesters via ROCOP of cyclic anhydrides and epoxides using aminotriphenolate-Cr complex in the presence of various co-catalysts (Table 2).
위 실험 결과를 종합해보면, (salcy)AlCl과 aminotriphenolate-Cr 촉매 모두 조촉매의 종류에 따라 전환율과 선택성이 크게 영향을 받는 것을 확인할 수 있었다. 이 중 (salcy)AlCl 촉매는 PPNCl, DMAP, TBABr 등 다양한 조촉매와의 호환성이 뛰어나 대부분의 조건에서 높은 전환율과 선택성을 보였다. 반면, Cr 촉매는 동일한 조촉매 조건에서도 전환율이 전반적으로 낮았으며, 특히 DMAP과 TBABr 사용 시 활성은 상당히 감소하였다. 흥미롭게도, (salcy)AlCl에서 가장 낮은 활성을 보였던 TBD는 Cr 촉매 하에서는 상대적으로 우수한 전환율을 기록했다. 이러한 차이는 조촉매의 분자 수준 작용에 기인한다. PPNCl은 [PPN]+ 양이온이 Cl- 또는 카복실산에 의한 개환을 촉진하고 에폭사이드 활성화를 도와 반응을 가속화함으로써 높은 활성을 보이는 것으로 보고 되었다.16,17 반대로 (salcy)AlCl/TBD 조합에서는 사슬 내 에스터 그룹과 TBD 사이 수소 결합이 중간체를 과도하게 안정화해 전파 속도를 저해하는 것으로 알려져 있다.19 따라서 (salcy)AlCl 촉매는 TBD와 같은 일부 조촉매 조합에서는 효율이 저하되나, 전반적으로 다양한 조촉매 조건에서 안정적이고 높은 전환율을 보이며 범용성이 큰 시스템으로 평가된다. 반면 Cr 촉매는 PPNCl과 같은 특정 조촉매와의 조합에서 높은 선택성과 빠른 반응성을 나타내고 저분자량 폴리에스터 합성에 효과적임을 시사한다. 이와 같이 두 시스템 모두 목적에 따라 선택적으로 활용 가능한 촉매 시스템으로 기대된다.
|
Figure 1 Comparison of co-catalyst effects in ROCOP performance from entries 2-5 in Table 1. |
|
Table 1 Ring-opening Copolymerization of Epoxides and Cyclic Anhydrides Using (salcy)AlCl in the Presence of Various co-catalysts |
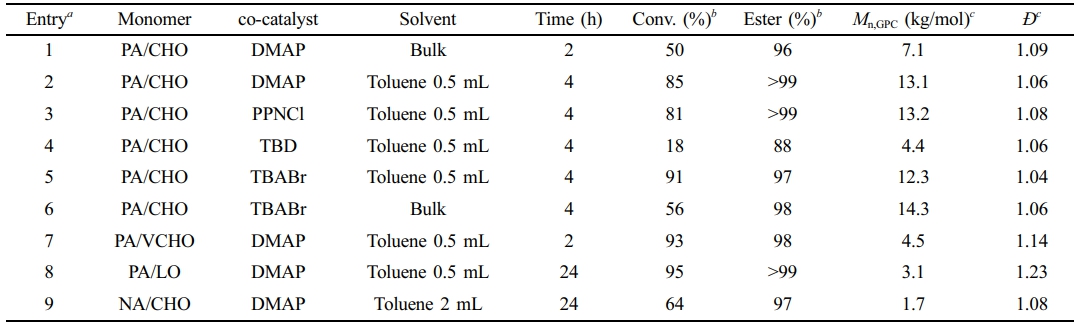
aROCOP reactions were performed using 4 mmol of cyclic anhydrides and epoxides with 0.016 mmol of (salcy)AlCl and co-catalysts at 110 ℃. bConv. (%) is the conversion of anhydrides, and ester (%) is the proportion of ester linkages over ether linkages; both were determined by 1H NMR analysis. cDetermined by GPC in THF calibrated with polystyrene standards, Dispersity (Ð) = weight-average molecular weight (Mw)/number-average molecular weight (Mn). |
|
Table 2 Ring-opening Copolymerization of PA and CHO Using Aminotriphenolate-Cr Complex in the Presence of Various co-catalysts |
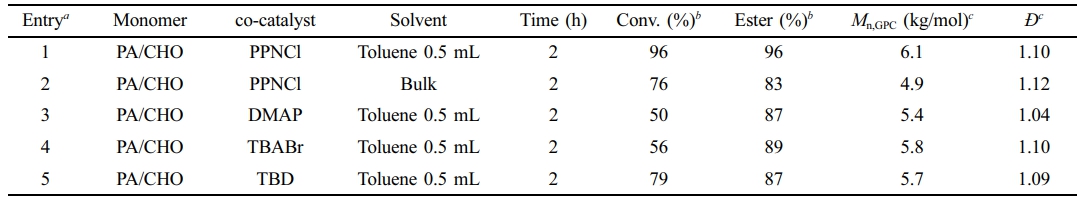
aReactions were performed using 4 mmol of cyclic anhydrides and epoxides with 0.016 mmol of Cr complex and co-catalysts. bConv. (%) is the conversion of anhydrides, and ester (%) is the proportion of ester linkages over ether linkages; both were determined by 1H NMR analysis. cDetermined by GPC in THF calibrated with polystyrene standards, Dispersity (Ð) = weight-average molecular weight (Mw)/number-average molecular weight (Mn). |
본 연구에서는 (salcy)AlCl과 aminotriphenolate 기반 Cr 복합체를 촉매로 사용하여 ROCOP 반응을 수행하였다. 네 가지의 조촉매와 용매 조건이 고분자 합성 효율 및 선택성에 미치는 영향을 체계적으로 비교하였다. 대표적인 단량체 조합인 PA/CHO 시스템에서는 (salcy)AlCl 촉매 하에서 DMAP과 PPNCl 모두 우수한 선택성(>99%)을 보였고, 낮은 분자량 분포도를 갖는 생성물을 합성하였다. TBABr은 가장 높은 전환율(91%)을 나타냈다. VCHO, LO, NA 등 다양한 단량체 조합을 적용한 결과, 용해도 차이와 치환기에 따라 생성된 폴리에스터 분자량에 차이가 발생하였다. Cr 복합체 시스템에서는 PPNCl이 가장 높은 전환율과 선택성을 보이는 효과적인 조촉매로 확인되었다. 결론적으로, 해당 결과는 ROCOP 반응에서 촉매, 조촉매 및 용매 조건 조절이 중합 효율 및 선택성 향상에 중요한 영향을 미침을 시사한다. 이 결과들은 향후 고기능성 폴리에스터 합성과 촉매 시스템 최적화를 위한 연구에 유용한 기초 정보를 제공할 수 있을 것으로 기대된다.
- 1. Pang, K.; Kotek, R.; Tonelli, A. Review of Conventional and Novel Polymerization Processes for Polyesters. Prog. Polym. Sci. 2006, 31, 1009-1037.
-

- 2. Zhang, Q.; Song, M.; Xu, Y.; Wang, W.; Wang, Z.; Zhang, L. Bio-based Polyesters: Recent Progress and Future Prospects. Prog. Polym. Sci. 2021, 120, 101430.
-

- 3. Driscoll, O. J.; Stewart, J. A.; McKeown, P.; Jones, M. D. Ring-Opening Copolymerization Using Simple Fe(III) Complexes and Metal- and Halide-Free Organic Catalysts. Macromolecules 2021, 54, 8443-8452.
-

- 4. Jérôme, C.; Lecomte, P. Recent Advances in the Synthesis of Aliphatic Polyesters by Ring-opening Polymerization. Adv. Drug Deliv. Rev. 2008, 60, 1056-1076.
-

- 5. Yokoyama, A.; Yokozawa, T. Converting Step-Growth to Chain-Growth Condensation Polymerization. Macromolecules 2007, 40, 4093-4101.
-

- 6. Kamber, N. E.; Jeong, W.; Waymouth, R. M.; Pratt, R. C.; Lohmeijer, B. G. G.; Hedrick, J. L. Organocatalytic Ring-Opening Polymerization. Chem. Rev. 2007, 107, 5813-5840.
-

- 7. Paul, S.; Zhu, Y.; Romain, C.; Brooks, R.; Saini, P. K.; Williams, C. K. Ring-opening Copolymerization (ROCOP): Synthesis and Properties of Polyesters and Polycarbonates. Chem. Commun. 2015, 51, 6459-6479.
-

- 8. Longo, J. M.; Sanford, M. J.; Coates, G. W. Ring-Opening Copolymerization of Epoxides and Cyclic Anhydrides with Discrete Metal Complexes: Structure–Property Relationships. Chem. Rev. 2016, 116, 15167-15197.
-

- 9. Diment, W. T.; Lindeboom, W.; Fiorentini, F.; Deacy, A. C.; Williams, C. K. Synergic Heterodinuclear Catalysts for the Ring-Opening Copolymerization (ROCOP) of Epoxides, Carbon Dioxide, and Anhydrides. Acc. Chem. Res. 2022, 55, 1997-2010.
-

- 10. Plajer, A. J.; Williams, C. K. Heterocycle/Heteroallene Ring-Opening Copolymerization: Selective Catalysis Delivering Alternating Copolymers. Angew. Chem., Int. Ed. 2022, 61, e202104495.
-

- 11. Lidston, C. A. L.; Severson, S. M.; Abel, B. A.; Coates, G. W. Multifunctional Catalysts for Ring-Opening Copolymerizations. ACS Catal. 2022, 12, 11037-11070.
-

- 12. Reis, N. V.; Deacy, A. C.; Rosetto, G.; Durr, C. B.; Williams, C. K. Heterodinuclear Mg(II)M(II) (M=Cr, Mn, Fe, Co, Ni, Cu and Zn) Complexes for the Ring Opening Copolymerization of Carbon Dioxide/Epoxide and Anhydride/Epoxide. Chem. Eur. J. 2022, 28, e202104198.
-

- 13. Andrea, K. A.; Plommer, H.; Kerton, F. M. Ring-opening Polymerizations and Copolymerizations of Epoxides Using Aluminum- and Boron-centered Catalysts. Eur. Polym. J. 2019, 120, 109202.
-

- 14. Jeong, S. Y.; Kim, J.; Lee, E.; Son, K.-s. Ring-Opening Copolymerization Using a Chromium Complex with a Readily Available Aminotriphenolate Ligand. Organometallics 2023, 42, 1125-1130.
-

- 15. Ryu, H. K.; Bae, D. Y.; Lim, H.; Lee, E.; Son, K.-s. Ring-opening Copolymerization of Cyclic Epoxide and Anhydride Using a Five-coordinate Chromium Complex with a Sterically Demanding Amino Triphenolate Ligand. Polym. Chem. 2020, 11, 3756-3761.
-

- 16. Kummari, A.; Pappuru, S.; Chakraborty, D. Fully Alternating and Regioselective Ring-opening Copolymerization of Phthalic Anhydride with Epoxides Using Highly Active Metal-free Lewis Pairs as a Catalyst. Polym. Chem. 2018, 9, 4052-4062.
-

- 17. Hošťálek, Z.; Trhlíková, O.; Walterová, Z.; Martinez, T.; Peruch, F.; Cramail, H.; Merna, J. Alternating Copolymerization of Epoxides with Anhydrides Initiated by Organic Bases. Eur. Polym. J. 2017, 88, 433-447.
-

- 18. Xie, R.; Zhang, Y.-Y.; Yang, G.-W.; Zhu, X.-F.; Li, B.; Wu, G.-P. Record Productivity and Unprecedented Molecular Weight for Ring-Opening Copolymerization of Epoxides and Cyclic Anhydrides Enabled by Organoboron Catalysts. Angew. Chem., Int. Ed. 2021, 60, 19253-19261.
-

- 19. Ota, I.; Suzuki, R.; Mizukami, Y.; Xia, X.; Tajima, K.; Yamamoto, T.; Li, F.; Isono, T.; Satoh, T. Organobase-Catalyzed Ring-Opening Copolymerization of Cyclic Anhydrides and Oxetanes: Establishment and Application in Block Copolymer Synthesis. Macromolecules 2024, 57, 3741-3750.
-

- 20. Zhu, L.; Liu, D.; Wu, L.; Feng, W.; Zhang, X.; Wu, J.; Fan, D.; Lü, X.; Lu, R.; Shi, Q. A trinuclear [Zn3(L)2(OAc)2] Complex Based on the Asymmetrical Bis-Schiff-base Ligand H2L for Ring-opening Copolymerization of CHO and MA. Inorg. Chem. Commun. 2013, 37, 182-185.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2024 Impact Factor : 0.6
- Indexed in SCIE
 This Article
This Article
-
2026; 50(2): 238-243
Published online Mar 25, 2026
- 10.7317/pk.2026.50.2.238
- Received on Aug 15, 2025
- Revised on Sep 29, 2025
- Accepted on Oct 24, 2025
 Services
Services
Shared
 Correspondence to
Correspondence to
- Kyung-sun Son
-
Department of Chemistry, Chungnam National University, Daejeon 34134, Korea
- E-mail: kson@cnu.ac.kr
- ORCID:
0000-0002-7804-1916









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.