- Formulation Study of HPMC-based Hot-melt Extruded Rebamipide Solid Dispersions for Solubility Enhancement and Sustained Release
Won Kyung Kim*,# , Giwon Lee*,#, Sunjae Park*, and Gilson Khang*, **, ***,†

*Department of PolymerNano Science & Technology, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896, Korea
**Department of Bionanotechnology and Bio-Convergence Engineering, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896, Korea
***Polymer Materials Fusion Research Center, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896, Korea- 용해도 개선 및 서방형 약물 방출 달성을 위한 HPMC 기반 열용융 압출 레바미피드 고체분산체의 제형 설계
*전북대학교 고분자나노공학과, **전북대학교 바이오나노융합공학과, ***전북대학교 고분자융합소재연구소
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
This study proposes a Hot Melt Extrusion method-based solid dispersion using HPMC to improve the solubility and achieve sustained release of rebamipide. The rebamipide solid dispersions show a 19-fold increase in water solubility compared with the pure rebamipide by combining pH adjustment and various surfactants. Fourier transform infrared spectroscopy (FTIR), X-ray diffractometer (XRD), and differential scanning calorimetry (DSC) analyses confirmed the amorphous transformation of rebamipide and its stable dispersion in the polymer matrix. Sustained-release tablet, prepared with rebamipide solid dispersion, showed first-order dissolution pattern over 14 hours, consistently with a diffusion-controlled mechanism. As a result, this study demonstrates the potential of combining solid dispersion and sustained-release technologies based on hot-melt extrusion method as an effective formulation platform for simultaneous solubility enhancement and controlled drug release.
본 연구에서는 난용성 위점막 보호제인 레바미피드에 열용융 압출을 적용하여 용해도를 개선하고, 동시에 서방화 용출을 달성할 수 있는 HPMC 기반 고체분산체를 제안하고자 하였다. pH 조절제와 다양한 계면활성제를 조합하여 열용융 압출을 통해 제조된 레바미피드 고체분산체는 원료 약물 대비 최대 19배까지 용해도가 증가하였다. Fourier transform infrared spectroscopy(FTIR), X-ray diffractometer(XRD) 및 differential scanning calorimetry(DSC) 분석을 통해 레바미피드의 무정형화 및 고분자 내 안정한 분산을 확인하였다. 레바미피드와 수용성고분자로 제조한 서방정은 약 14시간 동안 완만한 용출 패턴을 나타냈으며, 이는 서방정의 겔층 형성에 따른 확산 지연 기전과 일치하였다. 본 연구는 열용융 압출 기반 고체분산체와 서방화 기술을 결합하여 용해도 및 방출 제어를 동시에 구현할 수 있는 제형 플랫폼의 가능성을 제시한다.
To overcome poor bioavailability of Rebamipide, the formulation strategy was aimed to improve solubility and develop a sustained-release. The Rebamipide solid dispersion was prepared using the Hot Melt Extusion Method. HPMC was used as the polymer matrix with various surfactant and NaOH for facilitate solid dispersion formulation and further enhance solubility. The developed Rebamipide solid dispersion sustained release tablet exhibited various dissolution profiles depending on the surfactants as well as the presence of NaOH. In this study, all authors focused on exploring the practical usability of the HME-based sustained release Rebamipide tablet.
Keywords: rebamipide, solid dispersion, solubilization, hot-melt extrusion, sustained release.
이 논문은 2022년도 전북대학교 연구교수 연구비 지원 및 2024년도 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(No. RS-2024-NR121321).
저자(들)는 이해상충이 없음을 선언합니다.
약물의 생체 이용률을 결정하는 핵심 인자 중 하나는 약물의 수용성이다. 난용성 약물은 경구투여시 낮은 용해도로 인해 흡수가 제한적이고 충분한 약효를 발휘하기 위해 높은 용량의 투여가 필요하다.1 이러한 약물들은 Biopharmaceutics Classification System(BCS) Class II 및 IV에 해당하며 약물의 수용성과 투과성으로 인해 낮은 생체 이용률을 갖는 것이 특징이다. 이러한 난용성 약물을 가용화하여 낮은 수용해도를 개선하고 약물의 낮은 생체 이용률을 극복하는 연구가 활발히 이루어지고 있다.2
레바미피드(rebamipide, REB)는 프로스타글란딘의 생성을 촉진하여 염증성 사이토카인을 억제시킴으로써 항염증 효과를 유발하고 위점막의 점액 분비를 촉진하여 위점막을 재생 및 보호하는 약물이다. REB는 용해도와 투과성이 낮은 BCS Class IV 약물로 분류되며, 주로 소장 상부에서 흡수되고 소장하부로 갈수록 흡수율이 떨어진다.3,4 이러한 특징 때문에 1일 3회 복용이 필요하므로 환자의 복약 순응도 측면에서 매우 불리하다. 이를 보완하기 위하여 1일 2회 복용 가능한 서방정(무코스타 서방정®, Mucosta SR®)이 개발되어 있으나, 해당 의약품은 REB의 가용화 없이 방출 속도만 조절한 형태로 낮은 수용성 자체로 인한 문제를 근본적으로 개선하지 못하고 있다.5,6
고체분산체 기술은 약물을 친수성 고분자에 분산시켜 약물을 무정형 상태로 유지하게 함으로써 용해도를 개선하는 약제학적 기술이다. 무정형 상태의 약물은 결정성 구조가 없으므로, 결정 상태에서 용해에 필요했던 결정 격자에너지를 극복할 필요가 없으며, 이는 약물의 용해도 향상에 기여하는 결과로 이어진다.7,8 고체분산체에 사용되는 대표적인 수용성 고분자로는 히드록시프로필 메틸셀룰로오스(hydroxymethyl methylcellulose, HPMC), polyvinylpyrrolidone 및 polyethylene oxide 등이 있고 가용화제로는 poloxamer, sodium layryl sulfate (SLS), polyethylene glycol, polysorbate, cremophor RH-40 및 soluplus®등이 있다. 이러한 고분자와 가용화제는 고체분산체 내부의 약물이 무정형으로 안정한 구조를 형성하도록 기여한다. 본 연구에서는 가용화와 동시에 서방화 용출을 구현할 수 있고 제약 업계에서 널리 쓰이고 있는 HPMC를 고분자로 선정하였다. 또 계면활성제의 이온성 여부 및 HLB 값에 따른 용해도 개선 효과를 확인하기 위하여, 음이온성 계면활성제인 SLS와 비이온성 계면활성제인 Cremophor RH-40, Poloxamer 188 및 407을 선정하였다.9,10
Hot melt extrusion method(열용융압출 기술)은 고체분산체를 제조하는 기술로 최근 주목받고 있다. 열과 압력을 이용하여 고분자와 약물을 동시에 용융·혼합·압출하는 연속 공정으로 고체분산체를 효율적으로 제조할 수 있으며, 기존 가용화 기술인 spray drying 기술과는 다르게 용매를 사용하지 않고 공정이 비교적 간단하여 스케일업에도 용이하다.11-13
열용융압출기(hot melt extruder, HME)는 내부 챔버의 스크류에서 약물과 고분자 매트릭스를 녹임과 동시에 혼합함으로써 고분자 내 약물의 분산 균일성을 확보할 수 있고, 약물–고분자 간 상호작용, 유리전이온도, 점도 등의 고분자 물성을 기반으로 공정 최적화가 가능하다. 특히 챔버 내부의 스크류의 배열, 온도 및 압력 등의 공정 매개변수를 조절하는 것을 통해 공정 최적화가 가능하기에 상업적 스케일업에도 적합하기 때문에 고분자 과학의 응용 분야로 매우 유의미하다.12,13
또, 약물의 방출을 제어하는 서방화 기술은 약물의 지속성 확보 및 복약 횟수 감소의 이점을 제공하며, 낮은 생체이용률을 극복하기 위한 대표적인 약제학적 기술 중 하나이다.14,15 일반적인 경구투여 의약품은 복용 이후 혈중 약물 농도가 점차 상승하여 최대 농도에 도달한 뒤, 대사과정을 거쳐 농도가 감소하게 된다. 반면, 서방화 기술을 적용한 의약품은 고분자 매트릭스 및 삼투압 등을 활용한 기술로 약물 방출 속도를 조절함으로써 장시간동안 혈중 농도를 유효농도에 알맞게 유지할 수 있도록 설계된다. 이때 방출 속도는 고분자의 종류, 점도, 약물의 용해도 및 용출 환경에 따라 조절 가능하다.16
본 연구에서는 HME를 활용하여, 친수성 고분자인 HPMC, pH조절제인 NaOH 및 여러 계면활성제로 REB 고체분산체(REB-SD)를 제조함으로써 수용성을 향상시키는 동시에 서방화 기능을 부여하는 이중 기능 제형을 개발하였다.17 이를 위해 HPMC와 여러 가용화제를 조합하였고 HME 공정 조건을 최적화하였으며, 본 제형의 생체이용률 개선 가능성을 평가하였다.
시약 및 재료. 본 연구에 사용된 REB는 INIST ST(한국), 친수성 고분자인 HPMC는 Colorcon(미국), pH 조절제인 수산화 나트륨은 Showa(일본), 계면활성제인 SLS, Cremophor RH 40, Ploxamer 188 및 407은 Basf(독일)을 사용하였으며 실험에 사용된 모든 용매 및 시약은 HPLC 등급을 사용하였다.
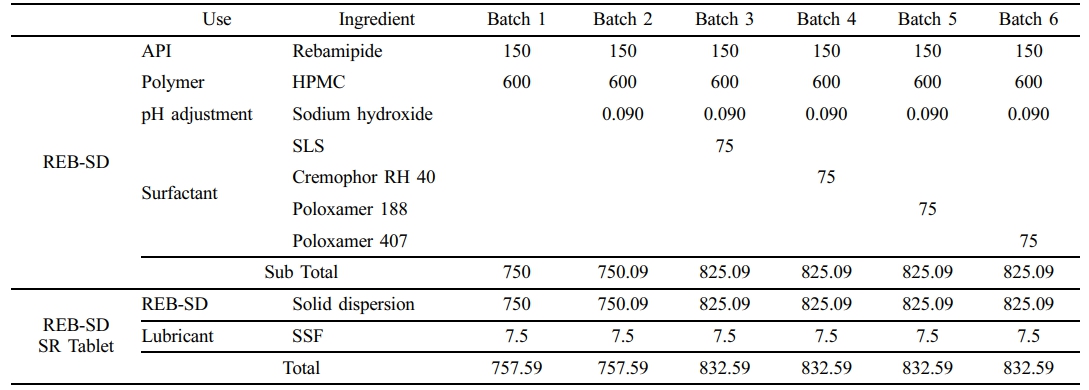
고체분산체 제조. 모든 배치는 Table 1과 같이 각 조성에 따라 원료의약품인 REB에 수용성 고분자인 HPMC, 수산화 나트륨 및 계면활성제를 첨가하여 HME 기술을 활용하여 REB 고체분산체(REB-SD)를 제조하였다. 그 과정을 간단하게 설명하면, 모든 원료들은 Table 1과 같이 칭량 후 30 mesh로 체과하였다. 그 후 혼합물은 HME(Process 11-hyqienic TSE, Thermo Fisher Scientific, 미국)를 통해 용융-압출되었으며, HME 조건은 Screw 속도는 30 rpm으로 고정하고 온도 조건은 Batch 1, 2의 경우 180 ℃, Batch 3, 4, 5, 6의 경우 160 ℃로 진행하였다. HME 공정 이후 길쭉한 형태의 필름을 얻었으며, 이를 막자, 막자사발 및 정제분쇄기를 통해 압출물을 분쇄한 후 30 mesh로 체과하여 파우더 형태로 수득하였다. 그 후 사용 전까지 데시케이터에 보관하였다.
가용화율 측정. REB 100 mg과 동량의 REB를 함유하는 REB-SD를 400 mL 증류수에 용해시킨 후 0.45 μm PTFE 필터를 사용하여 여과하였다. 여과액은 이동상에 희석하여 HPLC 분석을 통해 가용화도를 확인하였다. 모든 샘플은 각각 6회씩 측정하여 평균값과 표준편차를 계산하였다.
FTIR 분석. 본 연구에서 사용된 REB, HPMC 및 가용화제 및 제조된 REB-SD를 푸리에 변환 적외선 분광기(Fourier transform infrared spectroscopy, FTIR GX, Perkin Elmer, Waltham, USA)로 분석하여 HME 공정 중 물리화학, 구조적인 변화가 발생했는지 확인하고자 ATR-IR법으로 500~4000 cm-1 범위에서 측정하였다.
XRD 분석. 본 연구에서 사용된 REB, HPMC 및 가용화제 및 제조된 REB-SD의 포접이 잘 이루어졌는지 확인하기위해, X선 회절 분석기(X-ray diffractometer, XRD, MAX 2500, Japan)로 결정성을 분석하였다. X선 회절은 0.3 mm의 투명한 유리 기관을 사용하였고, 샘플 적정량을 적층한 후 30 mA, 40 KV의 조건에서 모든 시료는 1°/min의 속도로 측정범위 3-50°에서 분석하였다.
DSC 분석. 본 연구의 REB, HPMC 및 가용화제 및 제조된 REB-SD의 상전환을 확인하기 위해 시차 주사 열량계(differential scanning calorimetry, DSC, Perkin Elmer, USA)를 이용하여 분석하였다. DSC는 standard alum pan(Perkinelmer, USA)에 시료 5 mg을 넣고 커버를 덮어 압축하여 준비하였다. 모든 분석은 건조 질소 가스 하에서 25-350 ℃의 온도범위에서 10 ℃/min의 가열 속도로 수행하였다.
REB-SD 서방정 제조. REB-SD 서방정 제조를 위해 REB-SD 및 기타 부형제는 Table 1과 같이 각각 칭량하여 타정하였다. 간단하게 말하자면, 먼저 Table 1과 같이 REB-SD 및 부형제를 칭량 및 혼합 후 30 mesh에 체과하였다. 그 후 30 mesh에 체과된 혼합물은 40 mesh에 체과된 Sodium Stearyl Fumarate(SSF)와 1~2분가량 혼합하여 활택시킴으로써 최종 분체를 제조하였다.
제조된 최종 분체는 타정기(KT10SS, Keumsung, Korea)로 타정하여 REB-SD 서방정을 제조하였다. 타정 중 타정압과 REB-SD 서방정의 평균 경도, 최대경도는 REB-SD 서방정의 타정성 확인을 위해 함께 확인하였다.
REB 최종분체의 흐름성 및 타정성 평가. 최종 분체의 흐름성 및 타정성의 적합성을 확인하고자 BD/TD 시험을 진행하였다. 최종분체를 매스실린더에 넣고 부피밀도(Bulk density, BD)를 측정한 후, 1250회 밀도시험기(COPLEY Tapped Density Tester JV 200, UK)를 이용하여 압축밀도(Tapped density, TD)를 측정하였다. 측정한 BD와 TD로 흐름성 평가 지수인 카 지수(Carr’s index) 및 하우스너 비율(Hausner ratio)을 계산하여 최종 분체의 흐름성을 평가하였다.
REB-SD 서방정 용출률 평가. REB-SD 서방정의 용출률 평가를 위해 용출시험(USP Apparatus 2, 패들법)을 진행하였다. 용출액은 인산 완충 용액(pH 6.8, 900 mL)을 사용하였고, 온도와 패들 속도는 각각 37 ℃ 및 100 rpm으로 유지하였다. 각 1, 2, 4, 7, 10 및 14시간마다 시료를 2 mL씩 채취하고, 채취한 시료의 양과 동일한 양의 용출액을 채워주었다. 채취된 시료는 0.45 μm 필터에 여과 및 희석 후 HPLC로 분석하였으며, 용출률 계산식은 하기와 같다.
용출률(%) = {[(측정값-Y절편)/기울기] × 각 시점에 해당하는 용출액 부피}/(유효성분 함량 × 1000) × 100 × 희석배수 (1)
HPLC 분석. 가용화율 및 서방정 용출 평가를 위해 HPLC 분석을 실시하였다. 간단하게 말하자면, 장비는 HPLC 분석기(NS-4000 HPLC System, Futecs, Korea)를 사용하였고, 분석 컬럼은 C18 컬럼(ProntoSIL C18 SH 컬럼, 250 × 4.6 mm, 5 μm, Bischoff Chromatography, Germany)을 사용하였다. HPLC 조건은 유속 1.2 mL/min, 시료주입량 20 μL, 컬럼온도 36.5 ℃에서 측정하였고, UV 검출 파장은 327 nm, 측정 시간은 10분으로 설정하였다. 이동상은 메탄올과 증류수를 7:3 비율로 혼합한 용액을 사용하였으며, 아세트산을 사용하여 pH2.6으로 pH를 조정하고 초음파 처리를 통해 잔여 가스를 제거한 후 사용하였다.
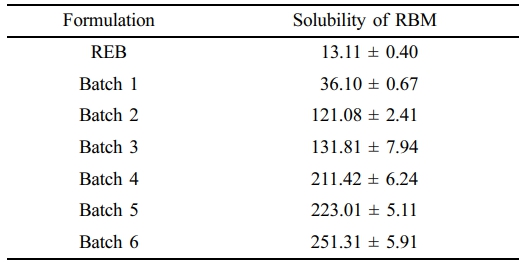
고체분산체 가용화율. REB와 각 배치별 고체분산체(Batch 1~6)의 용해도는 HPLC를 통해 포화 용해도를 분석하였으며 결과는 Table 2와 같다. REB의 수용성은 매우 낮아 증류수 400 mL 조건에서 용해도가 13.13±0.62 μg/mL 수준에 불과하였다. 반면, HME 공정을 통해 제조한 REB-SD(Batch 1~6)은 모든 제형에서 원료 약물 대비 유의적으로 높은 용해도를 나타냈다. 친수성 고분자인 HPMC 분산된 Batch 1은 36.10±0.67 μg/mL로 REB대비 약 3배 증가한 수치를 나타내었으며, 이는 결정형의 약물이 친수성 고분자 매트릭스에 분산되어 무정형으로 상전이를 통한 용해도 향상을 의미한다.8 pH 조절제인 NaOH가 첨가된 Batch 2의 경우 121.08±2.41 μg/mL으로 REB대비 약 9배 증가한 수치를 나타내었으며, 이는 약산성을 띠는 REB가 염기성 조건에서 이온화되어 용해도가 증가한 것으로 사료된다. 여기에 다양한 계면활성제를 첨가하여 고체분산체를 제조(Batch 3~6하였는데, 이들의 용해도는 각각 131.81± 7.94 μg/mL, 211.42±6.24 μg/mL, 223.01±5.11 μg/mL 및 251.31± 5.91 μg/mL을 나타냈다. 계면활성제가 첨가되며 REB-SD의 용해도가 적게는 약 10배에서 많게는 약 19배까지 증가한 수치를 나타내었는데, 이는 NaOH의 pH 조절과 계면활성제의 계면장력 저하효과로 인해 약물 용해도가 상승한 것으로 사료된다.18
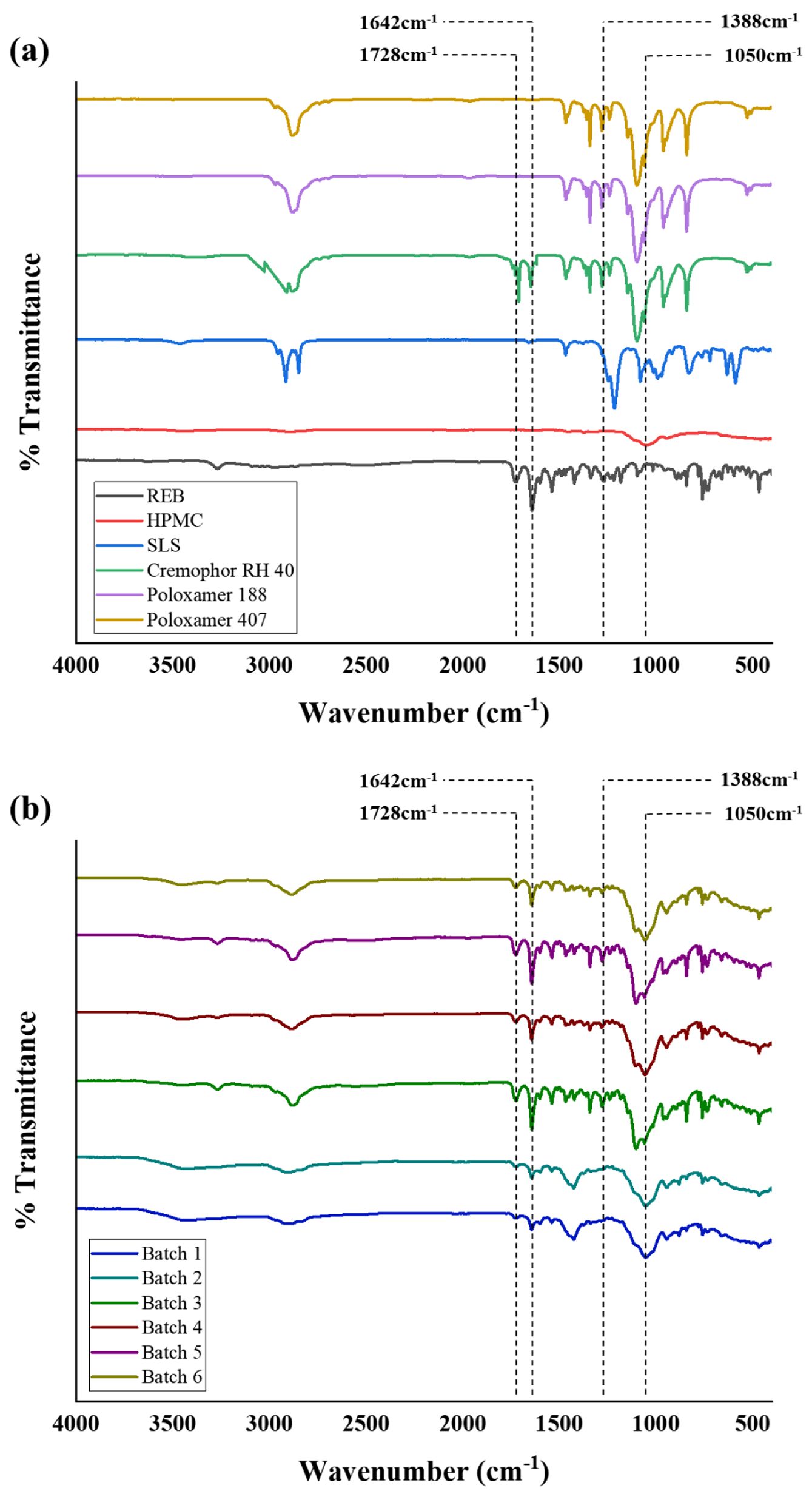
REB-SD의 FTIR 분석. REB, HPMC, 가용화제 및 각 배치별 고체분산체(Batch 1~6)의 물리화학적 상호작용 및 변화를 확인하기 위한 FTIR 분석 결과를 Figure 1에 나타내었다. REB는 3269 cm-1(N-H stretching), 1642 cm-1(C=O band), 1728 cm-1 (carboxylandamide groups) 및 1338 cm-1(C-H stretching)에서 특징적인 피크를 나타내었다. HPMC는 1050 cm-1(C-O-C stretching) 및 3425 cm-1(-OH stretching)에서 특징적인 피크가 관찰되었으며, 이 특징적인 피크들은 고체분산체(Batch 1~6)에서도 관찰됨에 따라, 고체분산체 제조과정 중 약물과 고분자의 변성이 일어나지 않았다고 판단하였다. 또한 고체분산체 FTIR 분석 결과, C-O-C stretching이 증가하여 HPMC와 유사한 구조적 특성이 나타나는데, 이는 REB가 HPMC의 에테르 결합 영역에 분산되며, 약한 수소결합 또는 반데르발스 상호작용이 형성되었음을 나타낸다.19
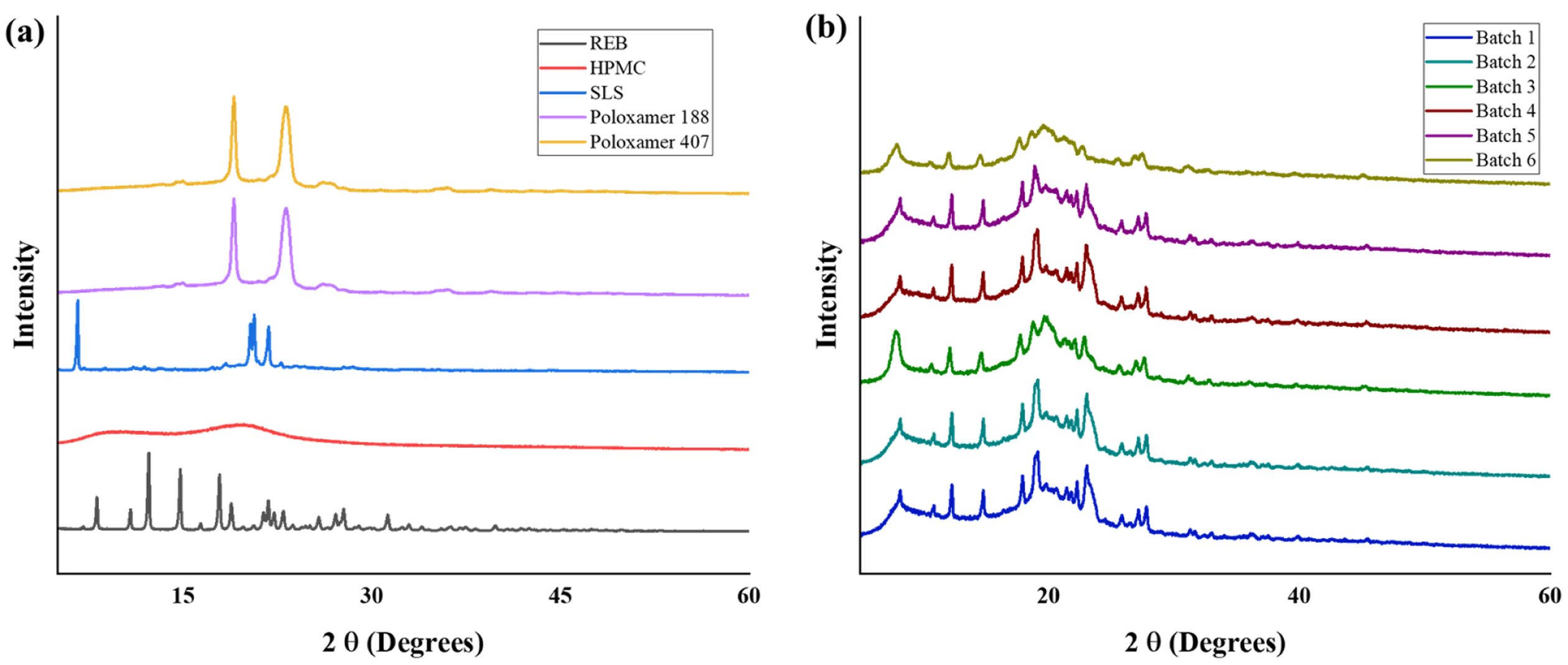
REB-SD의 XRD 분석. REB, HPMC, 가용화제 및 각 배치별 고체분산체(Batch 1~6)의 XRD 분석 결과를 Figure 2에 나타내었다. REB는 다양한 각도에서 많은 특징적인 회절 피크를 보였다. Batch 1~2의 고체분산체의 경우에는 가용화제가 첨가되지 않았음에도 회절 피크가 소실되거나 크게 감소하였으며, 나머지 가용화제가 첨가된 고체분산체(Batch 3~6)에서도 REB의 특징적인 회절 피크가 소실되거나 크게 감소한 넓은 비정질 패턴으로 전환되었다. 이는 HME 공정을 통해 REB가 HPMC 사슬 내 효과적으로 분산되어 결정형에서 비정질 상태로 안정적으로 분산되었음을 의미한다.19
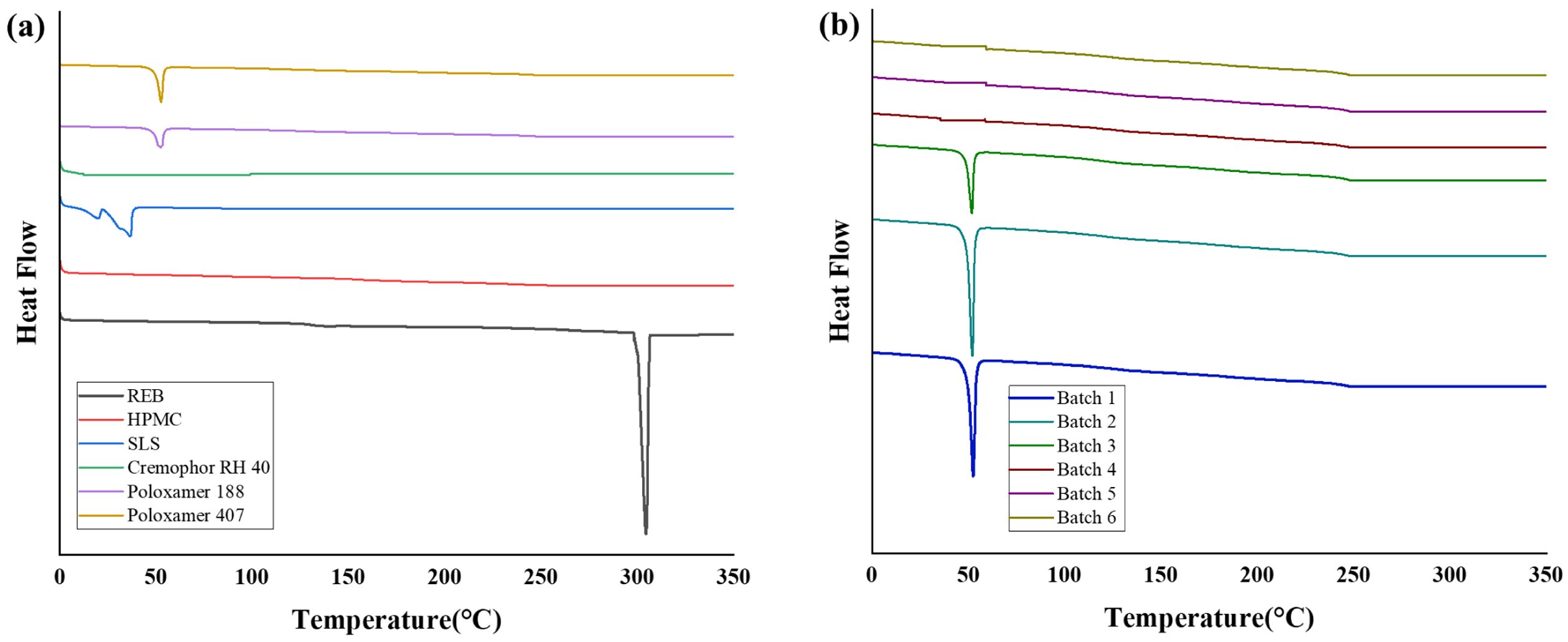
REB-SD의 DSC 분석. REB, HPMC, 가용화제 및 각 배치별 고체분산체(Batch 1~6)의 DSC 분석결과를 Figure 3과 같이 나타내었다. REB는 약 310 ℃ 부근에서 특징적인 흡열 피크를 보였으며, 이를 통해 REB가 특유의 결정 형태를 가지고 있음을 확인하였다. 고체분산체(Batch 1~6)에서는 해당 피크가 소실되거나 크게 감소하였고, 이는 REB가 열용융압출 공정을 통해 상전이가 발생하였음을 확인하였다. 특히, Batch 1~3에서 약 50 ℃ 부근에 흡열피크가 나타났는데, 이는 고온 및 고전단 조건 하에서 성분간 혼합을 유도하는 열-용융-압출로 이어지는 공정에 의해 만들어진 REB-SD 내부의 REB-HPMC 혼합 무정형 상의 열적 거동으로 해석될 수 있다. 이러한 열적 거동도 계면활성제의 물리화학적 특성 차이에 따라 다르게 나타났다. 자세하게 말하자면, 음이온성 계면활성제인 SLS를 포함한 Batch 3의 경우 50 ℃ 부근의 열적 거동이 유지된 반면, 비이온성 계면활성제인 Cremophor RH40 및 Poloxamer(188/407)를 포함한 Batch 4~6의 조성에서는 해당 이벤트가 관찰되지 않았다. 이는 비이온성 계면활성제가 REB-SD를 보다 효과적으로 가소화하여 분자 이동성을 증가시켰고, 이로인해 열적 이완 거동을 완화한 반면, SLS는 상대적으로 가소화 효과가 제한적이거나 이온성 상호작용에 의해 혼합계 구조가 유지되었기 때문으로 사료된다.19
종합적으로, FTIR, XRD 및 DSC 결과는 REB-SD에서 REB가 비정질 상태로 존재하며 고분자와 상호작용하여 안정한 고체분산체가 형성되었음을 보여주고 있다.
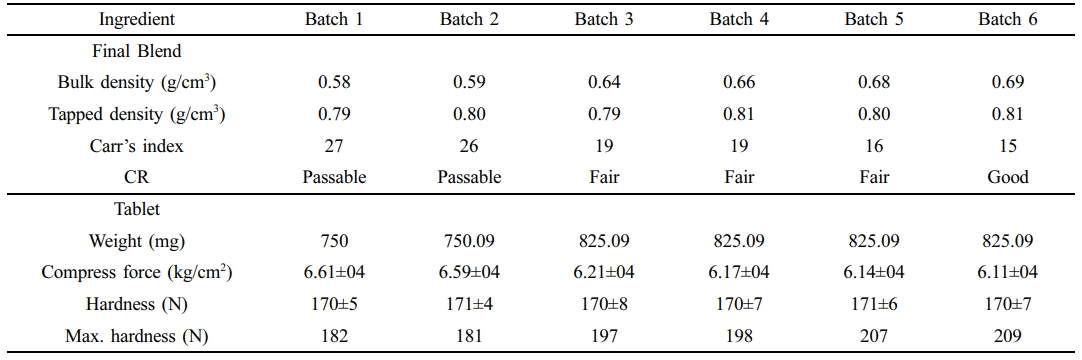
BD/TD 및 유동성 평가. 최종 분체(Batch 1~6)를 BD/TD 시험 측정을 통해 Carr’s index 및 Hausner ratio를 산출하여 Table 3과 같이 평가하였다. 모든 제형은 Possible ~ Good 수준의 준수한 유동성을 나타내었다. 이는 HME 공정 후 분쇄(분말화) 및 체과 과정을 통해 적절한 입자 분포가 확보되었기 때문으로 판단된다.20
REB-SD 서방정의 타정 특성. REB-SD 서방정(Batch 1~6)은 평균 170N의 경도로 타정하였다. 타정 결과 Table 3. BD/TD 및 타정결과와 같이 170N을 타정하는데 6.11 kg/cm2에서 6.61 kg/cm2의 압력을 가하였고, 최대 경도는 182N에서 209N을 나타내었다. HPMC의 압축성이 우수하여 REB-SD의 타정성이 우수할 것으로 예상하였으나, spray drying을 통해 제조한 REB-SD의 타정성(평균 경도: 200N, 타정압: 4.81 kg/cm2~ 6.12 kg/cm2 & 최대 경도 260N~325N)과 비교하였을때 낮은 타정성을 나타냈다.21 이는 REB-SD를 제조하기위해 HME 공정으로 얻은 필름을 분쇄하여 수득하였기 때문에 spray drying을 통해 얻은 고체분산체와 비교하여 높은 취성(Brittleness)을 가지기 때문인 것으로 사료된다.21-23
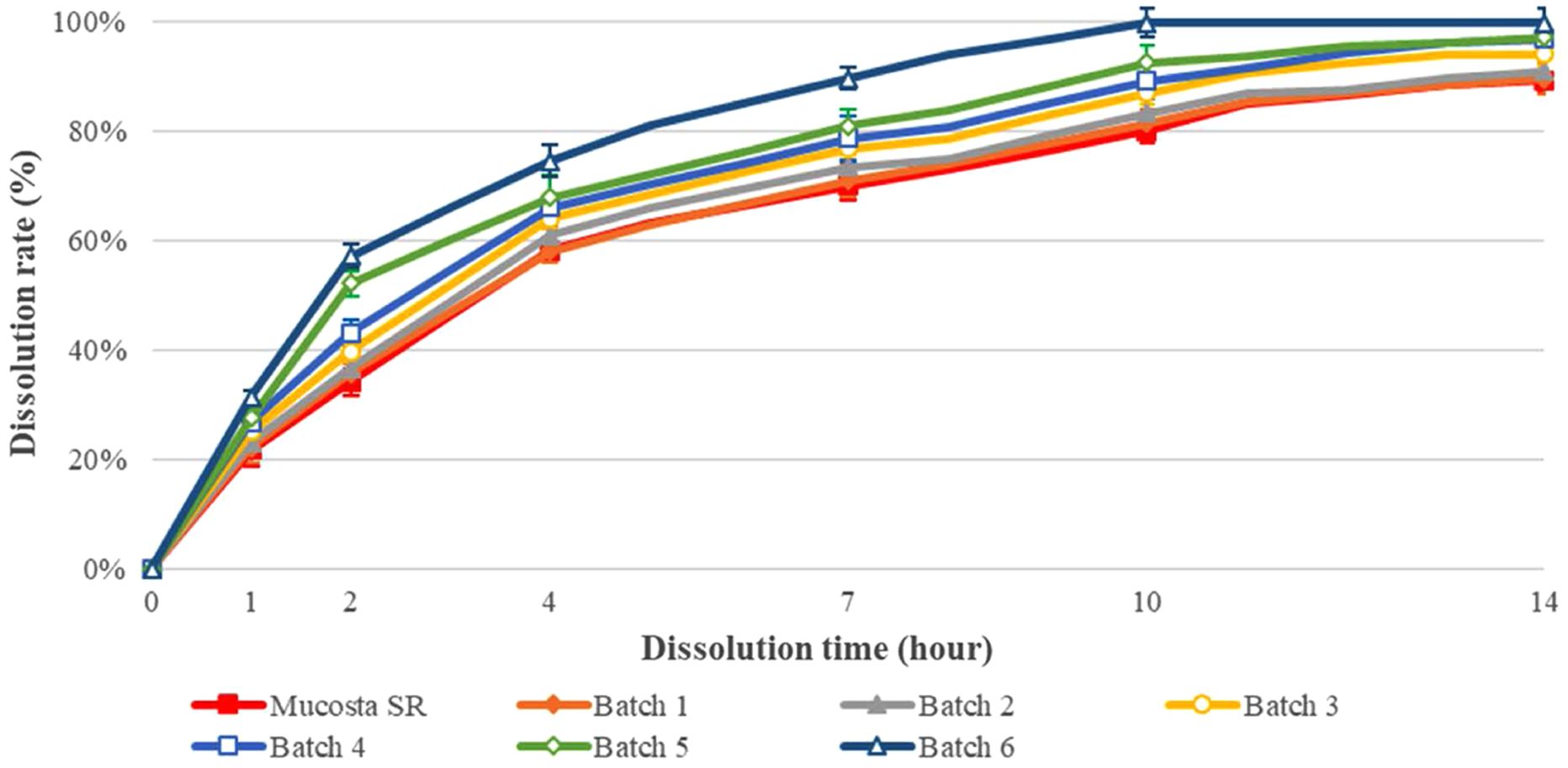
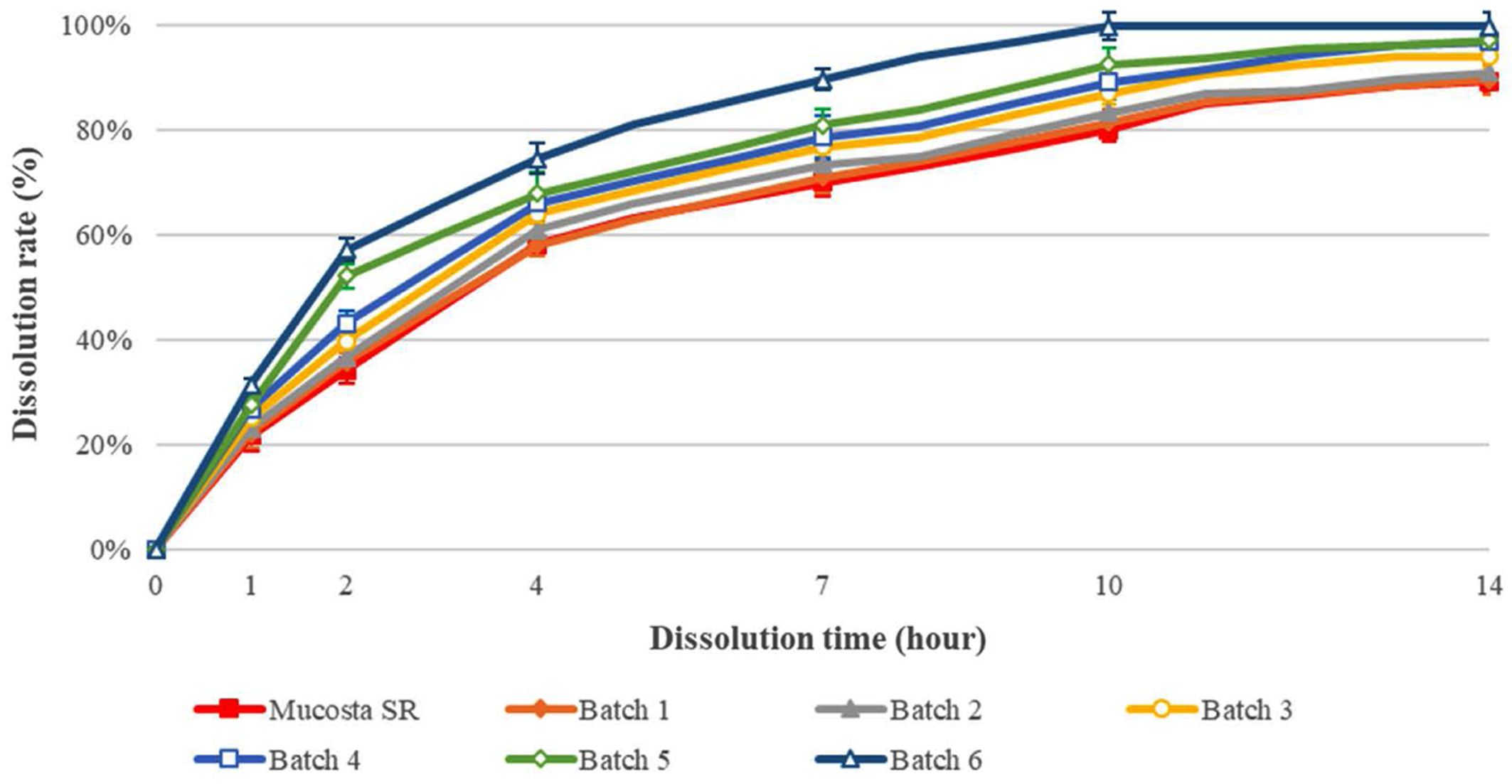
REB-SD 서방정의 용출 평가. REB-SD 서방정(Batch 1~6)의 용출 테스트는 Figure 4와 같다. REB-SD 서방정의 용출 초기에는 빠른 용출 속도를 보였으나, 모든 제형이 방출 속도가 조절되며 약 70~90% 이상의 누적 용출률을 14시간에 걸쳐 지속적인 약물 방출을 나타내며, HPMC의 영향으로 용출의 후반부로 갈수록 방출 속도가 완만하게 유지되는 1차 방출 패턴의 서방화 효과가 뚜렷하게 관찰되었다.14,15,24 이는 HPMC 매트릭스가 수화되며 겔을 형성하여 약물 확산을 지연시키는 HPMC의 기전과 일치한다. 그리고 고체분산체의 용해도가 높을수록 서방정의 용출률이 증가함을 확인하였다.23,24
|
Figure 1 FTIR spectra of (a) raw materials: REB, HPMC, SLS, Cremophor RH 40, Poloxamer 188, 407; (b) REB-SD: Batch 1~ Batch 6. |
|
Figure 2 XRD result of (a) raw materials: REB, HPMC, SLS, Poloxamer 188, 407; (b) REB-SD: Batch 1~Batch 6 |
|
Figure 3 DSC result of (a) raw materials: REB, HPMC, SLS, Cremophor RH 40, Poloxamer 188, 407; (b) REB-SD: Batch 1~Batch 6. |
|
Figure 4 Dissolution test of Mucosta SR and REB-SD SR tablet (Batch 1~6). |
|
Table 2 Solubility Test of REB and REB-SD (Batch 1~Batch 6) in Water (unit: μg/mL) |
|
Table 3 BD/TD of the Final Blend and Compression Result of the REB-SD SR Tablet (Batch 1~6) |
본 연구는 HME기반 고체분산체와 HPMC 매트릭스 서방화 기술을 결합하여 REB의 낮은 수용성과 짧은 작용 지속성을 동시 개선하는 제형의 가능성을 입증했다. pH 조절을 통한 약물 용해도 개선, 계면활성제의 가용화, HME로 달성된 비정질화 및 HPMC에 의한 약물 방출 지연을 결합하여 복합적으로 작용해 용해도와 용출 증대 및 용출 특성이 개선되었으며, 그 결과 용출 증대와 1일 2회 투여를 목표로 한 약 14시간의 서방화 용출이 구현되었다.
먼저, REB의 용해도증가에 따른 용출률 증대는 뚜렷하게 나타났다. HPMC 만으로 제조한 고체분산체는 기존의 REB보다 3배 내외의 용해도 증가가 관찰되었고, HPMC와 NaOH이 첨가된 배치 Batch 2에서는 pH조절에 따른 이온화도의 증가로 용해도가 REB대비 약 9배 상승하였다. 여기에 계면활성제를 추가(Batch 3~6)하자 계면장력 저하효과로 인해 약물 용해도가 REB대비 약 10~19배까지 개선되었다. 이러한 용해도 증대는 서방정에서도 전체 방출 속도 증가로 이어졌으며, 특히 Poloxamer 407이 처방된 Batch 6의 경우 REB의 용해도 증대에 따라 방출 속도가 증가하여 10시간만에 모든 방출이 완료되었다. 이는 용출 구동력(용해도/활성도 차)이 커질수록 HPMC 겔층 내 확산이 증가한다는 점에서 일치한다.25
정제 공정성 측면에서는 모든 배치의 최종 분체가 Carr index / Hausner ratio 기준 possible~good의 유동성을 보였으며 직타에도 적합하였다. 다만 HME 필름 분쇄체의 취성으로 HPMC의 압축성에 대한 기대만큼의 압축성은 제한적이었고, 정제 경도 170N(최대 182~209N) 달성에 타정압 6.1~6.6 kg/cm-2이 필요하였다. 이전에 Spray drying method로 제조한 고체분산체와 비교하여 보았을때, 타정성이 비교적 낮은 것을 확인하였다.21 이는 HME로 제조한 고체분산체의 취성과 관련이 있을 것으로 사료되며, 추후 스케일업 시 고체분산체 또는 최종 분체에 소량의 가소제 및 압축 보조 부형제등의 도입을 통해 고체분산체의 취성 완화 및 타정성 제어를 검토할 필요가 있다.22,23
본 연구를 통해 HME로 제조한 REB-SD와 HPMC 매트릭스의 결합은 REB의 용해도 증대와 지속 방출을 동시에 달성할 수 있는 전략임을 확인하였다. 고체분산체 제조를 통한 가용화와 HPMC 겔층 확산의 시너지가 성능 개선의 근거이다. 본 연구의 열 용융 압출 REB-SD 서방정 기술은 추후 공정, 안정성 및 위장 환경 변수를 체계적으로 다듬으면 임상적 및 상업적 확장성이 높은 플랫폼으로 발전 가능한 전략이다.
- 1. Stielow, M.; Witczynska, A.; Kubryn, N.; Fijalkowski, L.; Nowaczyk, J.; Nowaczyk, A. The Bioavailability of Drugs—The Current State of Knowledge. Molecules. MDPI. 2023, 28, 8038.
-

- 2. Gomez-Orellana, I. Strategies to Improve Oral Drug Bioavailability. Expert Opin. Drug Deliv. 2005, 2, 419-433.
-

- 3. Naito, Y. Yoshikawa, T. Rebamipide: A Gastrointestinal Protective Drug with Pleiotropic Activities. Expert Rev. Gastroenterol. Hepatol. 2010, 4, 261-270.
-

- 4. Matysiak-Budnik, T.; Heyman, M.; Megraud, F. Review Article: Rebamipide and The Digestive Epithelial Barrier. Aliment. Pharmacol. Ther. 2003, 18, 55-62.
-

- 5. Kumar, P.; Chaudhary, M.; Badola, A. Method Development and Formulating Rebamipide Sustained Release Tablets and Its Evaluatuin. IJPSR. 2021, 12, 1044-1052.
-

- 6. Seok, S. H.; Ha, J.; Kim, G.; Kim, B. H.; Lee, D. W.; Choi, M.; Lee, S. Kim, J.; Park, E. Effect of Gastric Residence Time on The Oral Absorption of Rebamipide Sustained-Release Tablets in Beagle Dogs. J. Pharm. Investig. 2021, 51, 759-766.
-

- 7. Moon, B.; Son, Y.; Kim, S. J.; Park, S.; Kim, W. K.; Song, J. E.; Khang, G. Formulation Design of pH Adjusted Rebamipide Solid Dispersions for Improved Solubility. Polym. Korea. 2024, 48, 299-304.
-

- 8. Tran, P. H. L.; Tran, T. T. D.; Lee, K. H.; Kim, D. J.; Lee, Beom. J. Dissolution-Modulating Mechanism of pH Modifiers in Solid Dispersion Containing Weakly. Expert Opin. Drug Deliv. 2010, 7, 647-661.
-

- 9. Nair, A. R.; Lakshman, Y. D.; Anad, V. S. K.; Sree, K. S. N.; Bhat, K.; Degale, S. J. Overview of Extensively Employed Polymeric Carriers in Solid Dispersion Technology. AAPS PharmSciTech. 2020, 21, 309.
-

- 10. Qi, Sheng.; Roser, S.; Edler, K. J.; Pigliacelli, C.; Rogerson, M.; Weuts, L.; Dycke, F. V.; Stokbroekx, S. Insights into the Role of Polymer-Surfactant Complexes in Drug. Pharm. Res. 2013, 30, 290-302.
-

- 11. Halagali, P. Sharannavar, B. R. The Hot Melt Extrusion (HME) in Pharmaceutical Technology: A Comprehensive Review. IJSAT. 2025, 16, 2.
-

- 12. Li, X.; Hong, X.; Shuai, S.; Han, X.; Li, C. Zhang, H. Wang, Z.; Ren, M.; Jin, L. Zheng, A. A Review of Hot Melt Extrusion Technology: Advantages, Applications, Key Factors and Future Prospects. J. Drug Deliv. Sci. Technol. 2024, 98, 105884.
-

- 13. Connell, P. O.; Yoon, J. H.; Geever, L. M.; Kumar, D.; Healy, A. M.; Serrano, D. R. Accelerated Predictive Stability (APS) Strategies Applied to Screening Pharmaceutical Formulations: A Comparison of Spray Dried and Hot Melt Extruded Nifedipine Amorphous Solid Dispersions. Int. J. Pharm. 2025, 126012.
-

- 14. Ratnaparkhi, M. P.; Jyoti, P. G. Sustained Release Oral Drug Delivery System - An Overview. IJPRR. 2013, 2, 11-21.
- 15. Pareek, S. P.; kumawat, S.; Sharma, V. Sharma, D. Rathore, D. S.; Agarwal, M. Review on Sustained Release Technology. Int. J. Pharm. Biol. Sci. Arch. 2019, 7, 29-38.
- 16. Zalte, H. D.; Saudagar, R. B. Review on Sustained Release Matrix Tablet, IJPBS. 2013, 3, 17-29.
- 17. Lu, Jiannan.; Obara, S.; Liu, F.; Fu, W.; Zhang, W.; Kikuchi, S. Melt Extrusion for a High Melting Point Compound with Improved Solubility and Sustained Release. AAPS PharmSciTech. 2018, 19, 358-370.
-

- 18. Chaudhari, S. P.; Dugar, R. P. Application of Surfactants in Solid Dispersion Technology for Improving Solubility of Poorly Water Soluble Drugs. J. Drug Deliv. Sci. Technol. 2017, 41, 68-77.
-

- 19. Liu, X.; Feng, X.; Williams III, R. O.; Zhang, Feng. Characterization of Amorphous Solid Dispersions. J. Pharm. Investig. 2018, 48, 19-41.
-

- 20. Shekunov, B. Y.; Chattopadhyay, P.; Tong, H. H. Y.; Chow, A. H. L. Particle Size Analysis in Pharmaceutics: Principles, Methods and Applications. Pharm. Res. 2007, 24, 203-227.
-

- 21. Moon, B.; Kim, W. K.; Son, Y.; Kim, S. J.; Park, S.; Song, J. E.; Khang, K. Research on Rebamipide Sustained-release Tablets Using Solubilization Technology and Gastric Retention System. Polym. Korea. 2025, 49, 59-66.
-

- 22. Mohan, S. Compression Physics of Pharmaceutical Powders: A Review. Int. J. Pharm. Sci. Res. 2012, 3, 1580-1592.
- 23. Iver, R.; Hegde, S.; Zhang, Y. E.; Dinunzio, J.; Singhal, D.; Malick, A.; Amidon, G. The Impact of Hot Melt Extrusion and Spray Drying on Mechanical Properties and Tableting Indices of Materials Used in Pharmaceutical Development. J. Pharm. Sci. 2013, 102, 3604-3613.
-

- 24. Vlad, R. A.; Pintea, A.; Pintea, C.; Redai, E. M.; Antonoaea, P. Birsan, M. Ciurba, A. Hydroxypropyl Methylcellulose—A Key Excipient in Pharmaceutical Drug Delivery Systems. Pharm. 2025, 17, 784.
-

- 25. Tran, P. H. L., Tran T. T. D.; Park, J. B.; Lee, B. J. Controlled Release Systems Containing Solid Dispersions: Strategies and Mechanisms. Pharm. Res. 2011, 28, 2353-2378.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2024 Impact Factor : 0.6
- Indexed in SCIE
 This Article
This Article
-
2026; 50(2): 348-355
Published online Mar 25, 2026
- 10.7317/pk.2026.50.2.348
- Received on Dec 10, 2025
- Revised on Jan 26, 2026
- Accepted on Jan 28, 2026
 Services
Services
Shared
 Correspondence to
Correspondence to
- Gilson Khang
-
*Department of PolymerNano Science & Technology, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896, Korea
**Department of Bionanotechnology and Bio-Convergence Engineering, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896, Korea
***Polymer Materials Fusion Research Center, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896, Korea - E-mail: gskhang@jbnu.ac.kr
- ORCID:
0000-0002-6452-5653








 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.