- Solvent Size-Dependent Structure of Diblock Copolymer Micelles in n-alkanes
Department of Chemical Engineering, Hongik University, Seoul 04066, Korea
- 알칸 용매 내에서 용매 크기에 따른 블록공중합체 미셀 구조 연구
홍익대학교 화학공학과
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
The solvent size dependence of micellar structure formed by poly(styrene-b-ethylene-alt-propylene) (PS-PEP) block copolymer in n-alkane (n = 8, 10, 12, 14, 16), selective to the PEP block, was investigated using small-angle x-ray scattering and static light scattering (SLS). As the molecular weight of n-alkane decreases, the estimated Flory-Huggins interaction parameter between the solvent and the PS blocks increases, but the solvent penetration into the PS core becomes feasible due to the solvent entropy effect. This study reveals that the systematic control of oil molecules can tune the micellar structure and critical micelle temperature.
Poly(styrene-b-ethylene-alt-propylene)(PS-PEP) 블록공중합체는 알칸 용매 내에서 PS 코어와 PEP 코로나를 갖는 나노미터 크기 미셀을 형성한다. 본 연구에서는 소각 X선 산란법(SAXS)과 정적 광 산란법(SLS)을 이용하여 n-alkane(n=8, 10, 12, 14, 16) 내에서 용매 크기에 따른 PS-PEP 미셀의 구조를 분석하였다. 이론적으로 오일의 분자량이 작을수록 고분자와의 계산된 Flory-Huggins 상호작용 파라미터가 증가하지만, 용매의 엔트로피 효과에 의해 용매 분자가 미셀 코어로 쉽게 침투할 수 있다. 따라서, 알칸 유기용매의 분자량 조절을 통해 미셀의 구조 및 임계 미셀 온도를 체계적으로 제어할 수 있다.
The solvent size dependence of micellar structure formed by poly(styrene-b-ethylene-alt-propylene) (PS-SEP) block copolymer in n-alkane (CnH2n+2, n = 8, 10, 12, 14, 16) is investigated using small-angle X-ray scattering. Although the estimated Flory-Huggins interaction parameter (¥ö) between the solvent and the PS blocks increases with decreasing the molecular weight of n-alkane, the solvent penetration into the PS core plays a crucial role to determine the micellar structure.
Keywords: poly(styrene-b-ethylene-alt-propylene), block copolymer micelle, self-assembly, small-angle X-ray scattering, static light scattering.
본 연구는 한국연구재단 선도연구센터지원사업(NRF-2018R1A5A1024127)과 홍익대학교 학술진흥연구비에 의하여 진행되었으며, 이에 감사드립니다.
저자들은 이해상충이 없음을 선언합니다.
Detailed characteristics of PS-PEP, SAXS results of SEP-1 and SEP-2 micelle solutions, and Zimm-plot are shown in Supporting Information. 이 자료는 다음 사이트에서 얻을 수 있습니다(http://journal.polymer-korea.or.kr).
PK_2022_046_01_135_Supporting_Information_template.pdf (529 kb)
Supplementary Information
블록공중합체는 한 종류의 고분자가 다른 종류의 고분자와 공유결합을 통해 결합된 형태이며, 선택적 용매 안에서 한쪽 블록은 용해되고 다른 한쪽 블록은 상분리가 발생하여 자기조립 미셀을 형성한다. 미셀은 수 나노미터에서 수백 나노미터의 크기를 가지며, 온도, pH 등 외부 자극에 민감하게 반응하여 나노구조체의 크기 및 모양을 바꿀 수 있다.1-4 따라서, 약물과 유전자 전달체, 나노리소그래피, 오일의 점도 개선제 등 다양한 응용분야에서 활발히 이용되고 있다.5-10 블록공중합체 미셀에 대한 연구내용은 여러 리뷰 논문을 통해 확인할 수 있다.5-8
선택적 용매 안에서 형성된 블록공중합체 미셀의 구조를 결정하는 대표적인 요소는 코어 블록의 뻗침 정도, 코어 블록과 코로나 블록 사이의 계면 장력, 코로나 블록 사이의 부피 배제 효과가 있다.8-12 대표적으로, 엔트로피 효과에 의해 코어 블록은 Gaussian conformation 형태를 가지려 하지만, 엔탈피 효과로 코어 블록은 계면에서 멀어지는 stretched conformation 형태를 갖고자 한다. 이 둘간의 적절한 합의점에서 코어 반지름(Rc)과 응집된 사슬 수(aggregation number, Nagg), 전체 반지름 등 미셀의 열역학적 평형 구조가 결정된다. 이러한 효과를 고려하여 Halperin 등은 구형 미셀의 구조와 블록공중합체 디자인(예를 들어, 코어 블록의 반복 단위 수(Ncore)와 계면 장력(γ))의 상관관계에 관한 scaling theory를 제시하였다.12 코어 블록의 길이가 코로나 블록의 길이보다 충분히 짧은 경우(즉, hairy micelle)는 Rc~γ2/5M3/5core와 Nagg~ γ6/5N4/5core로 예측하였고, 반대로 코어 블록의 길이가 긴 경우(즉, crew-cut micelle)는 Rc~γ2/5N3/5core와 Nagg~γ6/5N4/5core로 예측하였다. 실험적으로도 블록공중합체의 디자인과 선택적 용매의 상호작용에 따른 미셀의 구조가 scaling theory의 예측과 일치하는 결과들이 보고되었다.13-17 Lund 등은 poly(ethylene-alt-propylene-b-ethylene oxide) (PEP-PEO) 블록공중합체를 물과 디메틸포름아마이드(N,N-dimethylformamide, DMF)의 이성분계 혼합 용매에서 DMF의 부피 분율에 따른 미셀 구조 분석을 통해 Nagg~γ6/5를 관찰하였고, 이는 제안된 scaling theory와 잘 부합한다.18 하지만, Nagg가 계면 장력이 낮은 구간에서는 scaling theory와 잘 맞지 않는 결과도 보고하였다. 또한, Kelly 등은 poly(butadiene-b-ethylene oxide)(PB-PEO) 블록공중합체를 물과 테트라하이드로퓨란(tetrahydrofuran, THF)용매의 이성분계 혼합 용매에서 THF의 부피 분율을 바꾸며 미셀 구조를 관찰하였고, 코어의 반지름이 계면 장력과 Rc~γ2/5의 관계를 갖는 것을 관찰하였다.19
대부분의 scaling theory는 미셀 코어에 용매가 침투하지 않는 것을 가정하고 있지만, 열역학적으로 용매 침투는 가능하며 미셀의 구조 및 임계온도(critical micelle temperature, CMT)에 영향을 줄 수 있다.20-25 Cooksey 등은 poly(ethylene oxide-b-caprolactone)(PEO-PCL) 블록공중합체를 물과 THF의 이성분계 용매 안에서 중성 용매인 THF의 분율을 바꾸어 가며 코어 내 용매 침투와 구조에 따른 거동을 관찰하였다.20 THF의 비율이 10에서 50%까지 증가하면 코어 내 용매 분율은 20%에서 70%까지 증가하며, 미셀의 사슬 응집수는 270개에서 90개까지 감소하였다. Choi 등은 polystyrene-b-(ethylene-alt-propylene)(SEP) 블록공중합체가 선택적 용매인 스쿠알란과 중성 용매인 도데실벤젠 안에서 미셀을 형성하였을 때, 도데실벤젠 부피 분율이 증가할수록 코어 내부의 용매 분율이 증가하고, CMT는 점진적으로 감소하는 것을 보고하였다.22 Quintana 등은 n-alkane에서 SEP 블록공중합체 미셀 구조를 관찰하여, 용매의 분자량이 작아질수록 CMT 및 Nagg가 감소하는 것을 보고하였다.23 Lund 등은 n-alkane 안에서 polystyrene-b-polybutadiene(PS-PB) 블록공중합체 미셀의 구조 분석을 통해, 용매의 분자량이 작아질수록 코어 내부의 용매 분율은 증가하고, Nagg는 감소함을 보고하였다.24 용매의 크기가 작아질수록 코어 블록과 용매 사이의 계산된 상호작용 파라미터(χcore-solvent)는 증가하기에 기존 scaling theory로는 이러한 결과를 설명하기 어렵다. Lund 등은 이러한 불일치를 용매가 미셀 코어로 침투하는 엔트로피 영향을 이용하여 설명하였다.24 또한 용매의 크기에 따른 코어 안 용매 침투 효과는 동종 중합체의 용해 연구에서 예상할 수 있다. Imre 등은 PS 동종 중합체를 n-octane과 2,3,4-trimethylpentane에서 각각 용해되는 온도를 측정하였다. 이때, n-octane과 2,3,4-trimethylpentane의 용해도 상수는 각각 15.7와 15.6 MPa0.5로 비슷하지만, 용해되는 온도는 285와 262 K로 몰 부피가 작은 이성질체 용매에서 더 잘 용해되었다.25 이처럼 용매가 미셀 코어로 침투하는 것이 용이한 경우, χ에 따른 이론적 거동만으로는 미셀 구조의 예측이 어렵기 때문에 용매의 크기를 체계적으로 조절해가며 미셀의 구조를 연구할 필요가 있다.
본 연구에서는 SEP 블록공중합체와 다양한 크기의 n-alkane 용매를 이용하여 용매의 크기에 따른 미셀의 구조를 연구하였다. 소각 X선 산란법(small-angle X-ray scattering, SAXS)과 정적 광 산란법(static light scattering, SLS)을 이용하여 다양한 온도에서 미셀의 크기 및 특징들을 측정하고 분석하였다. 용매의 크기에 따른 미셀 구조 변화 연구는 미셀의 응용분야를 넓히는데 기초자료로 사용될 수 있다.
PS-PEP 블록공중합체. PS의 부피 분율이 서로 다른 두 SEP 블록 공중합체를 리빙 음이온 중합과 선택적 수소화 반응을 통해 합성하였으며, 선행 연구논문에 자세하게 기록되어있다.26 분자량 분포는 THF를 이동상으로 하는 겔 투과 크로마토그래피(gel permeation chromatography, GPC, JASCO, Japan)를 이용하여 측정하였으며, PS와 PEP의 블록 비율은 1H NMR(500 MHz, Inova 500, USA)을 이용하였다. 본 연구에서 이용한 블록공중합체는 PS와 PEP이 각각 17 kg/mol과 75 kg/mol인 SEP-1과 26 kg/mol과 68 kg/mol인 SEP-2이다. 이들의 PS 및 PEP 블록의 밀도를 각각 1.047 g/cm3와 0.856 g/cm3로 가정하였을 때, SEP-1의 PS 부피 분율은 0.16이고 SEP-2의 PS 부피 분율은 0.24로 계산되었다.27 그리고 SEP-1과 SEP-2의 다분산 지수는 각각 1.05와 1.14로 Figure S1에 결과를 첨부하였다.
미셀 샘플 제조. 분자량이 다른 5종의 n-alkanes(CnH2n+2, n=8, 10, 12, 14, 16, Sigma Aldrich, USA)을 용매로 이용하였다. n-octane, n-decane, n-dodecane, n-tetradecane, n-hexadecane는 각각 OC, DE, DD, TD, HD로 표시하였다. 모든 샘플들은 1 wt%의 고분자 농도로 고분자 및 선택적 용매를 넣은 뒤, 공용매인 염화메틸렌을 소량 투입하여 교반 후 공용매를 증발시켰다. CMT까지 가열 후, 상온까지 천천히 식히는 열처리를 통해 재현성있는 잘 정의된 미셀 용액을 제조하였다.22,26
정적 광 산란(Static Light Scattering, SLS). SLS 측정은 multi-angle light scattering(BI-200SM, Brookhaven, USA, 레이져 파장(λ0)=636 nm)을 이용하여 상온에서 산란각도(θ) 30o와 120o 사이에서 측정하였다. 모든 샘플들은 0.45 μm 필터 투과 후, 0.5 wt%의 미셀 용액을 묽혀가며 계획된 고분자 농도(c) 용액을 만들어 산란세기를 측정하였다. Zimm plot은 아래 식에 의해 완성하였다.
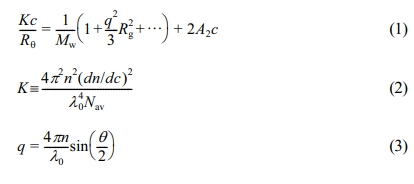
이때, Rθ, n, q, Rg, A2는 는 각각 Rayleigh ratio, 용매의 굴절율, scattering wave vector, radius of gyration, second virial coefficient이다. 용매인 OC, DE, DD, TD, HD의 굴절률은 각각 1.398, 1.412, 1.421, 1.429, 1.434이다. dn/dc는 고분자의 농도를 0.6, 0.5, 0.3, 0.2 mg/mL로 바꾸어가며, 굴절계(Abbemat 300, Anton Paar, Austria)로 측정하였으며, OC, DE, DD, TD, HD의 mL/mg는 각각 0.118, 0.125, 0.077, 0.099, 0.090 mL/mg이다. Rayleigh ratio 값은 고순도 톨루엔 (99.9≤, Sigma Aldrich, USA)을 이용하여 보정하였고, 636 nm 파장에서 1.372×105 cm-1으로 보고된 값과 거의 일치 한다.28 Zimm-plot을 통해 미셀의 Mw을 측정하여, 상온에서의 Nagg 값을 구하였다(Figure S4).
소각 X선 산란(Small-Angle X-ray Scattering, SAXS). SAXS는 포항 가속기 연구소(Pohang Accelerator Laboratory, PAL, Korea)의 9A-USAXS와 4C-SAXS 빔 라인에서 측정하였다. 빔 파장은 각각 0.621 Å와 0.734 Å이었고, 샘플과 검출기 사이의 거리는 4.52 m와 4.37 m였으며, 측정 q 범위는 0.009 Å-1 < q < 0.110 Å-1 이다. 모든 샘플들은 측정 전 3분 동안 열처리 하였으며, 최대 60초 동안 X선에 노출하였다. 모든 샘플들은 붕규산 모세관에 담아 봉인 후, 계획된 온도에서 측정하였다. 그리고 얻어진 등방성 2D 이미지는 1D의 q에 따른 산란세기로 환원되었고, glassy carbon을 이용하여 절대 산란세기로 환원하였다.
분석에 이용한 피팅 모델은 선행연구에서 소개된 구형 미셀 모델을 이용하였으며, 다분산의 반지름을 갖는 구형 코어와 표면에 흡착된 고분자 사슬을 가정하고 있다.26 구체적인 모델식은 Pedersen 모델을 기반으로 하였으며 아래와 같다.29
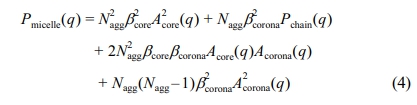
위 식은 구형 미셀의 형태함수로 4개의 상호작용을 고려한다. 코어 사슬의 자기상관 관계, 코로나 사슬의 자기상관 관계, 코어-코로나 블록 간 상호작용, 코로나 사슬 간 상호작용이 이에 해당하며, 각 형태함수의 자세한 식은 아래에 나타내고 있다. 또한, Nagg와 β는 각각 사슬 응집 수와 총 과잉 산란 길이이며 β는 아래와 같이 정의된다.
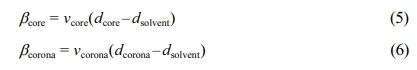
여기서 ν와 d는 각 블록의 볼륨과 산란 길이 밀도를 의미한다.
식 (4)의 첫번째 항은 반지름 Rc를 갖는 구형 코어의 자기 상관 함수와 계면에서 부드럽게 감소하는 산란 길이 밀도를 포함하며, 구형 미셀 코어의 형태함수 A2core는 아래와 같이 표현된다.
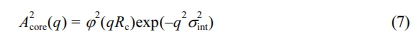
여기서 구의 형태함수는 φ= 3[sin(q2R2c -q2R2ccos(q2R2c)]/(q2R2c)3으로 정의된다. σint는 코어-코로나 계면 두께를 의미한다. 식 (4)의 두 번째 항은 코로나 사슬의 자기상관 함수이고, 코로나 사슬의 형태함수 Pchain(q)는 아래와 같다.
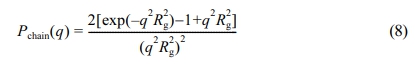
코로나 사슬의 경우 Gaussian conformation으로 가정하여 Debye function모델을 적용하였으며, 여기서 Rg는 코로나 사슬의 radius of gyration이다. 식 (4)의 세 번째 항은 코어와 코로나 블록 간 상호작용을 나타내고, 네 번째 항은 코로나 사슬 사이의 상호작용을 나타낸 부분이다. 이때 공통적으로 표현한 코로나 사슬의 형태함수 Acorona(q)는 아래와 같이 정의된다.
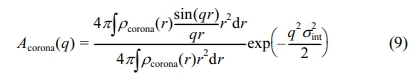
여기서 ρcorona(r)은 코로나 사슬의 방사형태 밀도분포를 normalized Fourier transform하여 나타낸 함수이다. 이 연구에서 용매에 잘 녹아있는 코로나 사슬의 형태를 고려하여 2개의 3차 b-spline 함수를 선형조합하여 이용하였으며, 사전연구에서도 잘 적용되었다.30 따라서, 산란세기 I(q)는 다음과 같이 정의된다.
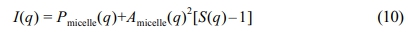
여기서 Amicelle(q)은 micelle form factor amplitude의 방사상 산란 길이 분포를 나타낸 함수이다. 이는 아래와 같이 정의 된다.
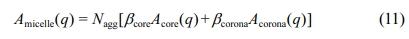
그리고 S(q)는 미셀의 공간상 분포와 관련된 함수로써, 반지름 Rhs인 구와 부피 분율 ηhs로 표현된 structure factor이다. 미셀 반지름의 다분산성을 표현하기 위해 아래와 같은 가우스 정규분포를 도입하였다.
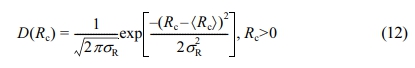
여기서
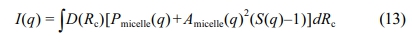
마지막으로, 최종 함수에 prefactor를 적용하여 model fitting을 진행하였고, prefactor는 상온에서 SLS로 측정한 Nagg값을 이용하여 결정하였다. 참고로, SLS를 통해 측정한 Nagg는 SEP-1이 OC, DE, DD, TD, HD 안에서 각각 44, 51, 60, 74, 71이고 SEP-2는 각각 94, 88, 82, 75, 72이다. 각 샘플에 대해 상온에서 결정한 prefactor는 측정된 모든 온도에 일괄 적용하였다.
SEP 블록공중합체는 n-alkane 용매 내에서 PS 코어와 PEP 코로나를 갖는 구형 미셀을 형성한다.22,25 본 연구에서 미셀의 구조를 결정하는 변인은 온도와 n-alkane의 종류이기 때문에, n-alkane과 SEP의 블록간 Flory-Huggins interaction parameter(χ)를 계산하였다. 용해도 상수를 이용하여 고분자와 용매 사이의 χ를 아래와 같이 정의할 수 있다.22,24,31-33
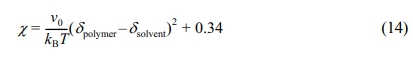
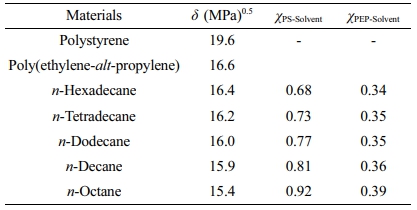
여기서 kB, T, δ는 볼츠만 상수, 절대온도, Hildebrand 용해도 상수이다. 또한, v0은 기준 부피로써 80 cm3/mol로 통일하였고, 상수 0.34는 고분자-용매 시스템에서 일반적으로 도입하는 값이다. Table 1은 각각의 용매와 PS, PEP 블록의 Hildebrand 용해도 상수와 계산된 χ값을 나타내었다. 용매의 크기가 커질수록 PS 코어 블록과 용매의 χ값은 작아지는 경향을 보인다.
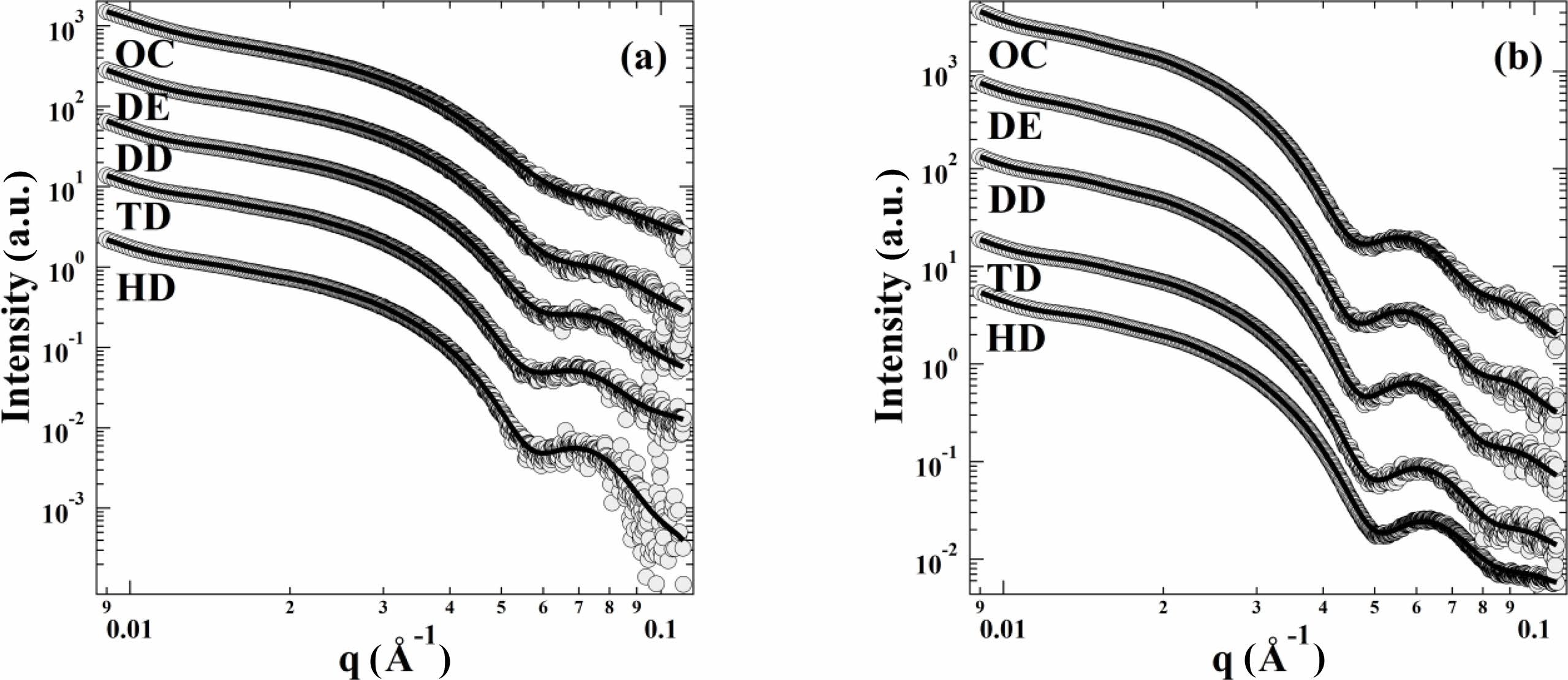
용매의 크기에 따른 미셀의 구조를 분석하기 위해 SAXS 측정을 진행하였고, Figure 1(a)와 1(b)는 각각 40 oC에서 SEP-1과 SEP-2의 용매에 따른 SAXS 결과이다. q>0.04 Å-1의 구간에서 첫번째 minimum을 포함하는 fluctuation이 명확하게 나타났으며, 용매의 크기가 작아질수록 첫번째 minimum이 점점 불분명해지는 것이 관찰되었다.26 SAXS 개형을 실험 파트에서 소개한 구형 미셀 모델로 fitting을 진행하였고, Figure 1에 결과를 실선으로 나타내었다. 모든 샘플의 온도에 따른 SAXS 개형은 Figure S2와 S3에 나타내었으며, fitting 결과는 Table S1과 S2에 나타내었다.
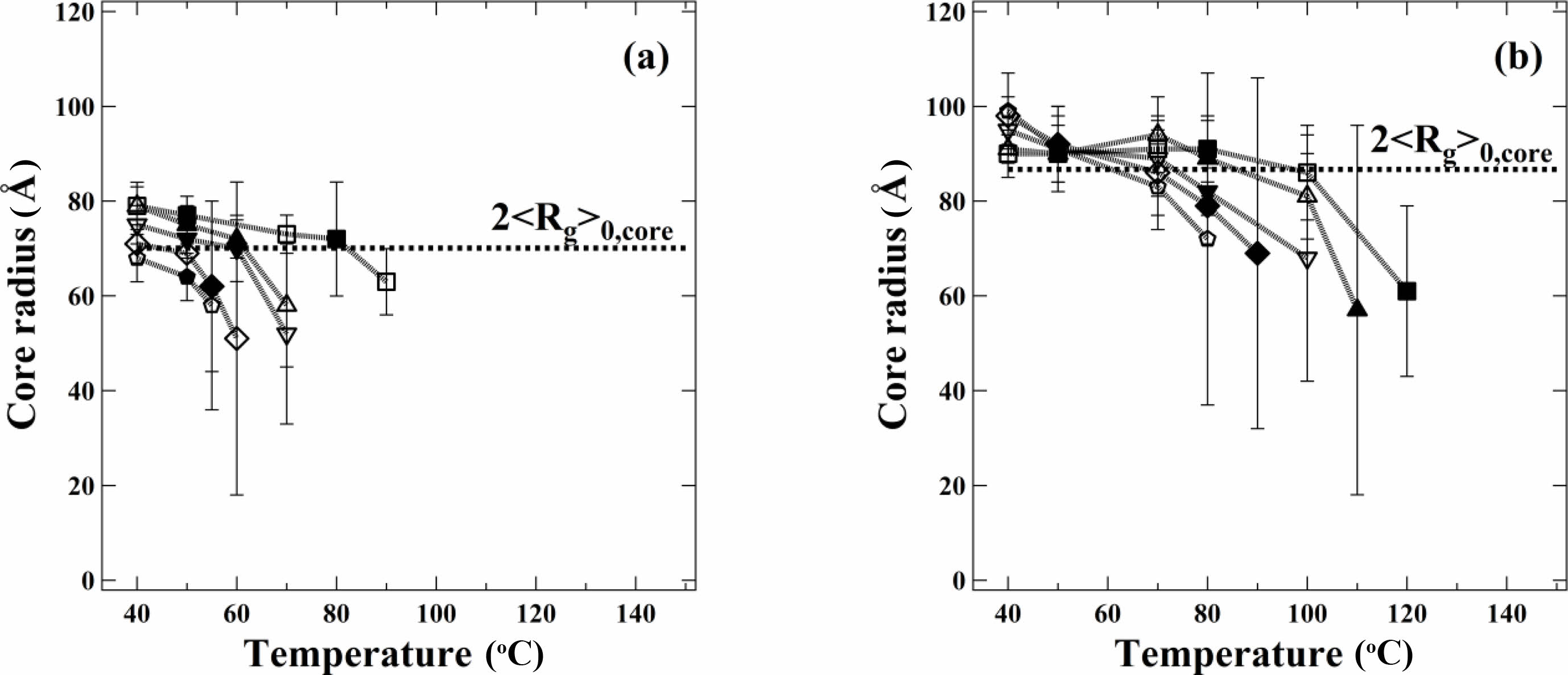
Figure 2는 가열 및 냉각 과정에서 (a) SEP-1과 (b) SEP-2 미셀의 온도에 따른 코어 반지름(Rc)을 나타내었다. 가열과 냉각과정에서 측정된 Rc가 거의 일치하므로, 미셀의 크기는 온도에 가역적으로 변하고 있음을 알 수 있다. SEP-1 미셀과 SEP-2 미셀은 용매 상관없이 온도가 증가할수록 Rc가 감소하며, 특정 온도이상에서는 fitting이 되지않는 미셀 해리 거동이 보인다. 식 (14)에 따르면 χ~1/T이므로, 온도가 증가할수록 chemical incompatibility가 작아지고 따라서 미셀의 크기는 감소하며, CMT 이상에서는 코어 블록도 용매에 녹기 때문에 미셀이 형성되지 않는다. 특이하게도 용매의 크기가 작아질수록 χ는 증가하였지만, Rc가 더 낮은 온도에서 급격히 감소하고, 따라서 CMT가 낮은 것을 확인하였다. SAXS 결과를 바탕으로 CMT를 정의하였을 때, SEP-1은 OC, DE, DD, TD, HD에서 각각 60, 65, 75, 80, 90 oC이고 SEP-2는 90, 100, 110, 120, 130 oC이다. 또한, Figure 2 점선은 용융 상태에서 PS의 Rg의 2배에 해당하는 값으로, 미셀의 코어 크기가 이와 비슷하다는 것은 코어 블록이 Gaussian conformation을 갖는다는 것을 의미한다.22,25 이는 과거 Choi 등의 SEP 블록공중합체를 스쿠알란 용매에서 온도에 따라 미셀의 거동을 관찰한 결과와 잘 일치한다.26
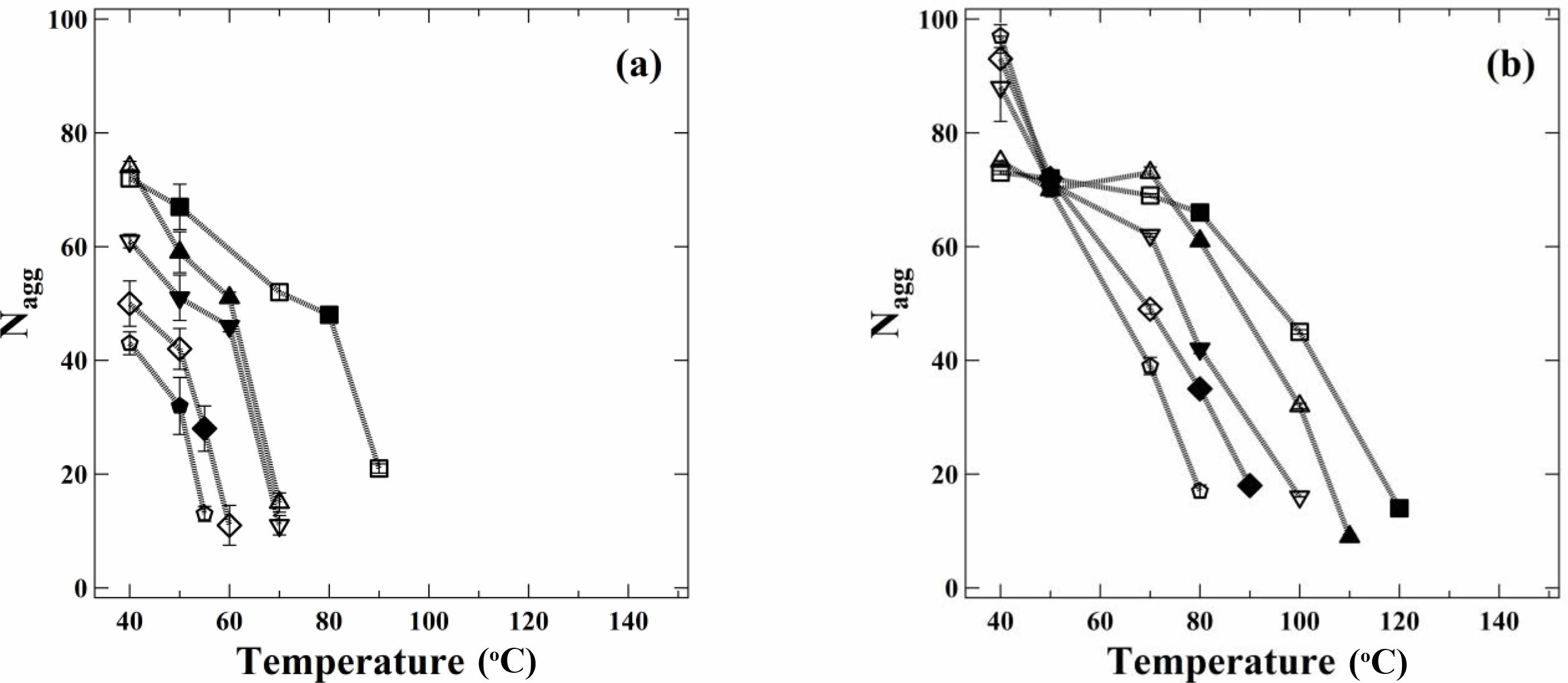
Figure 3은 가열 및 냉각 과정에서 (a) SEP-1과 (b) SEP-2 미셀의 Nagg를 나타내고 있다. SEP-1과 SEP-2 모두 온도가 증가하면서 CMT에 도달할 때까지 점진적으로 Nagg가 감소하였다. 또한, 코어가 유리 상태로 존재하는 상온을 제외하고는 SEP-1과 SEP-2의 미셀에서 용매의 크기가 작아질수록 Nagg가 작아진다. 과거 Quintana 등은 SLS를 이용하여 용매가 HD, DD, DE, OC, n-hexane으로 바뀔 때 Mw가 1.05×105 g/mol인 SEP 블록공중합체 미셀의 Mw를 관찰하였다. 용매의 크기가 작아질 때, 미셀의 Mw가 약 10×106 g/mol(Nagg=95)에서 6.0×106 g/mol(Nagg=57)로 감소한 결과를 보여주었다.23 또한, Lund 등은 PS-PB 블록공중합체를 20 oC일 때 HD, TD, DD, DE, n-heptane(HT)에서 Nagg가 각각 110, 106, 100, 85, 67로 감소하는 결과를 관찰하였다.24
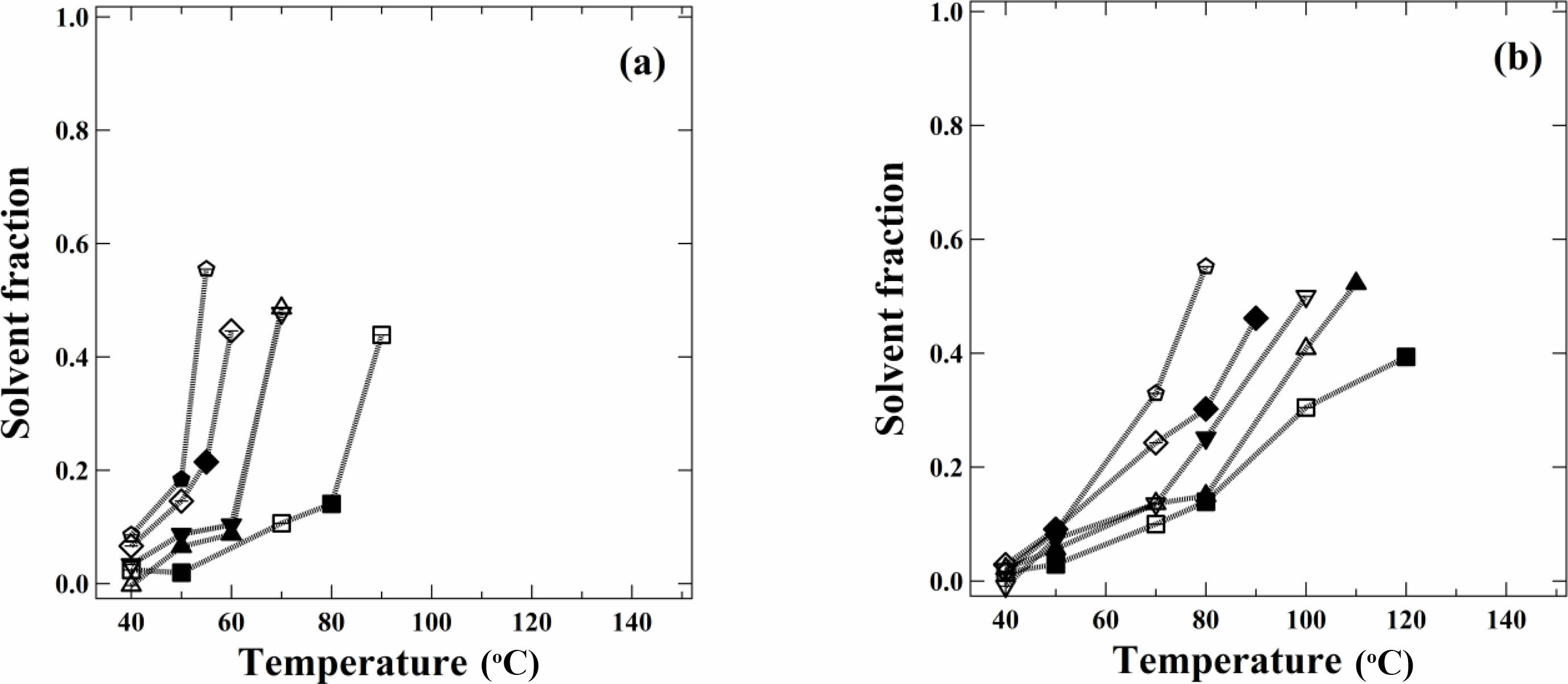
앞서 관찰한 Nagg와 Rc 결과를 이용하여 두 블록공중합체 미셀의 코어 내 용매 분율을 계산하였다.23,27 코어 내 용매 분율은 다음과 같이 정의되며, 이에 따른 계산 결과는 Figure 4에 나타내었다.
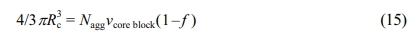
여기서 f는 코어 내 용매 분율, υ은 코어 블록의 부피이다. SEP-1과 SEP-2 미셀에서 코어 블록이 유리화에 가까운 상온에서는 코어 내 용매 분율은 0에 근접하며, 온도가 증가할수록 코어 내 용매 분율도 증가하였다. 이는 과거 다른 미셀 시스템의 결과와 잘 일치한다. 과거 Bang 등은 polystyrene-b-polyisoprene(PS-PI) 블록공중합체가 TD 용매 안에서 30 oC일 때, 코어 내 용매 분율은 0에 가깝게 나타남을 관찰하였다.30 Gang 등은 PS-PI 블록공중합체가 DE 안에서 미셀이 잘 정의되어 있을 때, 코어 내 용매 분율이 0.15 미만임을 확인하였다.34 Choi 등은 SEP 블록공중합체가 스쿠알란 용매 안에서 40 oC일때, 코어 내 용매 분율은 0에 가깝지만 CMT 근처에서 40%까지 급격하게 증가하는 결과를 확인하였다.22
온도 증가에 따른 코어 내 용매 분율의 증가는 온도 증가에 따른 χ값의 감소에 기인한다. 특이한 점은 용매의 크기가 작을수록 χ값은 증가하지만, 코어 내 용매 분율이 증가한다는 것이다. 과거 Lund 등은 20 oC에서 PS-PB 블록공중합체가 HD, TD, DD, DE, HT로 용매 크기가 감소할수록 χ가 0.58, 0.61, 0.65, 0.70, 0.81로 증가하지만 코어 내 용매 분율도 0.39, 0.41, 0.40, 0.51, 0.53으로 증가하는 것을 보고하였고, 이는 우리의 결과와 일치한다.24 이는 이론적으로 계산된 χ의 경향성과 달리 용매의 크기에 기인한 용매 분자의 엔트로피 효과가 미셀 구조에 큰 영향을 주고 있음을 알 수 있다.
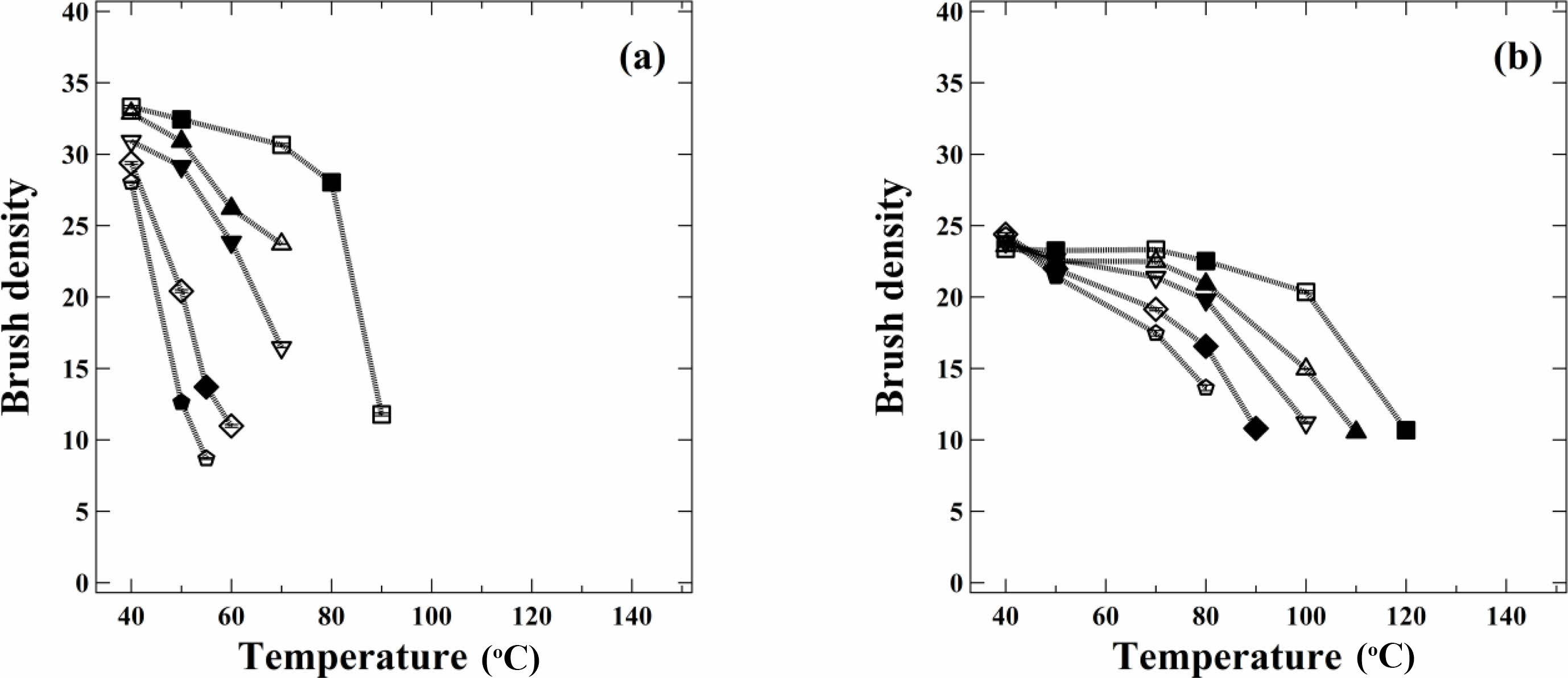
용매의 크기에 따른 코로나의 brush density를 아래의 식으로 계산하여 Figure 5에 나타내었다.26
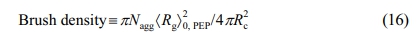
Brush density는 하나의 코로나 사슬이 코어 표면에서 차지하는 투영 면적을 의미한다. 여기서 <Rg>0, PEP는 용융된 상태에서 PEP사슬의 Rg이고 298 K에서 6
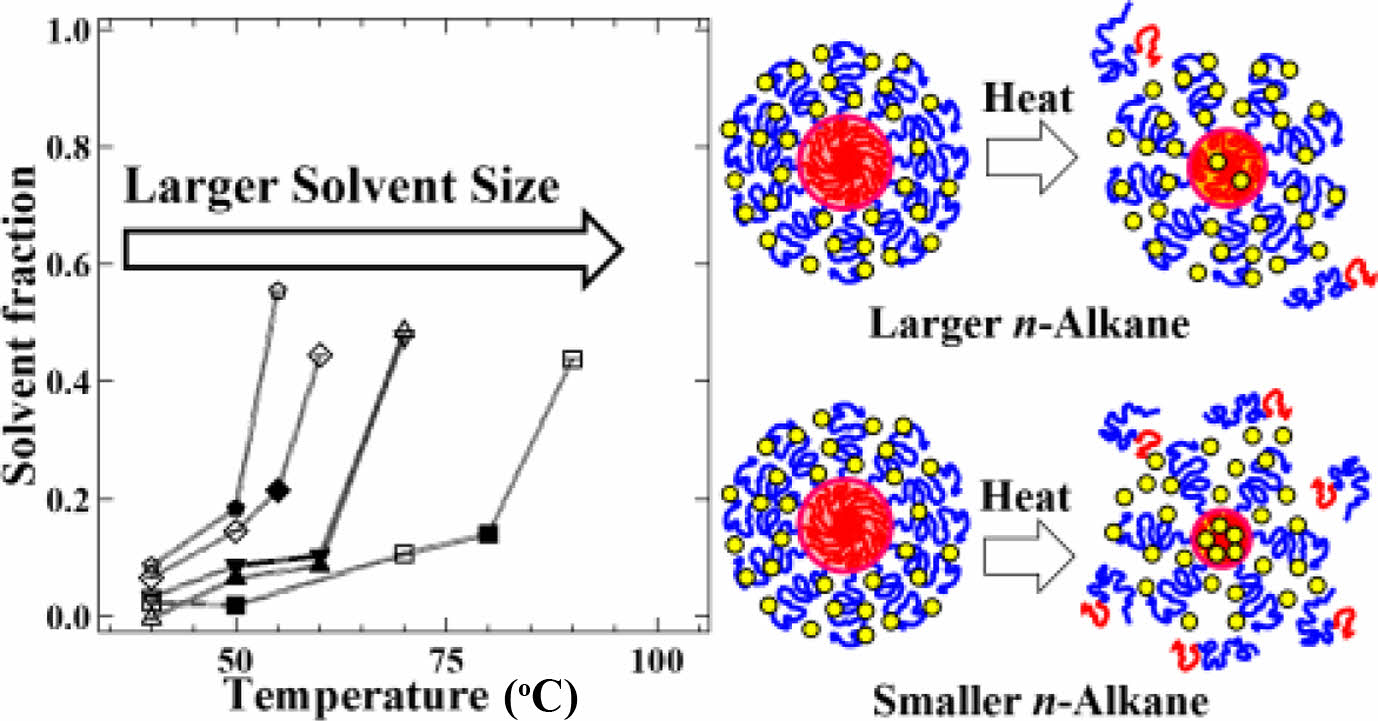
SAXS를 통한 미셀의 구조 결과들을 종합해볼 때 SEP-1과 SEP-2 미셀 모두 상온을 제외하면, 같은 온도에서 용매의 크기가 작아질수록 Rc, CMT, Nagg, brush density가 감소하고 코어 내 용매 분율이 증가하였다(Scheme 1). 이러한 현상은 Table 1에서 계산된 용매 크기에 따른 χ값의 경향과 반대 방향의 결과이며, 용매가 작아짐에 따라 용매 엔트로피 영향이 커지는 것을 반영하고 있다. 즉, 작은 크기의 용매가 코어 블록과 더 잘 섞일 수 있고, 결과적으로 코어 블록과 용매 간 계면 장력을 낮추는 역할을 한다. 이는 식 (14)에서 가정하고 있는 깨끗한 계면이 더 이상 유효하지 못함을 의미하며, 용매의 크기가 충분히 작고 코어 블록과 상용성이 높은 경우는 용매의 엔트로피 효과가 반영되어야 한다.
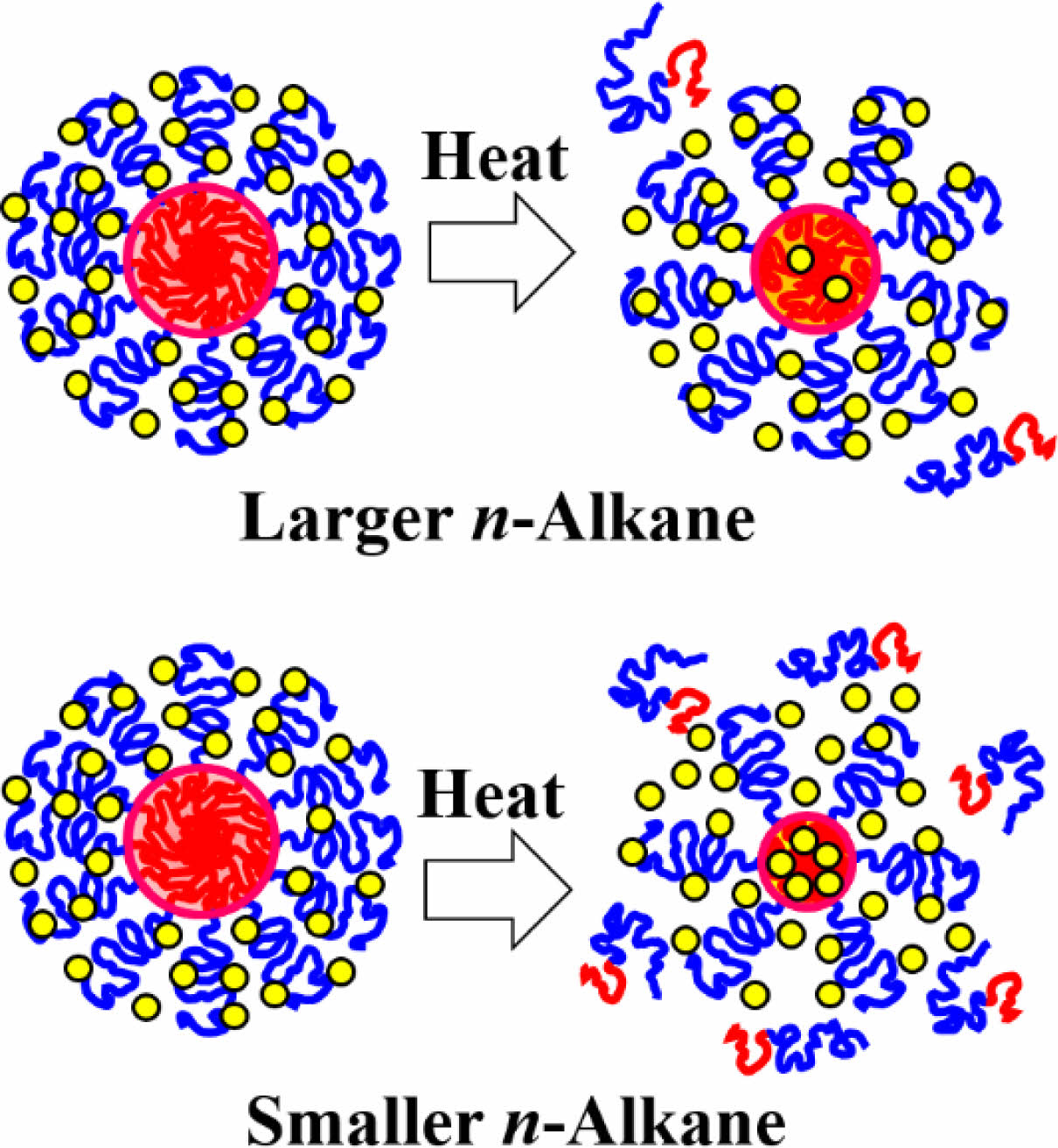
Scheme 1. Schematics of temperature dependent micelle structure in n-alkanes. At higher temperature, smaller n-alkane molecules are more penetrated into the cores.
용매의 엔트로피 효과는 용매의 코어 침투로 코어 블록의 유리전이 온도(Tg)가 감소하는 결과와 일치한다. Kambour 등은 PS 동종중합체를 n-pentane, n-hexane, n-heptane, n-octane을 이용해 용매의 크기에 따라 용해되는 정도를 연구하였다. 이때 n-pentane, n-hexane, n-heptane, n-octane 각각 용해도 상수는 14.36, 14.88, 15.34, 15.42로 보고하였으며, 용매의 크기가 감소할수록 PS와 χ가 증가한다. 하지만 작은 크기의 용매가 엔트로피 효과에 의해 침투하는 속도가 빠르며 용해가 더 잘되었다고 보고하였다.35 Evans 등은 poly(methyl meth- acrylate)-b-poly(tert-butyl methacrylate)(PMMA-PtBMA) 블록공중합체가 2-ethylhexanol 용매 안에서 형성한 미셀 코어의 Tg를 관찰하였다.36 일반적으로 PMMA의 Tg는 120 oC로 알려져 있으나 이 연구팀에서 PMMA 코어 블록의 Tg를 확인한 결과 약 21 oC 정도로 낮아졌고, 그 원인은 코어 내 침투한 약 30 vol%의 용매에 의한 것이라 보고하였다. Wang 등은 SEP 블록공중합체를 이용하여 스쿠알란과 도데실벤젠의 혼합 용매에서 미셀의 구조를 관찰하였다.21 이 연구팀의 결과에 따르면 코어 내 용매 분율이 0, 0.13, 0.21로 증가할 때, 코어의 유리전이 온도는 70, 37, 20 oC로 감소하였다.
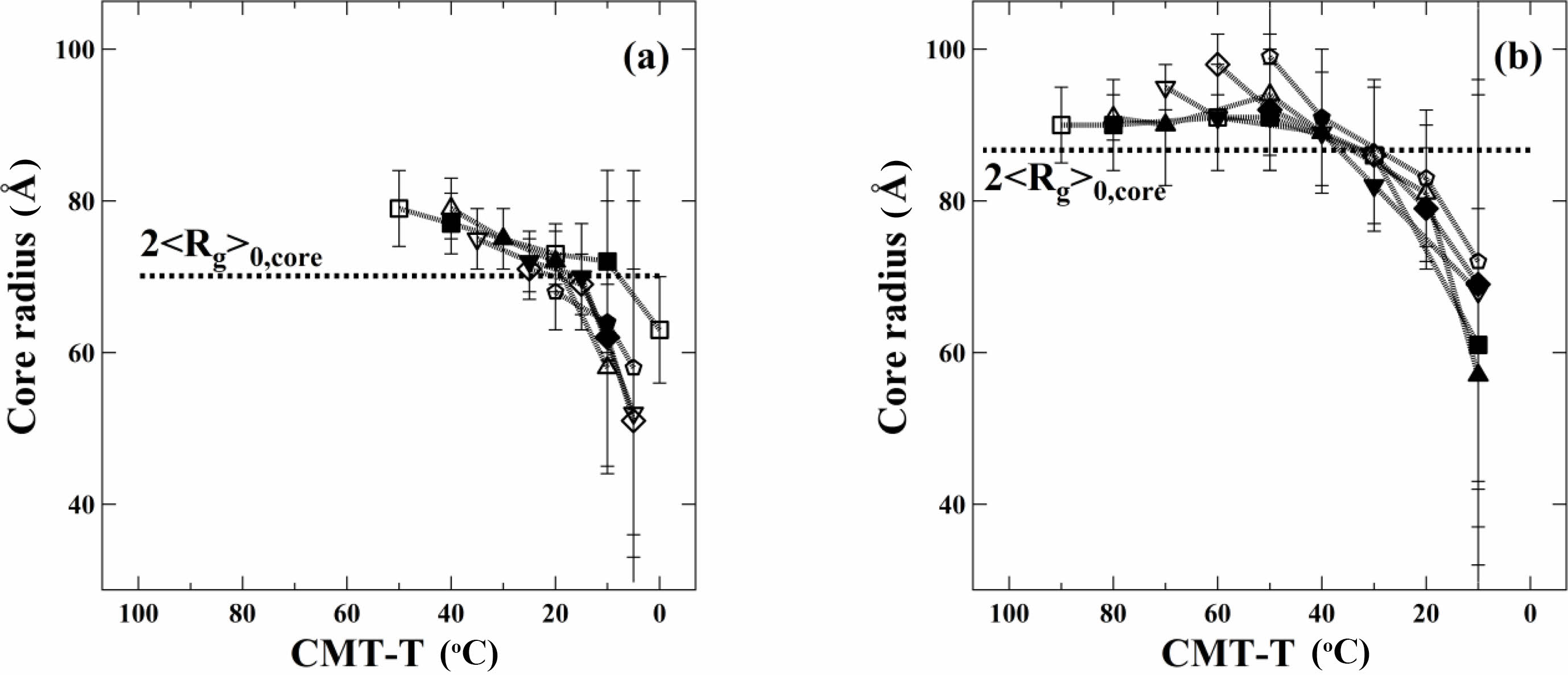
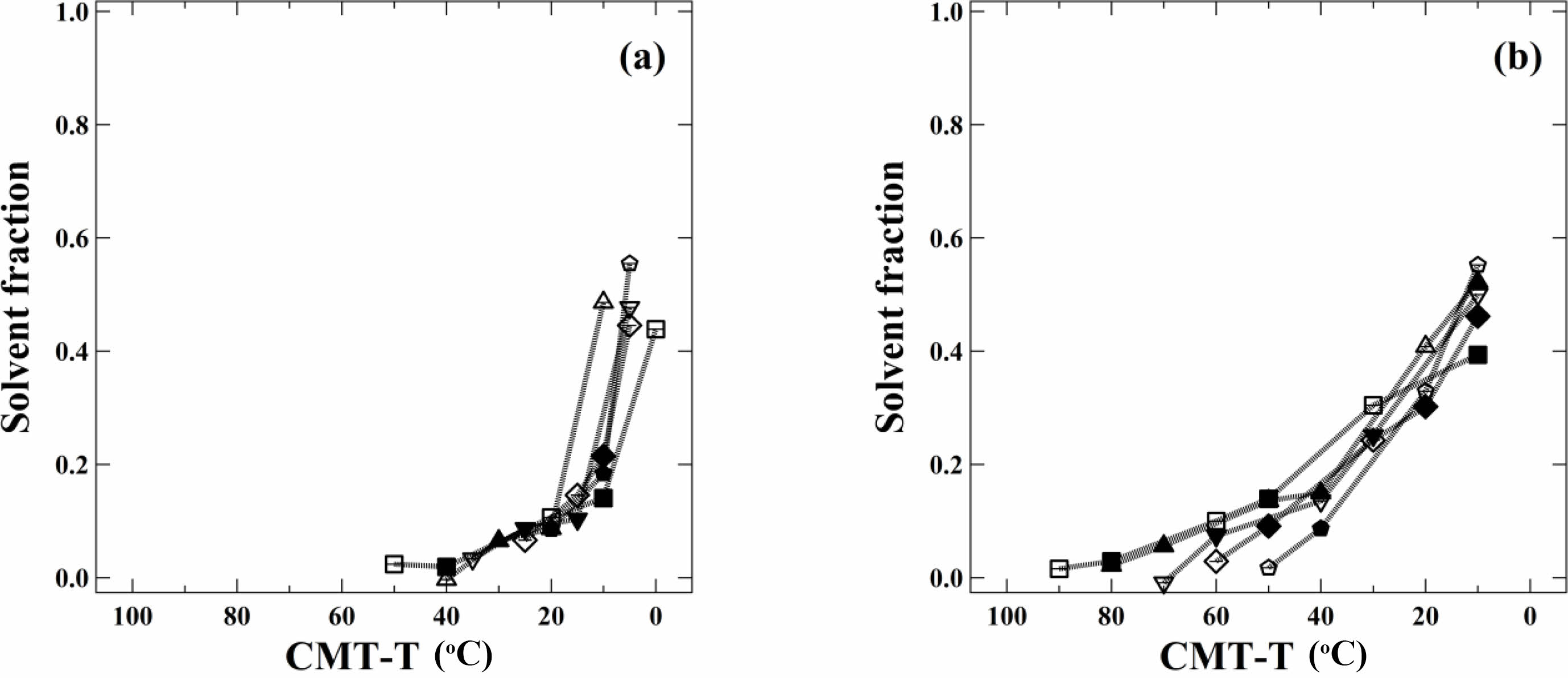
Figure 6과 Figure 7은 SEP-1과 SEP-2 미셀에서 Rc와 코어 내 용매 분율에 대하여 CMT-T를 x축으로 하여 다시 나타낸 결과이다. 대표적인 미셀 구조 파라미터가 오차범위 내에서 거의 일치하는 것을 확인할 수 있고, 이는 용매의 온도에 따른 상용성이 거의 동일하다는 것을 의미한다. 용매의 크기에 따라 CMT는 바뀌었지만, 용매의 화학적 구조가 비슷하기 때문에 CMT에서 멀어질수록 비슷한 정도로 코어 블록에 대한 상용성이 감소한다. 이러한 결과는 휘발유 등 n-alkane 기반의 혼합 유기 용매 내에서 용매의 비율을 잘 조절함으로써 CMT 등 미셀 구조를 잘 제어할 수 있음을 제시하고 있다. 따라서 이를 응용하면 n-alkane과 같이 오일 기반 미셀 용액에서 미셀 구조에 기인한 다양한 용액 특성을 조절할 수 있을 것이라 시사한다.
|
Figure 1 SAXS profiles for (a) SEP-1; (b) SEP-2 in n-alkanes at 40 oC. Dots are SAXS results and the solid curves are the best fit to the detailed fitting model. Data are vertically shifted for clarity. |
|
Figure 2 Temperature dependence of the core radius Rc for 1 wt% (a) SEP-1; (b) SEP-2 micelles in n-alkanes: n-hexadecane (square), ntetradecane (triangle), n-dodecane (revers triangle), n-decane (rhombus), n-octane (pentagon). Open and filled symbols are measured upon heating and cooling, respectively. Twice the unperturbed radius of gyration for the core block (2 |
|
Figure 3 Temperature dependence of aggregation number for 1 wt% (a) SEP-1; (b) SEP-2 micelles in n-alkanes: n-hexadecane (square), ntetradecane (triangle), n-dodecane (revers triangle), n-decane (rhombus), n-octane (pentagon). Open and filled symbols are measured upon heating and cooling, respectively. |
|
Figure 4 Temperature dependence of solvent fraction in the core for 1 wt% (a) SEP-1; (b) SEP-2 micelles in n-alkanes: n-hexadecane (square), n-tetradecane (triangle), n-dodecane (revers triangle), n-decane (rhombus), n-octane (pentagon). Open and filled symbols are measured upon heating and cooling, respectively. |
|
Figure 5 Temperature dependence of brush density for 1 wt% (a) SEP-1; (b) SEP-2 micelles in n-alkanes: n-hexadecane (square), n-tetradecane (triangle), n-dodecane (revers triangle), n-decane (rhombus), n-octane (pentagon). Open and filled symbols are measured upon heating and cooling, respectively. |
|
Figure 6 CMT-T dependence of the core radii for PS-b-PEP in n-alkanes 1 wt% dilute solution; (a) SEP-1; (b) SEP-2. Twice the unperturbed radius of gyration for the core block (2 |
|
Figure 7 CMT-T dependence of the solvent fraction in the cores for PS-b-PEP in n-alkanes 1 wt% dilute solution; (a) SEP-1; (b) SEP-2. |
|
Table 1 Calculated Flory-Huggins Interaction Parameters using Hildebrand’s Solubility Parameters |
본 연구는 다양한 크기의 n-alkane 내에서 블록공중합체 미셀의 코어 크기, 응집된 사슬 수, 코어 내 용매 분율, 코로나 사슬의 구조 등을 SAXS와 SLS를 통해 분석하였다. 용매의 크기가 작아질수록 용해도에 기반한 χ는 증가하지만, CMT가 더 낮은 것을 확인하였다. 이는 용매의 엔트로피 효과로 인해 작은 용매일수록 코어 침투가 용이하기 때문이다. 또한, CMT-T에 따른 미셀 구조적 경향성이 거의 일치하는 것을 확인하였다. 결과적으로 n-alkane 용매를 이용할 때 용매의 크기에 따른 엔탈피-엔트로피 기여도를 이해하고 이를 이용해 미셀의 구조를 체계적으로 조절할 수 있음을 보여주었다. 나아가 체계적으로 조절된 용매의 크기는 미셀의 구조를 제어 할 수 있는 변수로 이용이 가능함을 보여주었다. 이는 미셀의 구조를 제어하는 다양한 변수들 중에서 쉽게 이용할 수 있는 변수로 생각되며 미셀 구조의 제어를 필요로 하는 응용분야를 확장시킬 수 있음을 시사한다. 또한 오일과 같은 다양한 크기의 용매가 혼합된 용매를 이용할 때 미셀의 구조를 예측하고 제어하는데 필요한 기초연구로 판단된다.
- 1. Choi, S.; Bates, F.; Lodge, T. Molecular Exchange in Ordered Diblock Copolymer Micelles. Macromolecules 2011, 44, 3594-3604.
-

- 2. Van Der Kooij, H.; Spruijt, E.; Voets, I.; Fokkink, R.; Cohen Stuart, M.; Van Der Gucht, J. on the Stability and Morphology of Complex Coacervate Core Micelles: From Spherical to Wormlike Micelles. Langmuir 2012, 28, 14180-14191.
-

- 3. Spruijt, E.; Leermakers, F.; Fokkink, R.; Schweins, R.; Van Well, A.; Cohen Stuart, M.; Van Der Gucht, J. Structure and Dynamics of Polyelectrolyte Complex Coacervates Studied by Scattering of Neutrons, X-rays, and Light. Macromolecules 2013, 46, 4596-4605.
-

- 4. Gohy, J.; Varshney, S.; Antoun, S.; Jérôme, R. Water-Soluble Complexes Formed by Sodium Poly(4-styrenesulfonate) and a Poly(2-vinylpyridinium)-block-poly(ethyleneoxide) Copolymer. Macromolecules 2000, 33, 9298-9305.
-

- 5. Riess, G. Micellization of Block Copolymers. Prog. Polym. Sci. 2003, 28, 1107-1170.
-

- 6. Babi, J.; Zhu, L.; Lin, A.; Uva, A.; El‐Haddad, H.; Peloewetse, A.; Tran, H. Self‐assembled Free‐floating Nanomaterials from Sequence‐defined Polymers. J. Polym. Sci. 2021, ASAP.
-

- 7. Voets, I.; de Keizer, A.; Cohen Stuart, M. Complex Coacervate Core Micelles. Adv. Colloid Interface Sci. 2009, 147-148.
-

- 8. Gohy, J. F. Block Copolymer Micelles. Adv. Polym. Sci. 2005, 190, 65-136.
-

- 9. Hiemenz, P.; Lodge, T. Polymer Chemistry, 2nd Edition; CRC Press, Taylor & Francis Group: Boca Raton, 2007.
- 10. Hamley, I.; Block Copolymers in Solution: Fundamentals and Applications; John Wiley and Sons: Chichester, 2005; pp 7-104.
- 11. Bates, F. Polymer-Polymer Phase Behavior. Science 1991, 251, 898-905.
-

- 12. Halperin, A.; Tirrell, M.; Lodge, T. Tethered Chains in Polymer Microstructures. Adv. Polym. Sci. 1992, 100, 31-71.
-

- 13. Milner, S. Polymer Brushes. Science 1991, 251, 905-914.
-

- 14. Leibler, L.; Orland, H.; Wheeler, J. Theory of Critical Micelle Concentration for Solutions of Block Copolymers. J. Chem. Phys. 1983, 79, 3550-3557.
-

- 15. Nagarajan, R. Thermodynamics of Nonionic Polymer-micelle Association.Colloids Surf. 1985, 13, l-17.
-

- 16. Lund, R.; Willner, L.; Stellbrink, J.; Radulescu, A.; Richter, D. Role of Interfacial Tension for the Structure of PEP-PEO Polymeric Micelles. A Combined SANS and Pendant Drop Tensiometry Investigation. Macromolecules2004, 37, 9984-9993.
-

- 17. Ma, Y.; Lodge, T. Poly(methyl methacrylate)-block-poly(n-butyl methacrylate) Diblock Copolymer Micelles in an Ionic Liquid: Scaling of Core and Corona Size with Core Block Length. Macromolecules 2016, 49, 3639-3646.
-

- 18. Lund, R.; Willner, L.; Richter, D. Kinetics of Block Copolymer Micelles Studied by Small-Angle Scattering Methods. Adv. Polym. Sci. 2013, 259, 51-158.
-

- 19. Kelley, E.; Smart, T.; Jackson, A.; Sullivan, M.; Epps, T. Structural Changes in Block Copolymer Micelles Induced by Cosolvent Mixtures. Soft Matter 2011, 7, 7094-7102.
-

- 20. Cooksey, T.; Singh, A.; Le, K.; Wang, S.; Kelley, E.; He, L.; Robertson, M. Tuning Biocompatible Block Copolymer Micelles by Varying Solvent Composition: Core/Corona Structure and Solvent Uptake. Macromolecules 2017, 50, 4322-4334.
-

- 21. Wang, E.; Zhu, J.; Zhao, D.; Xie, S.; Bates, F.; Lodge, T. Effect of Solvent Selectivity on Chain Exchange Kinetics in Block Copolymer Micelles. Macromolecules. Macromolecules 2020, 53, 417-426.
-

- 22. Choi, S.; Lee, W.; Lodge, T.; Bates, F. Structure of Poly(styrene-b-ethylene-alt-propylene) Diblock Copolymer Micelles in Binary Solvent Mixtures. J. Polym. Sci. B: Polym. Phys. 2016, 54, 22-31.
-

- 23. Quintana, J.; Villacampa, M.; Andrio, A.; Munoz, M.; Katime, I. Micellization of a Polystyrene-block-poly(Ethylene/propylene) Copolymer in n-alkanes. 2. Structural Study. Macromolecules 1992, 25, 3129-3136.
-

- 24. Lund, R.; Willner, L.; Lindner, P.; Richter, D. Structural Properties of Weakly Segregated PS-PB Block Copolymer Micelles in n-Alkanes: Solvent Entropy Effects. Macromolecules 2009, 42, 2686-2695.
-

- 25. Imre, A.; Alexander, W.; Hook, V. The Effect of Branching of Alkanes on the Liquid-liquid Equilibrium of Oligostyrene/alkane Systems. Fluid Ph. Equilibria 2001, 187-188, 363-372.
-

- 26. Choi, S.; Bates, F.; Lodge, T. Structure of Poly(styrene-b-ethylene-alt-propylene) Diblock Copolymer Micelles in Squalane. J. Phys. Chem. B 2009, 113, 13840-13848.
-

- 27. Fetters, L.; Lohse, D.; Richter, D.; Witten, T.; Zirkelt, A. Connection between Polymer Molecular Weight, Density, Chain Dimensions, and Melt Viscoelastic Properties. Macromolecules 1994, 27, 4639-4647.
-

- 28. Itakura, M.; Shimada, K.; Matsuyama, S.; Saito, T.; Kinugasa, S. A convenient method to determine the Rayleigh Ratio with Uniform Polystyrene Oligomers. J. Appl. Polym. Sci. 2006, 99, 1953-1959.
-

- 29. Pedersen, J. S.; Gerstenberg, M. C. Scattering Form-Factor of Block-Copolymer Micelles. Macromolecules 1996, 29, 1363-1365.
-

- 30. Bang, J.; Viswanathan, K.; Lodge, T. P.; Park, M. J.; Char, K. H. Temperature-dependent Micellar Structures in Poly(styrene-b-isoprene) Diblock Copolymer Solutions Near the Critical Micelle Temperature. J. Chem. Phys. 2004, 121, 11489-11500.
-

- 31. Belmares, M.; Blanco, M.; Goddard, W.; Ross, R.; Caldwell, G.; Chou, S.; Pham, J.; Olofson, P.; Thomas, C. Hildebrand and Hansen Solubility Parameters from Molecular Dynamics with Applications to Electronic Nose Polymer Sensors. J. Comput. Chem.2004, 25, 1814-1826.
-

- 32. Díaz, E.; Cazurro, A.; Ordóñez, S.; Vega, A.; Coca, J. Determination of Solubility Parameters and Thermodynamic Properties in Hydrocarbon-solvent Systems by Gas Chromatography. Braz. J. Chem. Eng. 2007, 24, 293-306.
-

- 33. Zhu, J.; Balieu, R.; Wang, H. The Use of Solubility Parameters and Free Energy Theory for Phase Behaviour of Polymer-modified Bitumen: A Review. Road Mater. Pavement Des. 2019, 1-22.
-

- 34. Cheng, G.; Hammouda B.; Perahia, D. Effects of Intermicellar Interactions on the Dissociation of Block Copolymer Micelles: SANS and NMR Studies. Macromol. Chem. Phys. 2014, 215, 341-350.
-

- 35. Kambour, R.; Gruner, C.; Romagosa, E. Solvent Crazing of “dry” Polystyrene and “dry” Crazing of Plasticized Polystyrene. J. Polymer. Sci. 1973, 11, 1879-1890.
-

- 36. Evans, C.; Henderson, K.; Saathoff, J.; Shull, K.;Torkelson, J. Simultaneous Determination of Critical Micelle Temperature and Micelle Core Glass Transition Temperature of Block Copolymer-Solvent Systems via Pyrene-Label Fluorescence. Macromolecules 2013, 46, 4131-4140.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(1): 135-143
Published online Jan 25, 2022
- 10.7317/pk.2022.46.1.135
- Received on Oct 26, 2021
- Revised on Nov 8, 2021
- Accepted on Nov 8, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Soo-Hyung Choi
-
Department of Chemical Engineering, Hongik University, Seoul 04066, Korea
- E-mail: shchoi@hongik.ac.kr
- ORCID:
0000-0002-4078-6285










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.